摘要:69.图中③.⑤处的地形为 ( ) A.③是山顶.⑤是盆地 B.都是盆地 C.③是火山口.⑤是平原 D.都是高原
网址:http://m.1010jiajiao.com/timu3_id_46864[举报]
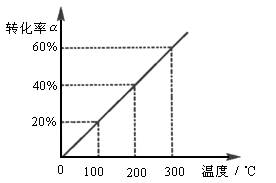
已知存在反应:X(g)+2Y(g)ƒ2Z(g),现将X和Y按体积比1∶2混合于一密闭容器中,并加压到3´107Pa时达平衡状态,此时反应物、生成物的物质的量之比为6∶1,则此时对应于图中坐标上的温度为( )
A.300℃ B.100℃ C.200℃ D.400℃
查看习题详情和答案>>
某研究性学习小组设计了一组实验来探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成同主族元素C和Si的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律,图2中A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润的红纸.
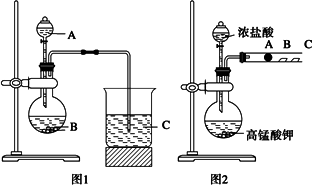
已知常温下浓盐酸与高锰酸钾能反应生成氯气.
(1)从以下所给物质中选出甲同学设计的实验所用到物质:
图1中试剂A为________(填代号);
①稀HNO3溶液 ②浓盐酸 ③碳酸钙 ④Na2SO3溶液 ⑤SiO2
写出图1烧瓶中发生反应的离子方程式________.
(2)甲同学所做实验图1烧杯中现象为________________;
(3)乙同学所做实验图2中B处的现象为________________;
(4)写出图2中A处发生反应的离子方程式:________.
某研究性学习小组设计了一组实验来探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成同主族元素C和Si的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素的性质递变规律,图2中A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润的红纸.(已知常温下浓盐酸与高锰酸钾能反应生成氯气).

(1)甲同学设计的实验,固体B为大理石,试剂A为
①稀硝酸 ②浓盐酸 ③NaOH溶液 ④Na2SiO3溶液
(2)写出图1烧瓶中发生反应的离子方程式
(3)甲同学所做实验图1烧杯中现象为
(4)乙同学所做实验图2中B处的现象为
(5)写出图2中A处发生反应的离子方程式
(6)乙同学用图2来完成实验验证卤素单质氧化性:Cl2>Br2>I2,你认为合理吗?
查看习题详情和答案>>

(1)甲同学设计的实验,固体B为大理石,试剂A为
①
①
(填序号);①稀硝酸 ②浓盐酸 ③NaOH溶液 ④Na2SiO3溶液
(2)写出图1烧瓶中发生反应的离子方程式
2H++CaCO3=Ca2++H2O+CO2↑
2H++CaCO3=Ca2++H2O+CO2↑
;(3)甲同学所做实验图1烧杯中现象为
出现白色沉淀
出现白色沉淀
;(4)乙同学所做实验图2中B处的现象为
湿润的淀粉KI试纸变蓝
湿润的淀粉KI试纸变蓝
;(5)写出图2中A处发生反应的离子方程式
Cl2+2Br-=Br2+2Cl-
Cl2+2Br-=Br2+2Cl-
;(6)乙同学用图2来完成实验验证卤素单质氧化性:Cl2>Br2>I2,你认为合理吗?
不合理
不合理
(填“合理”或“不合理”)理由是通过B的气体主要是Cl2,即不能说明氧化性Br2>I2
通过B的气体主要是Cl2,即不能说明氧化性Br2>I2
.关于化学反应中能量变化的说法不符合事实的是( )
| A、化学键断裂吸收能量,化学键生成放出能量 | B、化学反应中有物质变化也有能量变化 | C、需要加热的化学反应不一定是吸热反应 | D、图中所示的反应为放热反应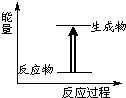 |
 第四周期的Cr、Fe、Co、Ni、Cu、Zn等许多金属能形成配合物.
第四周期的Cr、Fe、Co、Ni、Cu、Zn等许多金属能形成配合物.(1)Cr的核外电子排布式为
1s22s22p63s23p63d54s1
1s22s22p63s23p63d54s1
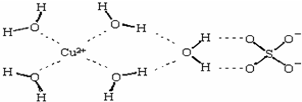
;(2)科学家通过X射线测得胆矾结构示意图可简单表示如下:图中虚线表示的作用力为
氢键、配位键
氢键、配位键
;(3)胆矾溶液与氨水在一定条件下可以生成Cu(NH3)4SO4?H2O晶体.在Cu(NH3)4SO4?H2O晶体中,[Cu(NH3)4]2+ 为平面正方形结构,则呈正四面体结构的原子团是
SO42-
SO42-
,该原子团中心原子的杂化轨道类型是sp3
sp3
;(4)在一定条件下,Cu+比Cu2+稳定,请解释其原因:
Cu+基态离子的价电子排布为3d10,Cu2+基态离子的价电子排布为3d9,前者为半充满,所以Cu+比Cu2+稳定
Cu+基态离子的价电子排布为3d10,Cu2+基态离子的价电子排布为3d9,前者为半充满,所以Cu+比Cu2+稳定
(5)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈正四面体构型.试推测四羰基镍的晶体类型是
分子晶体
分子晶体
,Ni(CO)4易溶于BC
BC
.A.水 B.四氯化碳 C.苯 D.硫酸镍溶液.