摘要:57.经济理论界专家认为.从证券市场发展看.应对国有企业和非国有企业采取平等态度私营企业上市对中国股票市场健康发展有重要意义.这一看法 ①充分肯定我国私营经济的主体地位 ②正确看到了私营经济对我国经济发展的重要作用 ③错误地认为国有经济和非国有经济应该实行同样的政策 ④主张各种经济成分应平等对待 A.①② B.②③ C.①④ D.②④
网址:http://m.1010jiajiao.com/timu3_id_46852[举报]
含氮废水(氮元素主要以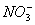 形式存在)对水体造成的污染越来越严重,若利用金属镁可以除去pH=7的某水体中的
形式存在)对水体造成的污染越来越严重,若利用金属镁可以除去pH=7的某水体中的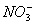 使之转化为N2,溶液变为碱性从而消除污染,但专家认为用金属铝消除氮的污染比镁更经济,其反应原理和金属镁相同。
使之转化为N2,溶液变为碱性从而消除污染,但专家认为用金属铝消除氮的污染比镁更经济,其反应原理和金属镁相同。
(1)写出镁和含氮废水中的![]() 反应的离子方程式:
反应的离子方程式:
_____________________________________________________________________。
(2)已知金属镁是从海水中提取的无水MgCl2电解制得的,若处理![]() 的浓度为0.2 mol/m3)需用含MgCl20.5%(质量分数)的海水_________t。
的浓度为0.2 mol/m3)需用含MgCl20.5%(质量分数)的海水_________t。
(3)若要用金属铝除去含![]() 0.3mol废水中的氮,(设氮元素均以
0.3mol废水中的氮,(设氮元素均以![]() 的形式存在)至少需消耗金属铝__________g。
的形式存在)至少需消耗金属铝__________g。
含氮废水进人水体而对环境造成的污染越来越严重,环境专家认为可以用金属铝将水体中的NO3-还原为N2,从而消除污染.其反应的离子方程式是:
6NO3-+10Al+6H2O=3N2↑+4Al(OH)3+6AlO2-
(1)现在要除去含氮元素0.3mol的废水中的NO3-(设氮元素都以NO3-的形式存在,下同),则至少需要消耗金属铝 g.
(2)有人认为金属镁比铝能更快消除氮的污染,反应原理和金属铝相同,其反应的离子方程式是:
2NO3-+5Mg+6H2O=N2↑+5Mg(OH)2+2OH-.
已知金属镁是从海水中提取的MgCl2通过电解[MgCl2(熔融)
Mg+Cl2].若要除去含氮元素0.3mol的废水中的NO3-,则至少需要含0.5%(质量分数)MgCl2的海水 kg.
查看习题详情和答案>>
6NO3-+10Al+6H2O=3N2↑+4Al(OH)3+6AlO2-
(1)现在要除去含氮元素0.3mol的废水中的NO3-(设氮元素都以NO3-的形式存在,下同),则至少需要消耗金属铝
(2)有人认为金属镁比铝能更快消除氮的污染,反应原理和金属铝相同,其反应的离子方程式是:
2NO3-+5Mg+6H2O=N2↑+5Mg(OH)2+2OH-.
已知金属镁是从海水中提取的MgCl2通过电解[MgCl2(熔融)
| ||
资料1:精制碘盐的成分为NaCl和KIO3,其中碘的含量为20~40mg?kg-1.
资料2:日本地震导致福岛两座核电站反应堆发生故障,铯和碘的放射性同位素大量外泄.
资料3:专家认为,每天服用1片碘片(含碘量100mg)可有效减小人体甲状腺对放射性碘的吸收.
请认真阅读以上资料,并回答下列问题:
(1)铯在周期表中的位置是
(2)下列物质中与KIO3属于同一类物质的是
①HIO3 ②碘酸钠 ③KOH ④I2O5 ⑤NaCl
(3)向碘盐的溶液中加入白醋和KI,再滴入淀粉溶液,溶液呈蓝色,则发生反应的离子方程式为
(4)若用精制碘盐来预防放射性碘对人体的伤害,是否可行?
查看习题详情和答案>>
资料2:日本地震导致福岛两座核电站反应堆发生故障,铯和碘的放射性同位素大量外泄.
资料3:专家认为,每天服用1片碘片(含碘量100mg)可有效减小人体甲状腺对放射性碘的吸收.
请认真阅读以上资料,并回答下列问题:
(1)铯在周期表中的位置是
第六周期ⅠA族
第六周期ⅠA族
.(2)下列物质中与KIO3属于同一类物质的是
②
②
(填序号).①HIO3 ②碘酸钠 ③KOH ④I2O5 ⑤NaCl
(3)向碘盐的溶液中加入白醋和KI,再滴入淀粉溶液,溶液呈蓝色,则发生反应的离子方程式为
IO3-+5I-+6CH3COOH=3I2+6CH3COO-+3H2O
IO3-+5I-+6CH3COOH=3I2+6CH3COO-+3H2O
.(4)若用精制碘盐来预防放射性碘对人体的伤害,是否可行?
不行
不行
(填“行”、“不行”),原因是因为从精致食盐中摄入的碘量达不到规定的量
因为从精致食盐中摄入的碘量达不到规定的量
.含氮废水进入水体而对环境造成的污染越来越严重,环境专家认为可以用金属铝将水体中的NO3-还原为N2,从而消除污染.
其反应的离子方程式是:6NO3-+10Al+18H2O→3N2↑+10Al(OH)3+6OH-
(1)现在要除去1m3含氮元素0.3mol的废水中的NO3-(设氮元素都以NO3-的形式存在,下同),则至少需要消耗金属铝
(2)有人认为金属镁比铝能更快消除氮的污染,其反应原理和金属铝相同;
①写出镁和含氮废水反应的离子方程式
②已知金属镁是从海水中提取的MgCl2,通过电解制得的.若要除去1m3含氮元素0.3mol的废水中的NO3-,则至少需要含0.5%(质量分数)MgCl2的海水
查看习题详情和答案>>
其反应的离子方程式是:6NO3-+10Al+18H2O→3N2↑+10Al(OH)3+6OH-
(1)现在要除去1m3含氮元素0.3mol的废水中的NO3-(设氮元素都以NO3-的形式存在,下同),则至少需要消耗金属铝
13.5
13.5
g;(2)有人认为金属镁比铝能更快消除氮的污染,其反应原理和金属铝相同;
①写出镁和含氮废水反应的离子方程式
2NO3-+5Mg+6H2O═N2↑+5Mg(OH)2+2OH-
2NO3-+5Mg+6H2O═N2↑+5Mg(OH)2+2OH-
;②已知金属镁是从海水中提取的MgCl2,通过电解制得的.若要除去1m3含氮元素0.3mol的废水中的NO3-,则至少需要含0.5%(质量分数)MgCl2的海水
14.25
14.25
kg.(8分)含氮废水进入水体而对环境造成的污染越来越严重,环境专家认为可以用金属铝将水体中的NO3-还原为N2,从而消除污染。其反应的离子方程式是:
6NO3-+ 10Al + 18H2O → 3N2↑+ 10Al(OH)3+ 6OH-
(1)现在要除去1m3含氮元素0.3mol的废水中的NO3-(设氮元素都以NO3-的形式存在,下同),则至少需要消耗金属铝__________g。
(2)有人认为金属镁比铝能更快消除氮的污染,其反应原理和金属铝相同。
① 写出镁和含氮废水反应的离子方程式:___________________________________
② 已知金属镁是从海水中提取的MgCl2,通过电解制得的。若要除去1m3含氮元素0.3mol的废水中的NO3-,则至少需要含0.5%(质量分数)MgCl2的海水_________kg。
查看习题详情和答案>>