摘要:B 两种物质的电荷平衡关系分别如下: NaF: [Na+]+[H+] = [F-]+[OH-]-----------① NaCN: [Na+]+[H+] = [CN-]+[OH-]---------② 因为HF比HCN易电离.所以NaF的水解程度比NaCN水解程度小.在这两种溶液中.NaF溶液中的[OH-]比NaCN溶液中的[OH-]小.反之. NaF溶液中的[H+]比NaCN溶液中的[H+]大;由于[NaF]与[NaCN]相同.即[Na+]相同.推知①左边大于②式左边. ①式右边也大于②式右边.所以可得: [Na+]+[H+]+[F-]+[OH-]>[Na+]+[H+]+[CN-]+[OH-].
网址:http://m.1010jiajiao.com/timu3_id_46376[举报]
 (2011?四川模拟)在1L密闭容器中,充入一定量的A发生反应:A(g)
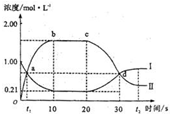
(2011?四川模拟)在1L密闭容器中,充入一定量的A发生反应:A(g)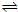 2B(g)(正反应为放热反应).当反应达到平衡后,改变影响平衡的一个条件,反应达到新的平衡.如图Ⅰ、Ⅱ两曲线分别表示整个反应过程中两种物质的浓度变化关系.下列说法正确的是( )
2B(g)(正反应为放热反应).当反应达到平衡后,改变影响平衡的一个条件,反应达到新的平衡.如图Ⅰ、Ⅱ两曲线分别表示整个反应过程中两种物质的浓度变化关系.下列说法正确的是( )
查看习题详情和答案>>
|
一定条件下,将X和Y两种物质按不同比例放入密闭容器中,反应达到平衡后,测得X、Y转化率与起始时两种物质的量之比[n(X)/n(Y)]的关系如图,则X和Y反应的方程式可表示为
| |
| [ ] | |
A. |
X+3Y |
B. |
3X+Y |
C. |
3X+2Y |
D. |
2X+3Y |




