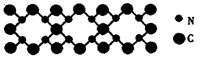
摘要:化学键.晶体类型及性质(近10年来的化学高考命题中的呈现率:70%) [点题]最近发现一种有钛原子和碳原子构成的气态团簇分子.结构如NaCl晶体图所示.顶角和面心的原子是钛原子.棱的中心和体心的原子是碳原子.它的化学式为 . [点晴] 错误解答:由结构图可知.顶点上的原子被8个晶胞共用.面心上的原子被两个晶胞共用.棱的中心的原子被4个晶胞共用.而体心中的原子被一个晶胞专用.根据这样的思路:每个晶胞中Ti的个数为8*=4,C的个数为1+12*(1/4)=4.因此每个晶胞中有4个Ti和4个C.该物质的化学式为Ti4C4.错误原因:忽略指定的结构为“气态团簇分子 .把它按常规的“晶胞 处理.正确解答:由于该结构为“气态团簇分子 .给出的结构就是一个“完整 的分子.因此结构中的每个原子都是构成分子的一部分.由于该“气态团簇分子 结构含有14个Ti和13个C.于是该物质的化学式为Ti14C13. [点题] 纳米材料的表面粒子占总粒子数比例极大.这是它有许多特殊性质的主要 原因.假设某纳米颗粒的大小和结构恰好与氯化钠晶胞相同 .则这种纳米颗粒的表面粒子数与总粒子数的比值为 A.7:8 B.13:14 C.25:26 D.26:27 [点晴] D . [点题]下列说法中正确的是 A.冰.水和水蒸气中都存在氢键 B.除稀有气体外的非金属元素都能生成不同价态的含氧酸 C.金属离子和自由电子间通过金属键形成的晶体是金属晶体 D.CO2与SiO2都是分子晶体.所以它们有接近的熔.沸点 [点晴] 水分子之间存在形成氢键.水蒸气中不一定含有氢键,B中F.O没有含氧酸,D中SiO2是原子晶体.故选C. [点题]钛酸钡的热稳定性好.且介电常数高.它在小型变压器中应用很多.在话筒和扩音器中用作陶瓷变频器.其晶体结构示意如图.试回答:
网址:http://m.1010jiajiao.com/timu3_id_46030[举报]
关于化学键或晶体类型的下列叙述中,错误的是
A.非金属元素间形成的化合物不可能有离子键
B.离子化合物中可能含有极性共价键或非极性共价键
C.同族元素的氧化物可以形成不同类型的晶体
D.不同族元素的氧化物可以形成相同类型的晶体
查看习题详情和答案>>
下列说法正确的是?
A.质子数相等,电子数也相等的两种粒子可能是不同的离子?
B.CaF2和Na2O2的化学键和晶体类型均相同?
C.C6H6、SiO2、CO2均为分子晶体?
D. ![]() 属于化学变化
属于化学变化