摘要: 钢铁发生电化腐蚀时正极发生的反应可能是 ( ) A.2H+ + 2e- = H2↑ B.2H2O +O2 +4e- = 4OHˉ C.Fe - 2e- = Fe2+ D.4OHˉ - 4e- = 2H2O + O2↑
网址:http://m.1010jiajiao.com/timu3_id_45382[举报]
钢铁发生电化学腐蚀时,如果钢铁表面吸附的水膜呈酸性,则发生
________腐蚀,正极反应式为________,负极反应式为________.如果钢铁表面吸附的水膜酸性很弱或呈中性,则发生________腐蚀,正极反应式为________,负极反应式为________.钢铁工业是国家工业的基础,请回答钢铁腐蚀、防护过程中的有关问题.
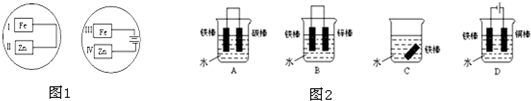
(1)若把锌片和铁片放在盛有食盐水和酚酞的表面皿中,如图1所示,能观察到酚酞变红的现象的区域是
(2)如图2所示各个装置中铁棒被腐蚀由易到难的顺序是
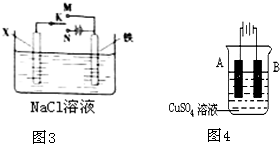
(3)利用如图3装置,可模拟铁的电化学防护,下列有关说法正确的是
A.若X为碳棒,为减缓铁的腐蚀,开关K应置于M处
B.若X为锌板,K置于M或N处,均能减缓铁的腐蚀
C.若X为碳棒,K置于M或N处,一段时间后溶液pH均不变
D.若X为碳棒,K置于M或N处,Cl-均向X电极移动
(4)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀.装置如图4,请回答:
①B电极对应的金属是
②若电镀前铁、铜两电极的质量相同,电镀完成后,若电镀时电路中通过的电子为0.2mol,将它们取出洗净、烘干、称量,则A、B两极质量相差
查看习题详情和答案>>

(1)若把锌片和铁片放在盛有食盐水和酚酞的表面皿中,如图1所示,能观察到酚酞变红的现象的区域是
Ⅰ、Ⅳ
Ⅰ、Ⅳ
(填I、II、III、IV),写出II处电极的电极反应式:Zn-2e-=Zn2+
Zn-2e-=Zn2+
;写出IV处电极的电极反应式:2H++2e-=H2↑
2H++2e-=H2↑
;写出该两种情况下发生的总反应的离子方程式:2Fe+O2+H2O=2Fe(OH)2
2Fe+O2+H2O=2Fe(OH)2
;Fe+2H2O
Fe(OH)2+H2↑
| ||
Fe+2H2O
Fe(OH)2+H2↑
.若把III的铁片改为碳棒,写出该处发生的电极反应式:
| ||
2Cl--2e-=Cl2↑
2Cl--2e-=Cl2↑
(2)如图2所示各个装置中铁棒被腐蚀由易到难的顺序是
ACBD
ACBD
(填字母)
(3)利用如图3装置,可模拟铁的电化学防护,下列有关说法正确的是
AB
AB
(填字母)A.若X为碳棒,为减缓铁的腐蚀,开关K应置于M处
B.若X为锌板,K置于M或N处,均能减缓铁的腐蚀
C.若X为碳棒,K置于M或N处,一段时间后溶液pH均不变
D.若X为碳棒,K置于M或N处,Cl-均向X电极移动
(4)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀.装置如图4,请回答:
①B电极对应的金属是
铁
铁
(写元素名称),A电极的电极反应式是Cu-2e-=Cu2+
Cu-2e-=Cu2+
②若电镀前铁、铜两电极的质量相同,电镀完成后,若电镀时电路中通过的电子为0.2mol,将它们取出洗净、烘干、称量,则A、B两极质量相差
12.8
12.8
g.