摘要:4.已知某温度下.N2(g)+3H2(g)≒ 2NH3(g),△H=-92.4 kJ/mol现有恒温.恒容且体积相 同的两个密闭容器A.B.A中通入1mol N2.3 mol H2.B中通入0.5 mol N2.1.5 mol H2. 反应一段时间后.测得两个容器中气体密度均不发生变化.下列判断正确的是 A.A中吸热92.4 kJ B.B中吸热46.2 kJ C.A中热量变化值一定大于B的2倍 D.A.B中平衡状态相同
网址:http://m.1010jiajiao.com/timu3_id_44944[举报]
已知某温度下:N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ?mol-1,恒温、恒容且容积相同的两个密闭容器A、B,A中通入1mol N2、3mol H2,B中通入0.5mol N2、1.5mol H2,反应一段时间后,A、B中均达到平衡状态.下列判断正确的是( )
查看习题详情和答案>>
已知某温度下:N2(g)+3H2(g) 2NH3(g);ΔH=-92.4 kJ·mol-1。现有恒温、恒容且容积相同的两个密闭容器A、B,A中通入1 mol N2、3mol H2,B中通入0.5 mol N2、1.5 mol H2,反应一段时间后,A、B中均达到平衡状态。下列判断正确的是…( )
2NH3(g);ΔH=-92.4 kJ·mol-1。现有恒温、恒容且容积相同的两个密闭容器A、B,A中通入1 mol N2、3mol H2,B中通入0.5 mol N2、1.5 mol H2,反应一段时间后,A、B中均达到平衡状态。下列判断正确的是…( )
A.A中吸热92.4 kJ B.A中热量变化值大于B中的2倍
C.B中放热46.2 kJ D.A中热量变化值等于B中的2倍
查看习题详情和答案>>已知某温度下,N2(g)+3H2(g)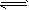 2NH3(g);△H=-92.4 kJ/mol;现有恒温、恒容且体积相同的两个密闭容器A、B,A中通入1mol N2、3mol H2,B中通入0.5mol N2、1.5mol H2,反应一段时间后,测得两个容器内压强均不再发生变化。下列判断正确的是
2NH3(g);△H=-92.4 kJ/mol;现有恒温、恒容且体积相同的两个密闭容器A、B,A中通入1mol N2、3mol H2,B中通入0.5mol N2、1.5mol H2,反应一段时间后,测得两个容器内压强均不再发生变化。下列判断正确的是
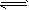 2NH3(g);△H=-92.4 kJ/mol;现有恒温、恒容且体积相同的两个密闭容器A、B,A中通入1mol N2、3mol H2,B中通入0.5mol N2、1.5mol H2,反应一段时间后,测得两个容器内压强均不再发生变化。下列判断正确的是
2NH3(g);△H=-92.4 kJ/mol;现有恒温、恒容且体积相同的两个密闭容器A、B,A中通入1mol N2、3mol H2,B中通入0.5mol N2、1.5mol H2,反应一段时间后,测得两个容器内压强均不再发生变化。下列判断正确的是[ ]
A.A中吸热92.4kJ
B.B中放热46.2kJ
C.A中热量变化值一定大于B的2倍
D.A、B中N2的体积分数相同
查看习题详情和答案>>
B.B中放热46.2kJ
C.A中热量变化值一定大于B的2倍
D.A、B中N2的体积分数相同
已知某温度下:N2(g)+3H2(g)![]() 2NH3(g)ΔH=-92.4 kJ·mol-1,恒温、恒容且容积相同的两个密闭容器A、B,A中通入1 mol N2、3 mol H2,B中通入0.5 mol N2、1.5 mol H2,反应一段时间后,A、B中均达到平衡状态。下列判断正确的是 ( )
2NH3(g)ΔH=-92.4 kJ·mol-1,恒温、恒容且容积相同的两个密闭容器A、B,A中通入1 mol N2、3 mol H2,B中通入0.5 mol N2、1.5 mol H2,反应一段时间后,A、B中均达到平衡状态。下列判断正确的是 ( )
A.A中N2转化率小于B中2倍 B.A中放热小于B中的2倍
C.A中放热大于B中的2倍 D.A中N2浓度大于B中2倍
查看习题详情和答案>> (2011?南京二模)三效催化转化器可减少汽车尾气中的主要污染物(CO、NOx等),部分反应如下:
(2011?南京二模)三效催化转化器可减少汽车尾气中的主要污染物(CO、NOx等),部分反应如下:①2NO(g)+2CO(g)=N2(g)+2CO2(g) ②CO(g)+H2O(g)?H2(g)+CO2(g)
(1)已知:N2(g)+O2(g)=2NO(g)△H=+180.5kJ?mol-1
2C (s)十O2(g)=2CO(g)△H=-221.0kJ?mol-1
C (s)十O2(g)=CO2(g)△H=-393.5kJ?mol-1
则反应①的△H=
-746.5kJ?mol-1
-746.5kJ?mol-1
.(2)已知某温度下,反应②的平衡常数K=1.0.在该温度下向某密闭容器中充入1.0mol CO和2.0molH2O,
经充分反应达平衡后,CO的平衡转化率为
66.7%
66.7%
,H2的体积分数为22.2%
22.2%
.(3)NaBH4/H2O2燃料电池是一种有广泛前景的汽车能源,结构如右图所示.电池工作时,负极发生的电极反应可表示为
BH4-+8OH--8e-=BO2-+6H2O
BH4-+8OH--8e-=BO2-+6H2O
.