摘要:14]. Al和Si.Ge和As在元素周期表金属和非金属过渡位置上.在其单质和化合物在建筑业.电子工业和石油化工等方面应用广泛.请回答下列问题: (1) As 的价层电子构型为 (2) AlCl3是化工生产中的常用催化剂.熔点为192.6℃.熔融状态以二聚体A12C16形式存在.其中铝原子与氯原子的成键类型是 (3) 超高导热绝缘耐高温纳米氮化铝(AlN)在绝缘材料中的应用广泛.AlN晶体与金刚石类似.每个Al原子与 个N原子相连.与同一个Al原子相连的N原子构成的空间构型为 .在四大晶体类型中.AlN属于 晶体. (4) Si和C 同主族.Si.C和O成键情况如下: 在C和O之间可以形成双键形成CO2分子.而Si和O则不能和碳那样形成有限分子原因是 . (5) SiCl4(l)常用作烟雾剂.原因Si存在3d轨道.能同H2O(l)配位而剧烈水解.在潮湿的空气中发烟.试用化学方程式表示其原理 .
网址:http://m.1010jiajiao.com/timu3_id_43545[举报]
蛇纹石矿可以看作由MgO、Fe2O3、Al2O3和SiO2组成.某实验小组设计如下流程欲分别制得单质Mg、Fe、Al和Si.
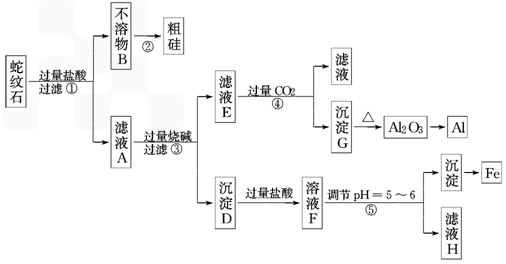
有关氢氧化物沉淀时的pH见下表
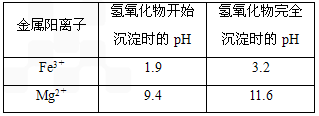
请回答下列问题:
(1)滤液A中含有的阳离子有___________________________________.
(2)操作②中涉及的化学方程式为_____________________________________________,操作④中生成沉淀G的离子方程式为_________________________________________.
(3)操作⑤中调节pH为5~6时,可以用到的试剂为(填序号)________.
a.NaOH溶液 b.氨水 c.MgO d.Mg(OH)2
(4)由滤液H制取金属Mg的流程如下
(1)滤液A中含有的阳离子有___________________________________.
(2)操作②中涉及的化学方程式为_____________________________________________,操作④中生成沉淀G的离子方程式为_________________________________________.
(3)操作⑤中调节pH为5~6时,可以用到的试剂为(填序号)________.
a.NaOH溶液 b.氨水 c.MgO d.Mg(OH)2
(4)由滤液H制取金属Mg的流程如下
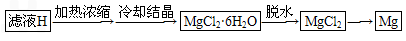
该流程中由MgCl2冶炼Mg的方法是________.在干燥的HCl气流中加热MgCl2·6H2O制取无水氯化镁的原因是__________________.
查看习题详情和答案>>
(2010?徐汇区二模)粉煤灰是燃煤电厂排出的工业废渣,其中含莫来石(Al6Si2O13)的质量分数为43.4%,还有含量较多的SiO2(其他成分不含Al和Si).用粉煤灰和纯碱在高温下烧结,可制取NaAlSiO4(霞石)、Na2SiO3和NaAlO2,有关化学方程式为:
Al6Si2O13+3Na2CO3→2NaAlSiO4+4NaAlO2+3CO2↑ ①
Al6Si2O13+5Na2CO3→2Na2SiO3+6NaAlO2+5CO2↑ ②
SiO2+Na2CO3→Na2SiO3+CO2↑ ③
(1)粉煤灰中铝的质量分数为
(2)用1mol Al6Si2O13和 4mol SiO2制得5mol NaAlO2、1mol NaAlSiO4,还应制得Na2SiO3
(3)若粉煤灰中 Al6Si2O13与 SiO2的物质的量之比为1:2,则1kg粉煤灰与6mol Na2CO3反应(反应物全部都参与反应),可制得NaAlO2
(4)若用100mol Al6Si2O13同时生产NaAlSiO4和NaAlO2,且n(NaAlSiO4):n(NaAlO2)=x,消耗Na2CO3y mol,试确定y与x的关系式
.
查看习题详情和答案>>
Al6Si2O13+3Na2CO3→2NaAlSiO4+4NaAlO2+3CO2↑ ①
Al6Si2O13+5Na2CO3→2Na2SiO3+6NaAlO2+5CO2↑ ②
SiO2+Na2CO3→Na2SiO3+CO2↑ ③
(1)粉煤灰中铝的质量分数为
16.5
16.5
%.(2)用1mol Al6Si2O13和 4mol SiO2制得5mol NaAlO2、1mol NaAlSiO4,还应制得Na2SiO3
5
5
mol,共消耗Na2CO38
8
mol(得到的固体中无SiO2).(3)若粉煤灰中 Al6Si2O13与 SiO2的物质的量之比为1:2,则1kg粉煤灰与6mol Na2CO3反应(反应物全部都参与反应),可制得NaAlO2
5.09
5.09
mol.(4)若用100mol Al6Si2O13同时生产NaAlSiO4和NaAlO2,且n(NaAlSiO4):n(NaAlO2)=x,消耗Na2CO3y mol,试确定y与x的关系式
| 500-100x |
| 1+x |
| 500-100x |
| 1+x |
粉煤灰是燃煤电厂排出的工业废渣,其中含莫来石(Al6Si2O13)的质量分数为43.4%,还有含量较多的SiO2(其他成分不含Al和Si)。用粉煤灰和纯碱在高温下烧结,可制取NaAlSiO4(霞石)、Na2SiO3和NaAlO2,有关化学方程式为:
Al6Si2O13+3Na2CO3→2NaAlSiO4+4NaAlO2+3CO2 ↑ ①
Al6Si2O13+5Na2CO3→2Na2SiO3+6NaAlO2+5CO2 ↑ ②
SiO2+Na2CO3→Na2SiO3+CO2 ↑ ③
(1)粉煤灰中铝的质量分数为 %。
(2)用l mol Al6Si2O13和4mol SiO2制得5mol NaAlO2、lmolNaAlSiO4,还应制得Na2SiO3 mol,共消耗Na2CO3 mol(得到的固体中无SiO2)。
(3)若粉煤灰中Al6Si2O13与SiO2的物质的量之比为1:2,则1妇粉煤灰与6molNa2CO3反应(反应物全部都参与反应),可制得NaAlO2 mol。
(4)若用100 mol Al6Si2O13同时生产NaAlSiO4和NaAlO2,且n(NaAlSiO4):n(NaAlO2)=x,消耗Na2CO3 ymol,试确定y与x的关系式。
查看习题详情和答案>>