摘要:13.一种光化学电池的结构如右图.当光照在表面涂有氯化银的银片上时.AgCl(s)Ag. [Cl表示生成的氯原子吸附在氯化银表面].接着Cl+e-→Cl-(aq).若将光源移除.电池会立即回复至初始状态.下列说法不正确的是 A.光照时.电流由X流向Y B.光照时.Pt电极发生的反应为:2Cl- +2e-=Cl2 C.光照时.Cl-向Ag电极移动 D.光照时.电池总反应为:AgCl(s) +Cu+(aq)Ag(s) +Cu2+(aq)+Cl-
网址:http://m.1010jiajiao.com/timu3_id_433942[举报]
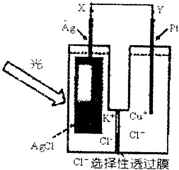 一种光化学电池的结构如图,当光照在表面涂有氯化银的银
一种光化学电池的结构如图,当光照在表面涂有氯化银的银片时,AgCl(s)
| 光 |
的氯原子吸附在氯化银表面],接着Cl(AgCl)+e-→Cl-(aq),
若将光源移除,电池会立即回复至初始状态.下列说法不正确
的是( )
| A、光照时,电流由X流向Y | ||
| B、光照时,Pt电极发生的反应为:2Cl--2e-=Cl2 | ||
| C、光照时,Cl-向Pt电极移动 | ||
D、光照时,电池总反应为:AgCl(s)+Cu+(aq)
|
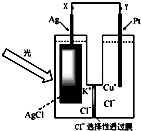 一种光化学电池的结构如图,当光照在表面涂有氯化银的银片上时,AgCl(s)
一种光化学电池的结构如图,当光照在表面涂有氯化银的银片上时,AgCl(s)| 光 |
| A、光照时,电流由X流向Y | ||
| B、光照时,Pt电极发生的反应为:2Cl-+2e-=Cl2 | ||
| C、光照时,Cl-向Ag电极移动 | ||
D、光照时,电池总反应为:AgCl(s)+Cu+(aq)
|
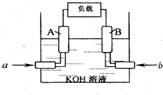 某甲烷一氧气燃料电池的结构如右图所示,该电池的两个电极均由多孔碳制成,以30%KOH溶液为电解质溶液,气体由多孔碳隙逸出并在电极表面放电,其总反应的化学方程式为:CH4+2O2+2KOH=K2CO3+3H2O。下列说法正确的是
某甲烷一氧气燃料电池的结构如右图所示,该电池的两个电极均由多孔碳制成,以30%KOH溶液为电解质溶液,气体由多孔碳隙逸出并在电极表面放电,其总反应的化学方程式为:CH4+2O2+2KOH=K2CO3+3H2O。下列说法正确的是
A.若b处通人的气体为氧气,则B极为正极
B.若有2 mol电子发生转移,则消耗的O2为5.6 L(标准状况)
C.放电一段时间后正极附近溶液的c(H+)增大
D.用多孔碳作电极是为了增大气体与溶液的接触面积
查看习题详情和答案>>