摘要:某温度时.将0.200mol的A气体充入2L抽空的密闭容器中.隔一定的时间对该容器内的物质进行分析.得到如下数据: 0 20 40 60 80 100 c(A)mol·L-1 0.100 0.470 0.050 c3 a b c(B)mol·L-1 0.000 0.060 c2 0.120 0.120 0.120 试填空: (1)该反应的化学方程式为 .表中c2 c3. a b. 若在相同情况下最初向该容器充入的是B气体.要达到上述同样的平衡状态.B的起始浓度是 mol·L-1. (2)在体积为l L的密闭容器中.充入lmol CO2和3mol H2.测得CO2和CH3OH(g)的浓度随时间变化如图所示. (I)从反应开始到平衡.甲醇的平均反应速率v(CH3OH)= , 该反应的平衡常数k= . (II)乙醇是重要的化工产品和液体燃料.同样可以利用CO2反应制取乙醇: 2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g) 25℃时.K=2.95×1011 在一定压强下.测得反应的实验数据如下表.分析表中数据回答下列问题: 500 600 700 800 1.5 45 33 20 12 2.0 60 43 28 15 3.0 83 62 37 22 ①温度升高.K值 (填“增大 .“减小 .或“不变 ). ②提高氢碳比[n(H2)/n(CO2)], K值 (填“增大 .“减小 .或“不变 ).
网址:http://m.1010jiajiao.com/timu3_id_432972[举报]
(14分)某温度时,将0.200mol的A气体充入2L抽空的密闭容器中,隔一定的时间对该容器内的物质进行分析,得到如下数据:
试填空:
(1)该反应的化学方程式为
(2)在体积为l L的密闭容器中,充入lmol CO2和3mol H2,测得CO2和CH3OH(g)的浓度随时间变化如图所示.

(I)从反应开始到平衡,甲醇的平均反应速率v(CH3OH)=
该反应的平衡常数k=
.
(II)乙醇是重要的化工产品和液体燃料,同样可以利用CO2反应制取乙醇:
2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g) 25℃时,K=2.95×1011
CH3CH2OH(g)+3H2O(g) 25℃时,K=2.95×1011
在一定压强下,测得反应的实验数据如下表.分析表中数据回答下列问题:
①温度升高,K值
②提高氢碳比[n(H2)/n(CO2)],K值
查看习题详情和答案>>
| 时间(S)浓度 | 0 | 20 | 40 | 60 | 80 | 100 |
| c(A)mol?L-1 | 0.100 | 0.070 | 0.050 | c3 | a | b |
| c(B)mol?L-1 | 0.000 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
(1)该反应的化学方程式为
A(g)=2B(g)
A(g)=2B(g)
,表中c2>
>
c3、a=
=
b(填>、<、=),若在相同情况下最初向该容器充入的是B气体,要达到上述同样的平衡状态,B的起始浓度是0.2
0.2
mol?L-1.(2)在体积为l L的密闭容器中,充入lmol CO2和3mol H2,测得CO2和CH3OH(g)的浓度随时间变化如图所示.

(I)从反应开始到平衡,甲醇的平均反应速率v(CH3OH)=
0.075mol?L-1?min-1
0.075mol?L-1?min-1
;该反应的平衡常数k=
| 16 |
| 3 |
| 16 |
| 3 |
(II)乙醇是重要的化工产品和液体燃料,同样可以利用CO2反应制取乙醇:
2CO2(g)+6H2(g)
 CH3CH2OH(g)+3H2O(g) 25℃时,K=2.95×1011
CH3CH2OH(g)+3H2O(g) 25℃时,K=2.95×1011在一定压强下,测得反应的实验数据如下表.分析表中数据回答下列问题:
 |
500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2.0 | 60 | 43 | 28 | 15 |
| 3.0 | 83 | 62 | 37 | 22 |
减小
减小
(填“增大”、“减小”、或“不变”).②提高氢碳比[n(H2)/n(CO2)],K值
不变
不变
(填“增大”、“减小”、或“不变”).(14分)某温度时,将0.200mol的A气体充入2L抽空的密闭容器中,隔一定的时间对该容器内的物质进行分析,得到如下数据:
试填空:
(1)该反应的化学方程式为______,表中c2______c3、a______b(填>、<、=),若在相同情况下最初向该容器充入的是B气体,要达到上述同样的平衡状态,B的起始浓度是______mol?L-1.
(2)在体积为l L的密闭容器中,充入lmol CO2和3mol H2,测得CO2和CH3OH(g)的浓度随时间变化如图所示.
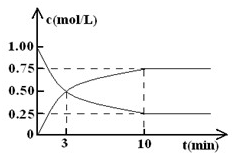
(I)从反应开始到平衡,甲醇的平均反应速率v(CH3OH)=______;
该反应的平衡常数k=______.
(II)乙醇是重要的化工产品和液体燃料,同样可以利用CO2反应制取乙醇:
2CO2(g)+6H2(g)
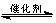
CH3CH2OH(g)+3H2O(g) 25℃时,K=2.95×1011
在一定压强下,测得反应的实验数据如下表.分析表中数据回答下列问题:
①温度升高,K值______(填“增大”、“减小”、或“不变”).
②提高氢碳比[n(H2)/n(CO2)],K值______(填“增大”、“减小”、或“不变”).
查看习题详情和答案>>
| 时间(S)浓度 | 0 | 20 | 40 | 60 | 80 | 100 |
| c(A)mol?L-1 | 0.100 | 0.070 | 0.050 | c3 | a | b |
| c(B)mol?L-1 | 0.000 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
(1)该反应的化学方程式为______,表中c2______c3、a______b(填>、<、=),若在相同情况下最初向该容器充入的是B气体,要达到上述同样的平衡状态,B的起始浓度是______mol?L-1.
(2)在体积为l L的密闭容器中,充入lmol CO2和3mol H2,测得CO2和CH3OH(g)的浓度随时间变化如图所示.

(I)从反应开始到平衡,甲醇的平均反应速率v(CH3OH)=______;
该反应的平衡常数k=______.
(II)乙醇是重要的化工产品和液体燃料,同样可以利用CO2反应制取乙醇:
2CO2(g)+6H2(g)
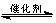
CH3CH2OH(g)+3H2O(g) 25℃时,K=2.95×1011
在一定压强下,测得反应的实验数据如下表.分析表中数据回答下列问题:
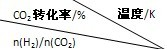 |
500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2.0 | 60 | 43 | 28 | 15 |
| 3.0 | 83 | 62 | 37 | 22 |
②提高氢碳比[n(H2)/n(CO2)],K值______(填“增大”、“减小”、或“不变”).