网址:http://m.1010jiajiao.com/timu3_id_43291[举报]
用下图所示装置(酒精灯、铁架台等未画出)制取三氯化磷,在曲颈甑d中放入足量白磷,将氯气迅速而又不间断地通入曲颈甑中,氯气与白磷就会发生反应,产生火焰。三氯化磷和五氯化磷的物理常数如下:
|
|
熔 点 |
沸 点 |
|
三氯化磷 |
-112℃ |
76℃ |
|
五氯化磷 |
148℃ |
200℃分解 |

(1)有浓盐酸、浓硫酸、白磷、二氧化锰、氢氧化钠等物质供选用。a、b中应该装入的试剂分别是:a________,b________。
(2)________仪器需要加热(填仪器对应的字母)。
(3)在蒸馏烧瓶e中收集生成的三氯化磷。为保证三氯化磷蒸气冷凝,应在水槽g中加入________。
(4)三氯化磷遇到水蒸气强烈反应,甚至发生爆炸,所以d、e仪器及装入其中的物质都不能含有水分。为除去氯气中的水分,c可以装入下列物质中的(填字母)________。
A.碱石灰
B.浓硫酸
C.无水氯化钙
(5)氯气和白磷反应放出大量的热,为使曲颈甑 d不致因局部过热而炸裂,实验开始前应在曲颈甑的底部放少量________。
(6)实验室的白磷保存于水中,取出白磷后用滤纸吸干表面水分,浸入无水酒精中片刻,再浸入乙醚中片刻即可完全除去水分。已知水与酒精互溶,酒精与乙醚互溶,用上述方法可除去水分的原因是________。
(7)为防止氯气污染空气,装置末端导出的气体最好用________(填字母)进行净化处理。
A.NaOH溶液
B.Ca(OH)2溶液
C.饱和食盐水
查看习题详情和答案>>
|
|
熔 点 |
沸 点 |
|
三氯化磷 |
-112℃ |
76℃ |
|
五氯化磷 |
148℃ |
200℃分解 |

(1)有浓盐酸、浓硫酸、白磷、二氧化锰、氢氧化钠等物质供选用。a、b中应该装入的试剂分别是:a________,b________。
(2)________仪器需要加热(填仪器对应的字母)。
(3)在蒸馏烧瓶e中收集生成的三氯化磷。为保证三氯化磷蒸气冷凝,应在水槽g中加入________。
(4)三氯化磷遇到水蒸气强烈反应,甚至发生爆炸,所以d、e仪器及装入其中的物质都不能含有水分。为除去氯气中的水分,c可以装入下列物质中的(填字母)________。
A.碱石灰
B.浓硫酸
C.无水氯化钙
(5)氯气和白磷反应放出大量的热,为使曲颈甑 d不致因局部过热而炸裂,实验开始前应在曲颈甑的底部放少量________。
(6)实验室的白磷保存于水中,取出白磷后用滤纸吸干表面水分,浸入无水酒精中片刻,再浸入乙醚中片刻即可完全除去水分。已知水与酒精互溶,酒精与乙醚互溶,用上述方法可除去水分的原因是________。
(7)为防止氯气污染空气,装置末端导出的气体最好用________(填字母)进行净化处理。
A.NaOH溶液
B.Ca(OH)2溶液
C.饱和食盐水
查看习题详情和答案>>
①二氧化锰;②碱石灰;③大理石;④氯化钠;⑤双氧水;⑥浓氨水;⑦浓盐酸;⑧蒸馏水。
请根据如图所示的实验装置结合实验原理回答下列问题。

(1)请在下表中填入利用该装置可以制取的气体和所需药品的编号(表格可以不填全)。
可以制取的气体(填化学式) | 所需药品的编号 |
|
|
|
|
|
|
|
|
(2)请简述检查该装置气密性的正确实验操作。
(3)资料显示:“氨气可在纯氧中安静燃烧……”某校化学小组学生设计如下装置(图中铁夹等夹持装置已略去),进行氨气与氧气在不同条件下反应的实验。

①将产生的氨气与过量的氧气通到装置A(催化剂为铂石棉)中,用酒精喷灯加热。请写出氨催化氧化的化学方程式是______________________________________;
②将过量的氧气与氨气分别从B装置中a、b两管进气口通入到装置B中,并在b管上端点燃氨气。则两气体通入的先后顺序是___________________________________________,理由是________________________________________________________。
(10分)在实验室里可以用如下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质(固定装置略去)。图中①为制取氯气的装置;②试管中装有15mL30%KOH溶液,并置于热水中,制取氯酸钾;③试管中装有15 mL 8%NaOH溶液,并置于冰水中;④中装有紫色石蕊试液。
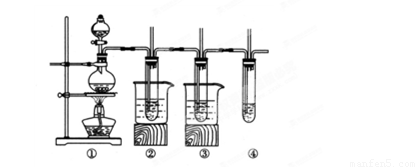
(1)③试管中制取次氯酸钠的化学方程式为
(2)实验中可观察到④试管中溶液的颜色发生如下变化,填写表格。
|
实验现象 |
原因 |
|
溶液最初从紫色变为 色 |
氯气与水反应生成的HCl使石蕊试液变红 |
|
随后溶液逐渐变为无色 |
|
|
最后溶液从无色逐渐变为 色 |
|
(3)此实验有一个明显的不足之处,应如何改进?
查看习题详情和答案>>
在实验室,可以用如图7所示的装置制取乙酸乙酯。请回答下列问题:
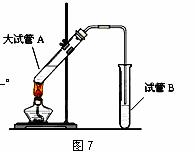
(1)左侧试管中需加浓硫酸做 ▲ 和吸水剂,
右侧试管中盛放的试剂是 ▲ ,
右侧导气管的下端不能插入液面以下,其目的是 ▲ 。
(2)写出实验室用乙醇和乙酸制取乙酸乙酯的化学反应方程式
▲ 。
(3)该反应是典型的可逆反应,若不把生成的乙酸乙酯及时蒸馏 出来,反应一段时间后,
就会达到化学平衡状态。下列能说明该反应已达到化学平衡状态的有(填序号) ▲ 。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水;
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸;
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸;
④混合物中各物质的浓度不再变化。
(4)若现有乙酸 90g、乙醇138g发生酯化反应得到66 g乙酸乙酯,试计算该反应的产率为 ▲ 。(产率指的是某种生成物的实际产量与理论产量的比值)
查看习题详情和答案>>