摘要:26.Cu-2e-=Cu2+. Cu2+ + 2e-=Cu (2)2AuCl4-+3SO2 + 6 H2O =2Au + 8Cl- + 3SO42- + 12H+ (3)王水中含有大量的Cl-.Au3+与Cl-可生成AuCl4-.使该平衡中Au3+浓度降低.平衡正移.金即可溶于王水
网址:http://m.1010jiajiao.com/timu3_id_43265[举报]
有关下图的说法正确的是( )
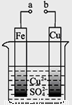
A.构成原电池时溶液中SO42- 移向Cu极
B.构成原电池时Cu极反应为: Cu﹣2e-=Cu2+
C.要使Fe极不被腐蚀,Cu片换Zn片或a接直流电源负极
D.a和b分别接直流电源正、负极,Fe片上有气体产生
查看习题详情和答案>>
有关下图的说法正确的是

A.构成原电池时溶液中SO42- 移向Cu极
B.构成原电池时Cu极反应为: Cu﹣2e-=Cu2+
C.要使Fe极不被腐蚀,Cu片换Zn片或a接直流电源负极
D.a和b分别接直流电源正、负极,Fe片上有气体产生
查看习题详情和答案>>
有关下图的说法正确的是
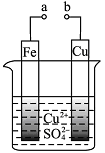
A.构成原电池时溶液中SO42- 移向Cu极
B.构成原电池时Cu极反应为: Cu﹣2e-=Cu2+
C.要使Fe极不被腐蚀,Cu片换Zn片或a接直流电源负极
D.a和b分别接直流电源正、负极,Fe片上有气体产生
查看习题详情和答案>>
有关下图的说法正确的是
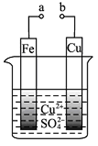
[ ]
A.构成原电池时溶液中SO42- 移向Cu极
B.构成原电池时Cu极反应为:Cu﹣2e-=Cu2+
C.构成电解池时Fe极质量既可增也可减
D.a和b分别接直流电源正、负极,Fe极会产生气体
查看习题详情和答案>>
B.构成原电池时Cu极反应为:Cu﹣2e-=Cu2+
C.构成电解池时Fe极质量既可增也可减
D.a和b分别接直流电源正、负极,Fe极会产生气体
|
用铁丝(电极a)、铜丝(电极b)和CuSO4溶液可以构成原电池或电解池,如图所示.则下列说法正确的是
| |
| [ ] | |
A. |
构成原电池时b极反应为:Cu﹣2e-=Cu2+ |
B. |
构成电解池时a极质量一定减少 |
C. |
构成电解池时b极质量可能减少也可能增加 |
D. |
构成的原电池或电解池工作后就可能产生大量气体 |
