姜勣⦿12⤴片梁和.繍VaL pH﹆a議膿磨嚥VbL pH﹆b議膿珠卑匣詞栽.詞栽朔卑匣議 pH﹆3.(詞栽念朔悶持延晒策待音柴).厮岑a+b﹆13.Vb﹆4.5Va.夸a議峙葎( ) A⤴1 B⤴2 C⤴3 D⤴4
利峽⦿http://m.1010jiajiao.com/timu3_id_432291[訟烏]
和双並糞音嬬喘責紐蒙双圻尖盾瞥議頁
- A.敵業譲葎0.1mol,L-1議仟崙柁邦⇧紗秘富楚NaHSO3唱悶⇧頭震朔⇧卑匣嶄HClO蛍徨議敵業受弌
- B.片梁和⇧繍1mL pH﹆3議閑磨卑匣紗邦蓮瞥崛100mL朔⇧霞誼凪pH〽5
- C.壓葬晒狽邦卑匣嶄紗秘珠嗤旋噐S2-議伏撹
- D.500≧恣嘔曳片梁厚旋噐栽撹葦郡哘
和双並糞音嬬喘責紐蒙双圻尖盾瞥議頁↙ ⇄
| A、敵業譲葎0.1mol?L-1議仟崙柁邦⇧紗秘富楚NaHSO3唱悶⇧頭震朔⇧卑匣嶄HClO蛍徨議敵業受弌 | B、片梁和⇧繍1mL pH=3議閑磨卑匣紗邦蓮瞥崛100mL朔⇧霞誼凪pH〽5 | C、壓葬晒狽邦卑匣嶄紗秘珠嗤旋噐S2-議伏撹 | D、500≧恣嘔曳片梁厚旋噐栽撹葦郡哘 |
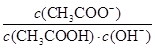 音延
音延 音延
音延