摘要:下列说法正确的是(B) A.铅蓄电池在放电过程中.负极质量减小.正极质量增加 B.常温下.反应C(s)+CO2不能自发进行.则该反应的ΔH>0 C.一定条件下.使用催化剂能加快反应速率并提高反应物的平衡转化率 D.相同条件下.溶液中Cu2+.Fe3+.Zn2+的氧化性依次减弱
网址:http://m.1010jiajiao.com/timu3_id_430844[举报]
下列说法正确的是
A.铅蓄电池在放电过程中,负极质量减小,正极质量增加
B.常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H>0
C.一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率
D.相同条件下,溶液中Cu2+、Fe3+、Zn2+的氧化性依次增强
查看习题详情和答案>>
下列说法正确的是( )
A.铅蓄电池在放电过程中,负极质量减小,正极质量增加
B.设想把“H2+Cl2===2HCl”设计成燃料电池,用于工业制盐酸,并进行发电
C.纯锌与稀硫酸反应产生氢气的速率较慢,再加入少量CuSO4固体,速率不变
D.原电池的两极一定是由活泼性不同的两种金属组成
查看习题详情和答案>>
下列说法正确的是
A.铅蓄电池在放电过程中,负极质量减小,正极质量增加
B.工业上冶炼活泼金属往往用电解的方法,如电解NaCl水溶液制备钠,电解Al2O3制Al
C.往往将闸门与直流电源的负极相连,这是牺牲阳极的阴极保护法
D.电解过程中,溶液中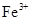 、
、 、
、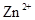 的氧化性依次减弱
的氧化性依次减弱
查看习题详情和答案>>
下列说法正确的是
| A.铅蓄电池在放电过程中,负极质量减小,正极质量增加 |
| B.常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H>0 |
| C.一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率 |
| D.相同条件下,溶液中Cu2+、Fe3+、Zn2+的氧化性依次增强 |