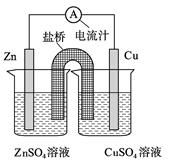
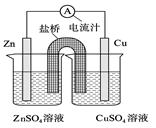
摘要:16. 右图为一原电池的结构示意图.下列说法中.不正确的是 A. 原电池工作时的总反应为Zn+Cu2+=Zn2++Cu.该反应一定为放热反应 B.原电池工作时.Zn电极流出电子.发生氧化反应 C.原电池工作时.铜电极上发生氧化反应.CuSO4溶液蓝色变深 D.如果将Cu电极改为Fe电极.Zn电极依然作负极
网址:http://m.1010jiajiao.com/timu3_id_429545[举报]
右图为一原电池的结构示意图,下列说法中,错误的是 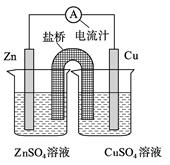
| A.Cu电极为正电极 |
| B.原电池工作时,电子从Zn电极流出 |
| C.原电池工作时的总反应为:Zn+Cu2+=Zn2++Cu |
| D.盐桥(琼脂-饱和KCl溶液)中的K+移向ZnSO4溶液 |
右图为一原电池的结构示意图,下列说法中,错误的是 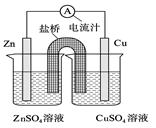
| A.Cu电极为正电极 |
| B.原电池工作时,电子从Zn电极流出 |
| C.原电池工作时的总反应为:Zn+Cu2+=Zn2++Cu |
| D.盐桥(琼脂-饱和KCl溶液)中的K+移向ZnSO4溶液 |
右图为一原电池的结构示意图,下列说法中,错误的是
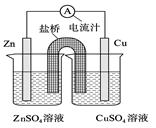
A.Cu电极为正电极
B.原电池工作时,电子从Zn电极流出
C.原电池工作时的总反应为:Zn+Cu2+=Zn2++Cu
D.盐桥(琼脂-饱和KCl溶液)中的K+移向ZnSO4溶液
查看习题详情和答案>>