网址:http://m.1010jiajiao.com/timu3_id_428861[举报]
 E是非金属性最强的元素,M是E的气态氢化物,在固定体积的密闭容器中,气体M存在如下关系:
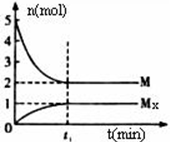
E是非金属性最强的元素,M是E的气态氢化物,在固定体积的密闭容器中,气体M存在如下关系:xM(g)?Mx(g),反应物和生成物的物质的量随时间的变化关系如图.下列说法正确的是( )
E是非金属性最强的元素,M是E的气态氢化物,在固定体积的密闭容器中,气体M存在如下关系:
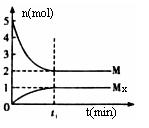 xM(g)
xM(g)![]() Mx (g),反应物和生成物的物质的量随时间的变化关系如下图。下
Mx (g),反应物和生成物的物质的量随时间的变化关系如下图。下
列说法正确的是 ( )
A.该反应的化学方程式是2HF![]() (HF)2
(HF)2
B.平衡时混合气体的平均摩尔质量是33.3
C.t1时刻,保持温度不变,再充入1molM,重新达到平衡时,![]() 将增大
将增大
D.M的沸点比同主族下一周期元素的气态氢化物沸点低
查看习题详情和答案>>E是非金属性最强的元素,M是E的气态氢化物,在固定体积的密闭容器中,气体M存在如下关系:
xM(g)![]() Mx (g),反应物和生成物的物质的量随时间的变化关系如下图。下列说法正确的是 ( )
Mx (g),反应物和生成物的物质的量随时间的变化关系如下图。下列说法正确的是 ( )

A.该反应的化学方程式是2HF![]() (HF)2
(HF)2
B.平衡时混合气体的平均摩尔质量是33.3
C.t1时刻,保持温度不变,再充入1molM,重新达到平衡时,![]() 将增大
将增大
D.M的沸点比同主族下一周期元素的气态氢化物沸点低
查看习题详情和答案>>E是非金属性最强的元素,M是E的气态氢化物,在固定体积的密闭容器中,气体M存在如下关系:
xM(g)![]() Mx(g),反应物和生成物的物质的量随时间的变化关系如下图。下列说法正确的是 ( )
Mx(g),反应物和生成物的物质的量随时间的变化关系如下图。下列说法正确的是 ( )
A.该反应的化学方程式是2HF![]() (HF)2
(HF)2
B.平衡时混合气体的平均摩尔质量是33.3
C.t1时刻,保持温度不变,再充入1molM,重新达到平衡时,![]() 将增大
将增大
D.M的沸点比同主族下一周期元素的气态氢化物沸点低
查看习题详情和答案>>
E是非金属性最强的元素,M是E的气态氢化物,在固定体积的密闭容器中,气体M存在如下关系:xM(g) Mx (g),反应物和生成物的物质的量随时间的变化关系如下图。下列说法正确的是
Mx (g),反应物和生成物的物质的量随时间的变化关系如下图。下列说法正确的是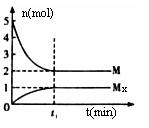
A.该反应的化学方程式是2HF (HF)2 (HF)2 |
| B.平衡时混合气体的平均摩尔质量是33.3 |
C.t1时刻,保持温度不变,再充入1molM,重新达到平衡时,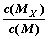 将增大 将增大 |
| D.M的沸点比同主族下一周期元素的气态氢化物沸点低 |