网址:http://m.1010jiajiao.com/timu3_id_428623[举报]
氨在工农业生产中应用广泛。在压强为30MPa时,合成氨平衡混合气体中NH3的体积分数如下:
|
温度/°C |
200 |
300 |
400 |
500 |
600 |
|
氨含量/% |
89.9 |
71.0 |
47.0 |
26.4 |
13.8 |
请回答:
(1)根据表中数据,结合化学平衡移动原理,说明合成氨反应是放热反应的原因是 。
(2)根据-4,合成氨的热化学方程式是 。

(3)在一定温度下,将2molN2和6molH2通入到体积为1L的密闭容器中,发生反应
N2+3H2
 2NH3,2min达到平衡状态时,H2转化率是50%,则用H2表示该反应的平均速率v(H2)=
;该温度下的平衡常数K=
(用分数表示);俗使K增大,可以采取的措施是
。
2NH3,2min达到平衡状态时,H2转化率是50%,则用H2表示该反应的平均速率v(H2)=
;该温度下的平衡常数K=
(用分数表示);俗使K增大,可以采取的措施是
。
(4)从化学平衡移动的角度分析,提高H2转化率可以采取的措施是 (选填序号字母)
a.及时分离出NH3 b.升高温度
c.增大压强 d.使用催化剂
查看习题详情和答案>>

(1)根据表中数据,结合化学平衡移动原理,说明合成氨反应是放热反应的原因________。
(2)根据下图,合成氨反应的热化学方程式是__________________。

 2NH3,
2NH3,2 min达到平衡状态时,H2的转化率是50%,则用H2表示该反应的平均反应速率v(H2)=___________;该温度下的平衡常数K=___________(用分数表示);欲使K增大,可以采取的措施是__________________。
(4)从化学平衡移动的角度分析,欲提高H2的转化率可以采取的措施是____(选填字母)。
a.及时分离出NH3 b.升高温度 c.增大压强 d.使用催化剂

(1)根据表中数据,结合化学平衡移动原理,说明合成氨反应是放热反应的原因____________________。
(2)根据下图,合成氨反应的热化学方程式是____________________。
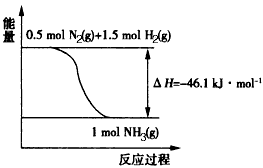
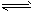 2NH3。
2NH3。2 min达到平衡状态时,H2的转化率是50%,则用H2表示该反应的平均反应速率v(H2)=____ ;该温度下的平衡常数K=________(用分数表示);欲使K增大,可以采取的措施是___________________。
(4)从化学平衡移动的角度分析,欲提高H2的转化率可以采取的措施是____(选填字母)。
a.及时分离出NH3 b.升高温度 c.增大压强 d.使用催化剂
氨在工农业生产中应用广泛。在压强为30MPa时,合成氨平衡混合气体中NH3的体积分数如下:
| 温度/°C | 200 | 300 | 400 | 500 | 600 |
| 氨含量/% | 89.9 | 71.0 | 47.0 | 26.4 | 13.8 |
请回答:
(1)根据表中数据,结合化学平衡移动原理,说明合成氨反应是放热反应的原因是 。
(2)根据-4,合成氨的热化学方程式是 。
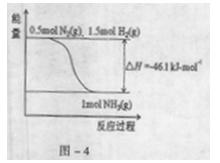
(3)在一定温度下,将2molN2和6molH2通入到体积为1L的密闭容器中,发生反应
N2+3H2 ![]() 2NH3,2min达到平衡状态时,H2转化率是50%,则用H2表示该反应的平均速率v(H2)= ;该温度下的平衡常数K= (用分数表示);俗使K增大,可以采取的措施是 。
2NH3,2min达到平衡状态时,H2转化率是50%,则用H2表示该反应的平均速率v(H2)= ;该温度下的平衡常数K= (用分数表示);俗使K增大,可以采取的措施是 。
(4)从化学平衡移动的角度分析,提高H2转化率可以采取的措施是 (选填序号字母)
a.及时分离出NH3 b.升高温度
c.增大压强 d.使用催化剂
查看习题详情和答案>>氨在工农业生产中应用广泛。在压强为30MPa时,合成氨平衡混合气体中NH3的体积分数如下:
| 温度/°C | 200 | 300 | 400 | 500 | 600 |
| 氨含量/% | 89.9 | 71.0 | 47.0 | 26.4 | 13.8 |
请回答:
(1)根据表中数据,结合化学平衡移动原理,说明合成氨反应是放热反应的原因是 。
(2)根据-4,合成氨的热化学方程式是 。
(3)在一定温度下,将2molN2和6molH2通入到体积为1L的密闭容器中,发生反应
N2+3H2 2NH3,2min达到平衡状态时,H2转化率是50%,则用H2表示该反应的平均速率v(H2)= ;该温度下的平衡常数K= (用分数表示);俗使K增大,可以采取的措施是 。
(4)从化学平衡移动的角度分析,提高H2转化率可以采取的措施是 (选填序号字母)
a.及时分离出NH3 b.升高温度
c.增大压强 d.使用催化剂
查看习题详情和答案>>