摘要:(一)必考题 17.下列中学化学中常见物质的转化关系图中.反应条件及部分反应物和产物未全部注明.已知A.D为金属单质.其他均为化合物.试回答下列问题: (1)写出物质C的化学式: (2)写出物质B的一种用途: (3)以J的饱和溶液制备胶体的操作为 . (4)写出下列反应的方程式: A→F的离子方程式 . H→I的化学方程式 试剂②可以由一种淡黄色固体粉末和一种常见液体发生反应而制得.其相应的化学方程式 (5)某同学认为J中可能同时含有同一种金属元素的两种阳离子.若要确认其中低价金属阳离子的存在.应选用 A.KSCN溶液和氯水 B.铁粉和KSCN溶液 C.浓氨水 D.酸性高锰酸钾 18.铜及其化合物一般都具有特征的颜色.例如Cu.Cu2O呈红色.CuO呈黑色.CuSO4·5H2O呈蓝色等.研究性学习小组甲为检测实验室用H2还原CuO所得红色固体中是否含有Cu2O进行了认真的探究. Ⅰ.查阅资料:①Cu2O属于碱性氧化物, ②在空气中灼烧Cu2O生成CuO,③Cu2O在酸性条件下能发生下列反应:Cu2O+2H+=Cu+Cu2++H2O. Ⅱ.设计实验方案: 方案1:取该红色试样溶于足量的稀硝酸中.观察溶液颜色变化 方案2:取该红色试样溶于足量的稀硫酸中.观察溶液是否呈蓝色 ⑴请你评价方案1和方案2.如果你认为方案合理.请简述其化学原理,如果你认为该方 案不合理.请简述原因. 方案1 : 方案2 : Ⅲ.研究性学习小组乙.设计了新的探究方案.拟通过干燥管中CuSO4是否变蓝判断红色固体中是否含有Cu2O.装置如图所示. (2)为确保探究的科学.合理.安全.你认为实验中还应采取的措施有: A.在氢气发生器与硬质玻璃管之间加一个干燥装置 B.加热前先排尽装置中的空气 C.在盛有硫酸铜的干燥管后再连接一个装有碱石灰的干燥管 19.现有一种溶液.其中可能含有Mg2+.Al3+.Fe2+.Cu2+.NH4+.当加入一种淡黄色固体并加热溶解时.有刺激性气味的气体放出和白色沉淀生成.加入淡黄色固体的物质的量与析出的沉淀和产生气体的物质的量的关系如图所示.试回答下列问题: (1)最终的白色沉淀的成分是 .你的理由是 (2)试确定该溶液中可能含有以上离子中的哪些离子并计算其相应的物质的量.完成下表 可能含有的离子 相应的物质的量 (4)图中a点的值为 (5)图中b点的气体组成成分是 .其物质的量之比是
网址:http://m.1010jiajiao.com/timu3_id_427412[举报]
必考题高锰酸钾是锰的重要化合物和常用的氧化剂.以下是工业上用软锰矿制备高锰酸钾的一种工艺流程.

(1)KMnO4稀溶液是一种常用的消毒剂.其消毒机理与下列
A.75%酒精 B.双氧水 C.苯酚 D.84消毒液(NaClO溶液)
(2)写出MnO2、KOH的熔融混合物中通入空气时发生的主要反应的化学方程式:
(3)向K2MnO4溶液中通入CO2以制备KMnO4,该反应中的还原剂是:
(4)上述流程中可以循环使用的物质有石灰、二氧化碳、
(5)若不考虑物质循环与制备过程中的损失,则1mol MnO2可制得
mol KMnO4.
查看习题详情和答案>>

(1)KMnO4稀溶液是一种常用的消毒剂.其消毒机理与下列
BD
BD
(填序号)物质相似.A.75%酒精 B.双氧水 C.苯酚 D.84消毒液(NaClO溶液)
(2)写出MnO2、KOH的熔融混合物中通入空气时发生的主要反应的化学方程式:
2MnO2+4KOH+O2
2K2MnO4+2H2O
| ||
2MnO2+4KOH+O2
2K2MnO4+2H2O
.
| ||
(3)向K2MnO4溶液中通入CO2以制备KMnO4,该反应中的还原剂是:
K2MnO4
K2MnO4
.(4)上述流程中可以循环使用的物质有石灰、二氧化碳、
KOH
KOH
和MnO2
MnO2
(写化学式).(5)若不考虑物质循环与制备过程中的损失,则1mol MnO2可制得
| 2 |
| 3 |
| 2 |
| 3 |
【必考题】
过氧化尿素[CO(NH2)2?H2O2]是一种无毒、无味的白色结晶粉末,具有尿素和过氧化氢双重性质,是一种新型的氧化剂和消毒剂,广泛应用于漂白、纺织、医药、农业、养殖业等领域.其合成如下:

试回答下列问题:
(1)实际生产中需控制n(H2O2):n(CO(NH2)2)]=1.2:1,并控制合成温度在25-30℃,其主要原因是
(2)从母液中分离出H2O2和尿素,采用的操作是
(a)盐析 过滤 (b)分液 过滤 (c)减压蒸馏 结晶 (d)常压蒸馏 萃取
(3)为测定产品中活性氧的含量(活性氧16%,相当于H2O234%),称取干燥样品12.000g,溶解,在250mL容量瓶中定容.准确量取25.00mL于锥形瓶中,加入1mL 6mol/L的硫酸,然后用0.2000mol/L KMnO4 标准溶液滴定,至滴入最后一滴时,溶液显浅红色且半分钟内不褪色,三次滴定平均消耗KMnO4溶液20.00mL(KMnO4溶液与尿素不反应).
①KMnO4溶液应盛放在
②完成并配平方程式:
③根据滴定结果,可确定产品中活性氧的质量分数为:
④若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量
⑤根据本次实验测得的活性氧含量,可判断该实验产品所含的一种主要杂质为
查看习题详情和答案>>
过氧化尿素[CO(NH2)2?H2O2]是一种无毒、无味的白色结晶粉末,具有尿素和过氧化氢双重性质,是一种新型的氧化剂和消毒剂,广泛应用于漂白、纺织、医药、农业、养殖业等领域.其合成如下:

试回答下列问题:
(1)实际生产中需控制n(H2O2):n(CO(NH2)2)]=1.2:1,并控制合成温度在25-30℃,其主要原因是
H2O2在实验过程中会有部分分解,增大过氧化氢的量可提高过氧化尿素的纯度
H2O2在实验过程中会有部分分解,增大过氧化氢的量可提高过氧化尿素的纯度
.(2)从母液中分离出H2O2和尿素,采用的操作是
c
c
.(a)盐析 过滤 (b)分液 过滤 (c)减压蒸馏 结晶 (d)常压蒸馏 萃取
(3)为测定产品中活性氧的含量(活性氧16%,相当于H2O234%),称取干燥样品12.000g,溶解,在250mL容量瓶中定容.准确量取25.00mL于锥形瓶中,加入1mL 6mol/L的硫酸,然后用0.2000mol/L KMnO4 标准溶液滴定,至滴入最后一滴时,溶液显浅红色且半分钟内不褪色,三次滴定平均消耗KMnO4溶液20.00mL(KMnO4溶液与尿素不反应).
①KMnO4溶液应盛放在
酸
酸
式(选填:“酸”、“碱”)滴定管中.②完成并配平方程式:
2
2
MnO4-+5
5
H2O2+6
6
H+=2
2
Mn2++8
8
H2O+5O2
5O2
③根据滴定结果,可确定产品中活性氧的质量分数为:
13.3%
13.3%
.④若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量
偏高
偏高
(选填:“偏高”、“偏低”或“不变”).⑤根据本次实验测得的活性氧含量,可判断该实验产品所含的一种主要杂质为
尿素
尿素
.必考题高锰酸钾是锰的重要化合物和常用的氧化剂.以下是工业上用软锰矿制备高锰酸钾的一种工艺流程.
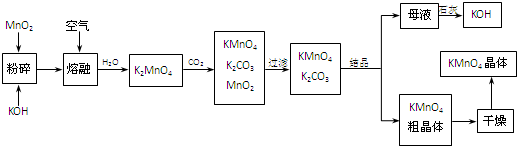
(1)KMnO4稀溶液是一种常用的消毒剂.其消毒机理与下列 (填序号)物质相似.
A.75%酒精 B.双氧水 C.苯酚 D.84消毒液(NaClO溶液)
(2)写出MnO2、KOH的熔融混合物中通入空气时发生的主要反应的化学方程式: .
(3)向K2MnO4溶液中通入CO2以制备KMnO4,该反应中的还原剂是: .
(4)上述流程中可以循环使用的物质有石灰、二氧化碳、 和 (写化学式).
(5)若不考虑物质循环与制备过程中的损失,则1mol MnO2可制得 mol KMnO4.
查看习题详情和答案>>

(1)KMnO4稀溶液是一种常用的消毒剂.其消毒机理与下列 (填序号)物质相似.
A.75%酒精 B.双氧水 C.苯酚 D.84消毒液(NaClO溶液)
(2)写出MnO2、KOH的熔融混合物中通入空气时发生的主要反应的化学方程式: .
(3)向K2MnO4溶液中通入CO2以制备KMnO4,该反应中的还原剂是: .
(4)上述流程中可以循环使用的物质有石灰、二氧化碳、 和 (写化学式).
(5)若不考虑物质循环与制备过程中的损失,则1mol MnO2可制得 mol KMnO4.
【必考题】
过氧化尿素[CO(NH2)2?H2O2]是一种无毒、无味的白色结晶粉末,具有尿素和过氧化氢双重性质,是一种新型的氧化剂和消毒剂,广泛应用于漂白、纺织、医药、农业、养殖业等领域.其合成如下:
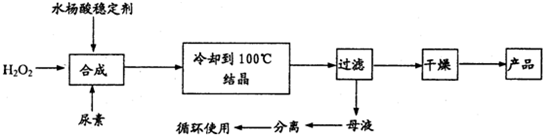
试回答下列问题:
(1)实际生产中需控制n(H2O2):n(CO(NH2)2)]=1.2:1,并控制合成温度在25-30℃,其主要原因是______.
(2)从母液中分离出H2O2和尿素,采用的操作是______.
(a)盐析 过滤 (b)分液 过滤 (c)减压蒸馏 结晶 (d)常压蒸馏 萃取
(3)为测定产品中活性氧的含量(活性氧16%,相当于H2O234%),称取干燥样品12.000g,溶解,在250mL容量瓶中定容.准确量取25.00mL于锥形瓶中,加入1mL 6mol/L的硫酸,然后用0.2000mol/L KMnO4 标准溶液滴定,至滴入最后一滴时,溶液显浅红色且半分钟内不褪色,三次滴定平均消耗KMnO4溶液20.00mL(KMnO4溶液与尿素不反应).
①KMnO4溶液应盛放在______式(选填:“酸”、“碱”)滴定管中.
②完成并配平方程式:______MnO4-+______H2O2+______H+=______Mn2++______H2O+______
③根据滴定结果,可确定产品中活性氧的质量分数为:______.
④若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量______(选填:“偏高”、“偏低”或“不变”).
⑤根据本次实验测得的活性氧含量,可判断该实验产品所含的一种主要杂质为______.
查看习题详情和答案>>
过氧化尿素[CO(NH2)2?H2O2]是一种无毒、无味的白色结晶粉末,具有尿素和过氧化氢双重性质,是一种新型的氧化剂和消毒剂,广泛应用于漂白、纺织、医药、农业、养殖业等领域.其合成如下:

试回答下列问题:
(1)实际生产中需控制n(H2O2):n(CO(NH2)2)]=1.2:1,并控制合成温度在25-30℃,其主要原因是______.
(2)从母液中分离出H2O2和尿素,采用的操作是______.
(a)盐析 过滤 (b)分液 过滤 (c)减压蒸馏 结晶 (d)常压蒸馏 萃取
(3)为测定产品中活性氧的含量(活性氧16%,相当于H2O234%),称取干燥样品12.000g,溶解,在250mL容量瓶中定容.准确量取25.00mL于锥形瓶中,加入1mL 6mol/L的硫酸,然后用0.2000mol/L KMnO4 标准溶液滴定,至滴入最后一滴时,溶液显浅红色且半分钟内不褪色,三次滴定平均消耗KMnO4溶液20.00mL(KMnO4溶液与尿素不反应).
①KMnO4溶液应盛放在______式(选填:“酸”、“碱”)滴定管中.
②完成并配平方程式:______MnO4-+______H2O2+______H+=______Mn2++______H2O+______
③根据滴定结果,可确定产品中活性氧的质量分数为:______.
④若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量______(选填:“偏高”、“偏低”或“不变”).
⑤根据本次实验测得的活性氧含量,可判断该实验产品所含的一种主要杂质为______.
【必考题】
过氧化尿素[CO(NH2)2?H2O2]是一种无毒、无味的白色结晶粉末,具有尿素和过氧化氢双重性质,是一种新型的氧化剂和消毒剂,广泛应用于漂白、纺织、医药、农业、养殖业等领域.其合成如下:

试回答下列问题:
(1)实际生产中需控制n(H2O2):n(CO(NH2)2)]=1.2:1,并控制合成温度在25-30℃,其主要原因是______.
(2)从母液中分离出H2O2和尿素,采用的操作是______.
(a)盐析 过滤 (b)分液 过滤 (c)减压蒸馏 结晶 (d)常压蒸馏 萃取
(3)为测定产品中活性氧的含量(活性氧16%,相当于H2O234%),称取干燥样品12.000g,溶解,在250mL容量瓶中定容.准确量取25.00mL于锥形瓶中,加入1mL 6mol/L的硫酸,然后用0.2000mol/L KMnO4 标准溶液滴定,至滴入最后一滴时,溶液显浅红色且半分钟内不褪色,三次滴定平均消耗KMnO4溶液20.00mL(KMnO4溶液与尿素不反应).
①KMnO4溶液应盛放在______式(选填:“酸”、“碱”)滴定管中.
②完成并配平方程式:______MnO4-+______H2O2+______H+=______Mn2++______H2O+______
③根据滴定结果,可确定产品中活性氧的质量分数为:______.
④若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量______(选填:“偏高”、“偏低”或“不变”).
⑤根据本次实验测得的活性氧含量,可判断该实验产品所含的一种主要杂质为______.
查看习题详情和答案>>
过氧化尿素[CO(NH2)2?H2O2]是一种无毒、无味的白色结晶粉末,具有尿素和过氧化氢双重性质,是一种新型的氧化剂和消毒剂,广泛应用于漂白、纺织、医药、农业、养殖业等领域.其合成如下:

试回答下列问题:
(1)实际生产中需控制n(H2O2):n(CO(NH2)2)]=1.2:1,并控制合成温度在25-30℃,其主要原因是______.
(2)从母液中分离出H2O2和尿素,采用的操作是______.
(a)盐析 过滤 (b)分液 过滤 (c)减压蒸馏 结晶 (d)常压蒸馏 萃取
(3)为测定产品中活性氧的含量(活性氧16%,相当于H2O234%),称取干燥样品12.000g,溶解,在250mL容量瓶中定容.准确量取25.00mL于锥形瓶中,加入1mL 6mol/L的硫酸,然后用0.2000mol/L KMnO4 标准溶液滴定,至滴入最后一滴时,溶液显浅红色且半分钟内不褪色,三次滴定平均消耗KMnO4溶液20.00mL(KMnO4溶液与尿素不反应).
①KMnO4溶液应盛放在______式(选填:“酸”、“碱”)滴定管中.
②完成并配平方程式:______MnO4-+______H2O2+______H+=______Mn2++______H2O+______
③根据滴定结果,可确定产品中活性氧的质量分数为:______.
④若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量______(选填:“偏高”、“偏低”或“不变”).
⑤根据本次实验测得的活性氧含量,可判断该实验产品所含的一种主要杂质为______.
查看习题详情和答案>>