网址:http://m.1010jiajiao.com/timu3_id_426958[举报]

(2)请从以下几个方面对甲乙两套实验装置的优缺点作出评价,并将符合题目要求的选项的序号填在表格中。
a.不容易控制反应速率;b.容易控制反应速率;c.有副反应发生;
d.可防止副反应发生;e.污染环境;f.可防止污染环境。

(4)实验室若用16mol/L的盐酸100mL与足量的二氧化锰反应,理论上最终生成的次氯酸钙的物质的量最多不超过___________________mol。
(12分)回答有关氯气制备的几个问题
实验室用浓盐酸、二氧化锰共热制氯气,并用氯气和Ca(OH)2制取少量漂白粉。现已知反应:2Cl2+2Ca(OH)2 Ca(ClO)2+CaCl2+2H2O,该反应是放热反应,温度稍高即发生副反应:6Cl2+6Ca(OH)2 Ca(ClO3)2+5CaCl2+6H2O。现有两个同学分别设计的两套实验装置如下图:

(1)写出制取氯气的化学方程式 。
(2)请从以下几个方面对甲乙两套实验装置的优缺点作出评价,并将符合题目要求的
选项的序号填在表格中。
a.不容易控制反应速率;b.容易控制反应速率;c.有副反应发生;d.可防止副反应发生;e.污染环境;f.可防止污染环境。
| 优 点 | 缺 点 |
甲装置 |
|
|
乙装置 |
|
|
(3)上述装置中甲由A、B两部分组成,乙由C、D、E三部分组成,请从上述装置中选取合理的部分,组装一套较完整的实验装置,装置各部分连接顺序是 (按气流流动的方向) 。该组合中还缺少的装置是 ,原因是 。
(4)实验室若用16mol/L的盐酸100mL与足量的二氧化锰反应,理论上最终生成的次氯酸钙的物质的量最多不超过 mol。
查看习题详情和答案>>地下水中硝酸盐造成的氮污染已成为一个世界性的环境问题.文献报道某课题组模拟地下水脱氮过程,利用Fe粉和KNO3溶液反应,探究脱氮原理及相关因素对脱氮速率的影响.
(1)实验前:①先用0.1 mol·L-1 H2SO4洗涤Fe粉,其目的是________,然后用蒸馏水洗涤至中性;②将KNO3溶液的pH调至2.5;③为防止空气中的O2对脱氮的影响,应向KNO3溶液中通入________(写化学式).
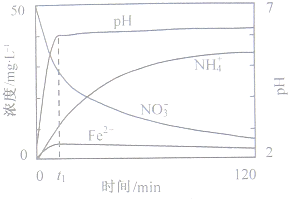
(2)下图表示足量Fe粉还原上述KNO3溶液过程中,测出的溶液中相关离子浓度、pH随时间的变化关系(部分副反应产物曲线略去).请根据图中信息写出t1时刻前该反应的离子方程式________.t1时刻后,该反应仍在进行,溶液中NH4+的浓度在增大,Fe2+的浓度却没有增大,可能的原因是________.

(3)该课题组对影响脱氮速率的因素提出了如下假设:
假设一:溶液的pH;
假设二:温度;
假设三:铁粉颗粒大小;…….
请你设计实验验证上述假设一,写出实验步骤及结论.(已知:溶液中的NO3-浓度可用离子色谱仪测定)
实验步骤及结论:________.
(4)氮的氧化物是造成大气污染的重要原因之一,氨的水溶液可用于吸收NO与NO2混合气体,反应方程式为
6NO+4NH3 5N2+6H2O 6NO2+8NH3
5N2+6H2O 6NO2+8NH3 7N2+12H2O
7N2+12H2O
NO
与NO2混合气体180 mol被8.90×103 g氨水(质量分数0.300)完全吸收,产生156 mol氮气.吸收后氨水密度为0.980 g/cm3.计算:①该混合气体中NO与NO2的体积比.
②吸收后氨水的物质的量浓度(答案保留1位小数)________.
 (2011?安徽)地下水中硝酸盐造成的氮污染已成为一个世界性的环节问题.文献报道某课题组模拟地下水脱氮过程,利用Fe粉和KNO3溶液反应,探究脱氮原理及相关因素对脱氮速率的影响.
(2011?安徽)地下水中硝酸盐造成的氮污染已成为一个世界性的环节问题.文献报道某课题组模拟地下水脱氮过程,利用Fe粉和KNO3溶液反应,探究脱氮原理及相关因素对脱氮速率的影响.(1)实验前:①先用0.1mol?L-1H2SO4洗涤Fe粉,其目的是
(2)图表示足量Fe粉还原上述KNO3溶液过程中,测出的溶液中相关离子浓度、pH随时间的变化关系(部分副反应产物曲线略去).请根据图中信息写出t1时刻前该反应的离子方程式
(3)改课题组对影响脱氮速率的因素提出了如下假设,请你完成假设二和假设三:
假设一:溶液的pH;
假设二:
假设二:
(4)请你设计实验验证上述假设一,写出实验步骤及结论.(已知:溶液中的NO3-浓度可用离子色谱仪测定)
实验结论:
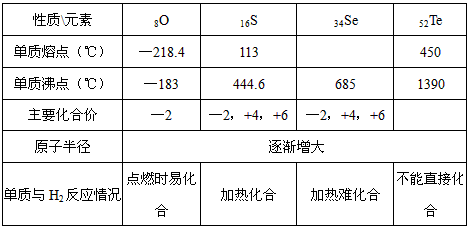
(1)硒的熔点范围可能是_______________
(2)氢硒酸有较强的_________(填“氧化性”或“还原性”),因此放在空气中长期保存易变质,其可能发生在化学反应方程式为_________。
(3)工业上Al2Te3可用来制备H2Te,完成下列化学方程式:
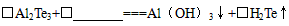
(4)已知在常温下,H2和S反应生成17gH2S放出56.1KJ的热量,试写出硫化氢分解的热化学方程式:
_______________________。
(5)下图所示为氧族元素单质与H2反应过程中的能量变化示意图,其中a、b、c、d分另表示氧族中某一元素的单质,Q为相同物质的量的单质与H2反应放出的热量。则:a代表_______,c代表_________(均可单质名称)
