摘要:化学方程式:① CaCO3 CaO+CO2 ② CaO+H2O === Ca (OH)2 ③ 2Cl2+2Ca (OH)2 === CaCl2+Ca(ClO)2+2H2O 答案:520.8g.(提示:根据关系式2 CaCO3--Ca(ClO)2+CaCl2计算)
网址:http://m.1010jiajiao.com/timu3_id_42595[举报]
下列各组热化学方程式中,化学反应的△H前者大于后者的是
①C(s)+O (g)==CO
(g)==CO (g) △H
(g) △H C(s)+
C(s)+ O
O (g)==CO(g) △H
(g)==CO(g) △H
②S(s)+O (g)==SO
(g)==SO (g) △H
(g) △H S(g)+O
S(g)+O (g)==SO
(g)==SO (g) △H
(g) △H
③H (g)+
(g)+ O
O (g)==H
(g)==H O(l) △H
O(l) △H 2H
2H (g)+O
(g)+O (g)==2H
(g)==2H O(l) △H
O(l) △H
④CaCO (s)==CaO(s)+CO
(s)==CaO(s)+CO (g) △H
(g) △H CaO(s)+H
CaO(s)+H O(l)==Ca(OH)
O(l)==Ca(OH) (s) △H
(s) △H
| A.①② | B.③④ | C.②③④ | D.②③ |
化学用语是学习化学的重要工具.下列用来表示物质变化的化学用语中,错误的是( )
查看习题详情和答案>>
| A.钢铁腐蚀时可能发生的正极反应:2H2O+O2+4e-=4OH- | ||||||
| B.表示H2燃烧热的热化学方程式:2H2(g)+O2(g)=2H2O(g);△H=-483.6kJ/mol | ||||||
C.纯碱水解的离子方程式:CO32-+H2O HCO3-+OH- | ||||||
D.Ca(HCO3)2溶液中加入过量澄清石灰水:C
|
某工厂废渣含MgCO3、SiO2、Fe2O3 、FeCO3和CaCO 3 、Al2O3 。科研小组拟对废渣进行综合利用制取氢氧化镁、芒硝(Na2SO4·10H2O)和硫酸铝,设计如下工艺:
 |
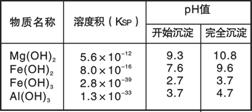 右表为几种沉淀的相关数据。回答以下问题:
右表为几种沉淀的相关数据。回答以下问题:
(1)滤渣Ⅰ中主要成分是CaSO4和
(填化学式)。
(2)欲检验滤液Ⅰ中是否含有Ca2+,
能否用碳酸钠溶液? (填“行”或“不行”)。
(3)滤液Ⅰ中加入试剂后,pH必须控制为9.0。如果pH过大,可能引起的后果是 。
(4)用化学方程式表示往滤液I中加入H2O2的目的
(5)滤液Ⅱ中c(Fe3+)= 。
(6)滤液Ⅲ的主要阳离子是____________(填离子符号);欲从滤液Ⅲ中分离出硫酸铝溶液,依次加入的试剂可以是
查看习题详情和答案>>