网址:http://m.1010jiajiao.com/timu3_id_42366[举报]
(1)甲的化学式为RClx。
①若甲为某短周期金属元素的氯化物,甲中含有的金属元素的原子半径在同周期金属元素中最小,其阳离子与氖原子有相同的电子层结构。则甲中含有的金属元素是________;
②若甲为某金属元素的棕色氯化物,将该氯化物水溶液加热蒸干并灼烧,得到的氧化物为红棕色粉末,则甲的化学式为________,甲中含有的金属元素在周期表中的位置为________,
③将上述两种金属中活泼性强的金属与另一种金属的最高价氧化物混合,引燃后可发生剧烈反应,其化学方程式为________,引燃该反应的实验操作是________。
(2)若甲、乙、丙、丁为单质或化合物,均含有某短周期中的同一种元素,常温下甲为气体,将甲通入常温下的KOH溶液中得到乙和丙,丙的水溶液具有强氧化性。
①电解乙溶液得到甲,该反应的化学方程式为__________;
②在一定条件下1 mol甲与2 mol KOH在溶液中反应得到乙和丁,n(乙):n(丁)=5:1,该反应的离子方程式为___________________。
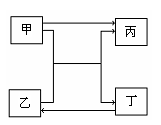
查看习题详情和答案>>右图中的甲、乙、丙和丁分别代表一种反应物或生成物,相互转化关系中部分反应条件略。请根据题目要求回答下列问题。
(1)若甲和乙均为含有10个电子的带电粒子,丙和丁
均为含有10个电子的分子,写出甲和乙共热时的
离子方程式 ;
若将丙溶入丁物质中,应选择的吸收装置为 (填序号)。
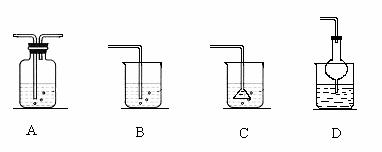
(2)若甲和乙均为含有18个电子的共价化合物,丁为黄色固体,则甲的电子式为
(3)若甲是含有10个电子的化合物,乙是含有18个电子的单质分子,写出甲和乙反应的
化学方程式 ;当乙发生反应
时,转移0.1mol电子,则标况下有 L单质气体乙参加反应。
(4)若甲、乙中均含有常见金属元素,甲为单质,乙中两元素原子的质量比为21:8,则
甲、乙发生反应的化学方程式为 。
(5)若甲和丁为非金属单质,乙和丙为非金属氧化物,则甲和丁可能为 、
(列出常见的两组的名称)。
查看习题详情和答案>>下图中的甲、乙、丙和丁分别代表一种反应物或生成物,相互转化关系中部分反应条件略.请根据题目要求回答下列问题.
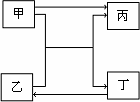
(1)若甲和乙均为含有10个电子的带电粒子,丙和丁均为含有10个电子的分子,写出甲和乙共热时的离子方程式________;
若将丙溶入丁物质中,应选择的吸收装置为________.(填序号).
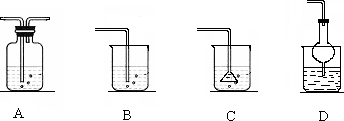
(2)若甲和乙均为含有18个电子的共价化合物,丁为黄色固体,则甲的电子式为________.
(3)若甲是含有10个电子的化合物,乙是含有18个电子的单质分子,写出甲和乙反应的化学方程式________;当乙发生反应时,转移0.1 mol电子,则标况下有________L单质气体乙参加反应.
(4)若甲、乙中均含有常见金属元素,甲为单质,乙中两元素原子的质量比为21∶8,则甲、乙发生反应的化学方程式为________.
(5)若甲和丁为非金属单质,乙和丙为非金属氧化物,则甲和丁可能为________、________(列出常见的两组的名称).
A、B、C、D、E、F是周期表中的前20号元素,原子序数逐渐增大。A元素是宇宙中含量最丰富的元素,其原子的原子核内可能没有中子。B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相等;C元素原子最外层p能级比s能级多1个电子;D原子p轨道上成对电子数等于未成对电子数;E的常见化合价为+3;F最高正价与最低负价的代数和为4; G+的M层电子全充满。用化学式或化学符号回答下列问题:

(1)G的基态原子的外围电子排布式为 ,周期表中F属于 区。
(2)B与F形成的一种非极性分子的电子式为 ;F的一种具有强还原性的氧化物分子的VSEPR模型为
(3)BD2在高温高压下所形成的晶胞如右图所示。该晶体的类型属于_______
(选填“分子”、“原子”、“离子”或“金属”)晶体
(4)设C元素的气态氢化物为甲,最高价氧化物的水化物为乙,甲与乙反应的产物为丙。常温下,有以下3种溶液:①pH=11的甲的水溶液 ②pH=3的乙的水溶液 ③pH=3的丙溶液,3种溶液中水电离出的cH+之比为
(5)丁、戊分别是E、F两种元素最高价含氧酸的钠盐,丁、戊溶液能发生反应。当丁、戊溶液以物质的量之比为1:4混合后,溶液中各离子浓度大小顺序为
(6)A和C形成的某种氯化物CA2Cl可作杀菌剂,其原理为CA2Cl遇水反应生成一种具有强氧化性的含氧酸,写出CA2Cl与水反应的化学方程式:___________________________
(7)往G的硫酸盐溶液中加入过量氨水,可生成一种配合物X,下列说法正确的是___ __
A.X中所含化学键有离子键、极性键和配位键
B.X中G2+给出孤对电子,NH3提供空轨道
C.组成X的元素中第一电离能最大的是氧元素
D.SO42-与PO43-互为等电子体,空间构型均为正四面体
查看习题详情和答案>>

(1)G的基态原子的外围电子排布式为 ,周期表中F属于 区。
(2)B与F形成的一种非极性分子的电子式为 ;F的一种具有强还原性的氧化物分子的VSEPR模型为
(3)BD2在高温高压下所形成的晶胞如右图所示。该晶体的类型属于_______
(选填“分子”、“原子”、“离子”或“金属”)晶体
(4)设C元素的气态氢化物为甲,最高价氧化物的水化物为乙,甲与乙反应的产物为丙。常温下,有以下3种溶液:①pH=11的甲的水溶液 ②pH=3的乙的水溶液 ③pH=3的丙溶液,3种溶液中水电离出的cH+之比为
(5)丁、戊分别是E、F两种元素最高价含氧酸的钠盐,丁、戊溶液能发生反应。当丁、戊溶液以物质的量之比为1:4混合后,溶液中各离子浓度大小顺序为
(6)A和C形成的某种氯化物CA2Cl可作杀菌剂,其原理为CA2Cl遇水反应生成一种具有强氧化性的含氧酸,写出CA2Cl与水反应的化学方程式:___________________________
(7)往G的硫酸盐溶液中加入过量氨水,可生成一种配合物X,下列说法正确的是___ __
A.X中所含化学键有离子键、极性键和配位键
B.X中G2+给出孤对电子,NH3提供空轨道
C.组成X的元素中第一电离能最大的是氧元素
D.SO42-与PO43-互为等电子体,空间构型均为正四面体