摘要:4.在某一澄清.透明的浅黄色溶液中,可能含有下列八种离子:H+.NH.Fe3+.Ba2+.Al3+.SO.HCO.I-.在检验方案设计时初步分析其溶液中最多可含离子 (不包括OH-)有( )w.w.^w.k.&s.5*高.考.资.源.网 A.4种 B.5种 C.6种 D.7种
网址:http://m.1010jiajiao.com/timu3_id_422824[举报]
在某一澄清、透明的浅黄色溶液中,可能含有下列八种离子:H+、NH4+、Fe3+、Ba2+、Al3+、SO42-、
HCO3-、I-,在检验方案设计时初步分析其溶液中最多可含离子(不包括OH-)
HCO3-、I-,在检验方案设计时初步分析其溶液中最多可含离子(不包括OH-)
[ ]
A.4种
B.5种
C.6种
D.7种
查看习题详情和答案>>
B.5种
C.6种
D.7种
在某澄清、透明的浅黄色溶液中,可能含有K+、NH4+、Fe3+、Ba2+、Al3+、SO42-、HCO3-、Cl-离子.进行下述实验(所加试剂均过量).

(1)气体A的化学式是
(2)待测液中一定存在
(3)写出溶液C与过量氨水主要发生的反应的离子方程式
(4)三硅酸镁被用来治疗胃酸过多的胃溃疡,是因为该物质不溶于水,服用后能中和胃酸,作用持久.把三硅酸镁(Mg2Si3O8?nH2O)改写成氧化物的形式为
查看习题详情和答案>>

(1)气体A的化学式是
NH3
NH3
,沉淀A的化学式是Fe(OH)3
Fe(OH)3
;(2)待测液中一定存在
NH4+、Al3+、Fe3+、SO42-;
NH4+、Al3+、Fe3+、SO42-;
;一定不存在Ba2+、HCO3-
Ba2+、HCO3-
;(3)写出溶液C与过量氨水主要发生的反应的离子方程式
Al3++3NH3?H2O=Al(OH)3↓+3NH4+
Al3++3NH3?H2O=Al(OH)3↓+3NH4+
.(4)三硅酸镁被用来治疗胃酸过多的胃溃疡,是因为该物质不溶于水,服用后能中和胃酸,作用持久.把三硅酸镁(Mg2Si3O8?nH2O)改写成氧化物的形式为
2MgO?3SiO2?nH2O
2MgO?3SiO2?nH2O
,它中和胃酸(HCl)的离子方程式是:2MgO?3SiO2?nH2O+4H+=2Mg2++3H2SiO3+(n-1)H2O
2MgO?3SiO2?nH2O+4H+=2Mg2++3H2SiO3+(n-1)H2O
.在某澄清、透明的浅黄色溶液中,可能含有K+、NH4+、Fe3+、Ba2+、Al3+、SO42-、HCO3-、Cl-离子.进行下述实验(所加试剂均过量).

(1)气体A的化学式是______,沉淀A的化学式是______;
(2)待测液中一定存在______;一定不存在______;
(3)写出溶液C与过量氨水主要发生的反应的离子方程式______.
(4)三硅酸镁被用来治疗胃酸过多的胃溃疡,是因为该物质不溶于水,服用后能中和胃酸,作用持久.把三硅酸镁(Mg2Si3O8?nH2O)改写成氧化物的形式为______,它中和胃酸(HCl)的离子方程式是:______.
查看习题详情和答案>>
在某澄清、透明的浅黄色溶液中,可能含有K+、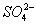 、Fe3+、Ba2+、Al3+、
、Fe3+、Ba2+、Al3+、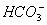 、
、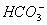 、Cl-离子。进行下述实验(所加试剂均过量)。
、Cl-离子。进行下述实验(所加试剂均过量)。
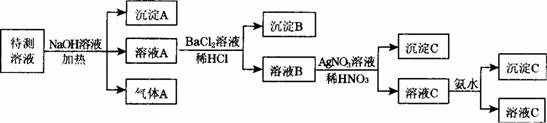
(1)气体A的化学式是_____________,沉淀A的化学式是____________________________
(2)检验溶液中是否含有K+的操作是________________________________________________。
________________________________________________________________;
(3)待测液中一定存在_________________________________________
(4)待测液中一定不存在__________;其原因是___________________________________
(5)写出溶液C与过量氨水反应的离子方程式________________________________________。
查看习题详情和答案>>