网址:http://m.1010jiajiao.com/timu3_id_420296[举报]

(1)结合上图数据,判断下列说法正确的是
A.在交通运输中排放的NOx与燃料的不充分燃烧有关
B.在上世纪60年代以前,在交通运输中排放的SO2主要是使用燃煤的内燃机所致
C.近年来在工业生产中SO2排放量的下降,主要是减少了燃烧的煤的质量
D.随着汽车工业的发展,在形成酸雨的因素中,NOx所占比重在逐渐增大
(2)在上图表示的历史进程中,由工业生产所导致的SO2的排放量明显地在逐年减少.请用化学方程式说明人类在为解决SO2污染问题中所进行的一个反应过程:
(3)汽车排放的尾气中含有未燃烧充分的CmHn、以及N2、CO2、NO、CO等.有人设计利用反应2NO+2CO?N2+2CO2 将有害的污染物转化为可参与大气循环的N2和CO2.
在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
| 时间/h | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol?L-1 | 1.00×10-3 | 4.5×10-4 | 2.5×10-4 | 1.5×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol?L-1 | 3.6×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
(4)某次降雨过程收集到10L的雨水,向雨水中滴加1mL6mol/L的H2O2,充分反应后测得溶液的pH=3.62[c(H+)=2.4×10-4mol/L]),再向溶液中加入足量的Ba(OH)2溶液,经过滤、晾干、称重,得沉淀的质量为0.1864g.若假设雨水的酸性仅由NOx和SO2的排放所致.请计算排放在空气中的NOx和SO2的物质的量之比接近于
(1)硅的制备方法是制约太阳能发展的瓶颈,硅的制备原料是石英砂,石英与焦炭在高温电炉中反应可以制得硅.该反应的化学方程式是
(2)氮化硅Si3N4是一种高温结构材料,粉末状态的Si3N4可以由SiCl4的蒸气和NH3反应制取.粉末状Si3N4对空气和水都不稳定.但将粉末状的Si3N4和适量氧化镁在230×1.01×l05Pa和185℃的密闭容器中热处理,可以制得结构十分紧密、对空气和水都相当稳定的固体材料,同时还得到对水不稳定的Mg3N2.
①写出由SiCl4和NH3反应制取Si3N4的化学反应方程式
②现用四氯化硅和氮气在氢气气氛保护下,加强热发生反应,使生成的Si3N4沉积在石墨表面可得较高纯度的氮化硅,该制造方法称为:
③在Si3N4和适量氧化镁在230×1.01×105 Pa和185℃的密闭容器中热处理的过程中,除生成Mg3N2外,还可能生成
(20分)
(I)多项选择题(6分)
CH3+、CH3-、CH3-都是重要的有机反应中间体,有关它们的说法正确的是 。
| A.它们均由甲烷去掉一个氢原子所得 |
| B.它们互为等电子体,碳原子均采取sp2杂化 |
| C.CH3-与NH3、H3O+互为等电子体,几何构型均为三角锥形 |
| D.CH3+中的碳原子采取sp2杂化,所有原子均共面 |
(II)(14分)
锌是一种重要的金属,锌及其化合物有着广泛的应用。
(1)指出锌在周期表中的位置: 周期, 族, 区。
(2)葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂。写出Zn2+基态电子排布式 ;葡萄糖分子中碳原子杂化方式有 。
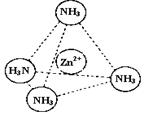
(3)Zn2+能与NH3形成配离子[Zn(NH3)4]2+。配位体NH3分子属于 (填“极性分子”或“非极性分子”);在[Zn(NH3)4]2+中,Zn2+位于正四面体中心,N位于正四面体的顶点,试在左下图中表示[Zn(NH3)4]2+中Zn2+与N之间的化学键。
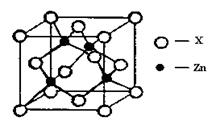
(4)右上图表示锌与某非金属元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为 ;该化合物的晶体熔点比干冰高得多,原因是 。 查看习题详情和答案>>
《有机化学基础》
18-1.(6分,该题为多项选择题,全选对得6分,漏选按比例给分,错选或多选为0分)
下列关于有机物的说法中,正确的是( )
| A.蔗糖是高分子化合物,其水解产物能发生银镜反应 |
| B.橡胶和纤维不一定都是合成高分子材料 |
| C.常温下淀粉遇碘酒变蓝色,葡萄糖能与新制Cu(OH)2发生反应 |
| D.将某烃类的混合气体跟Cl2混合光照,发现有油状液滴生成,说明混合气体肯定含有甲烷 |
 分子中所有原子不可能共平面
分子中所有原子不可能共平面18-2.(14分)已知:一个碳原子上连有两个羟基时,易发生下列转化:

请根据下图作答:

(1)A的核磁共振氢谱中出现 组峰;E中含有的官能团的名称是 ;
(2)反应③的化学方程式为 ;
(3)已知B的相对分子质量为162,其完全燃烧的产物中CO 2和H2O的物质的量之比为 n(CO2)︰n (H2O)=2︰1,则B的分子式为 ;
(4)F是高分子光阻剂生产中的主要原料。F具有如下特点:①属于芳香族化合物;②能跟FeCl3溶液发生显色反应;③能发生加聚反应;④苯环上的一氯代物只有两种。F在一定条件下发生加聚反应的化学方程式为 ;
(5)化合物G是F的同分异构体,属于芳香族化合物,能发生银镜反应。G有多种可能的结构,请写出它们的结构简式 。 查看习题详情和答案>>
(20分)
(I)多项选择题(6分)
下列说法中正确的是 。
A.丙烯分子中有8个σ键,1个π键
B.在SiO2晶体中,1个Si原子和2个O原子形成2个共价键
C.NF3的沸点比NH3的沸点低得多,是因为NH3分子间有氢键,NF3只有范德华力
D.NCl3和BC13分子中,中心原子都采用sp3杂化
E.在“冰→水→水蒸气→氧气和氢气”的变化过程中,各阶段被破坏的粒子间主要的相互作用依次是氢键、分子间作用力、极性键
(II)(14分)
人类在使用金属的历史进程中,经历了铜、铁、铝之后,第四种将被广泛应用的金属被科学家预测是钛(Ti),它被誉为“未来世纪的金属”。试回答下列问题:
(1)Ti元素在元素周期表中的位置是第________周期第________族;其基态原子的电子排布式为________。
(2)在Ti的化合物中,可以呈现+2、+3、+4三种化合价,其中以+4价的Ti最为稳定。偏钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构示意图如图所示,它的化学式是 ,其中Ti4+的氧配位数为 ,Ba2+的氧配位数为 ,

(3)常温下的TiCl4是有刺激性臭味的无色透明液体,熔点-23.2℃,沸点136.2℃,所以TiCl4应是 化合物,其固体是 晶体。TiCl4在潮湿空气中易挥发,水解而冒白烟,这是因为水解后有 生成。
(4)已知Ti3+可形成配位数为6的配合物,其空间构型为正八面体,如下图1所示,我们通常可以用下图2所示的方法来表示其空间构型(其中A表示配体,M表示中心原子)。配位化合物[Co(NH3)4Cl2]的空间构型也为八面体型,它有 种同分异构体,请在下图方框中将其画出。

查看习题详情和答案>>