摘要:9.X.Y是原子序数相差2的高*考#资^源*网两种短周期元素.下列相关说法正确的高*考#资^源*网是 A.X与Y可能位于同一周期.但不可能位于同一主族 B.X与Y可能形成原子个数比为1 :1型的高*考#资^源*网共价化合物.但不能形成原子个数比为1 :1型的高*考#资^源*网离子化合物 C.X离子与Y离子的高*考#资^源*网电子层结构可以相同.也可以不同 D.X与Y形成的高*考#资^源*网共价化合物中.其原子个数之比可能是1 :1.1 :2.但不能是1 :3
网址:http://m.1010jiajiao.com/timu3_id_419783[举报]
X、Y是原子序数相差2的两种短周期元素,下列相关说法正确的是
A.X与Y可能位于同一周期,但不可能位于同一主族
B.X与Y可能形成原子个数比为1 :1型的共价化合物,但不能形成原子个数比为1 :1型的离子化合物
C.X离子与Y离子的电子层结构可以相同,也可以不同
D.X与Y形成的共价化合物中,其原子个数之比可能是1 :1、1 :2,但不能是1 :3
查看习题详情和答案>>X、Y是原子序数相差2的两种短周期元素,下列相关说法正确的是
- A.X与Y可能位于同一周期,但不可能位于同一主族
- B.X与Y可能形成原子个数比为1 :1型的共价化合物,但不能形成原子个数比为1 :1型的离子化合物
- C.X离子与Y离子的电子层结构可以相同,也可以不同
- D.X与Y形成的共价化合物中,其原子个数之比可能是1 :1、1 :2,但不能是1 :3
X、Y是原子序数相差2的两种短周期元素,下列相关说法正确的是
| A.X与Y可能位于同一周期,但不可能位于同一主族 |
| B.X与Y可能形成原子个数比为1 :1型的共价化合物,但不能形成原子个数比为1 :1型的离子化合物 |
| C.X离子与Y离子的电子层结构可以相同,也可以不同 |
| D.X与Y形成的共价化合物中,其原子个数之比可能是1 :1、1 :2,但不能是1 :3 |
U、V、W、X、Y是原子序数依次增大的五种短周期常见元素.Y的单质在W2中燃烧的产物可使品红溶液褪色.U的单质在W2中燃烧可生成UW和UW2两种气体.X的单质是一种金属,该金属在UW2中剧烈燃烧生成黑、白两种固体.
请回答下列问题:
(1)V元素原子的L层电子排布式为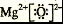
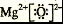 .
.
(2)U元素形成的同素异形体的晶体类型可能是(填序号)
①原子晶体 ②离子晶体 ③分子晶体 ④金属晶体
(3)U、V、W形成的10电子氢化物中,U、V的氢化物沸点较低的是(写化学式)
(4)YW2气体通入BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体VW,有关反应的离子方程式为
查看习题详情和答案>>
请回答下列问题:
(1)V元素原子的L层电子排布式为
2s22p3
2s22p3
;XW的电子式为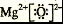
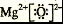
(2)U元素形成的同素异形体的晶体类型可能是(填序号)
①③
①③
.①原子晶体 ②离子晶体 ③分子晶体 ④金属晶体
(3)U、V、W形成的10电子氢化物中,U、V的氢化物沸点较低的是(写化学式)
CH4
CH4
;V、W的氢化物分子结合H+能力较强的是(写化学式)NH3
NH3
,用一个离子方程式加以证明NH3+H3O+=NH4++H2O
NH3+H3O+=NH4++H2O
.(4)YW2气体通入BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体VW,有关反应的离子方程式为
3SO2+2NO3-+3Ba2++2H2O=3BaSO4↓+2NO+4H+
3SO2+2NO3-+3Ba2++2H2O=3BaSO4↓+2NO+4H+
,由此可知VW和YW2还原性较强的是(写化学式)SO2
SO2
.