摘要:14.耐火材料主要成分为MgO和A1O.某厂用蛭石(主要成份为:MgO.Fe2O3.A12O3.SiO2)作原料生产耐火材料.化学课外小组同学用蛭石进行了以下实验: Ⅰ.查阅资料得知0.1mol/L的离子浓度时.氢氧化物沉淀时的pH为 氢氧化物 Fe(OH)3 Mg(OH)2 AI(OH)3 开始沉淀时的pH 2.3 10.4 4.0 开始溶解:7.8 完全沉淀时的pH 3.7 12.4 5.2 完全溶解:10.8 Ⅱ.实验流程如下: 请回答以下问题: (1)写出下列物质化学式:试剂I ,固体F . (2)步骤②可把pH调节到 .下列氧化剂中最好选用 (填字母) A.KMnO4 B.H2O2 C.NaClO D.浓HNO3 (3)步骤③中C生成D的离子反应方程式为 .要保证固体D杂质尽量少.步聚②调节溶液的pH合理范围是 : A.5.7~2.8 B.7.8~12.4 C.小于7.8 D.大于12.4 (4)步骤④中反应的离子方程式为 .
网址:http://m.1010jiajiao.com/timu3_id_419201[举报]
江苏省东海县矿产丰富,除了水晶制品名扬天下外,蛭石、蛇纹石等矿石储量大,品位高,其相关的耐火、保温隔热材料(主要成分为MgO、Al2O3)工业也较发达.
某中学化学探究小组通过查阅相关资料,对蛭石的组成进行了实验探究.
I、相关资料:①蛭石的成分可看成是由MgO、Fe2O3、Al2O3、SiO2组成
②氢氧化物开始沉淀及沉淀完全时的pH
Ⅱ、相关实验:

Ⅲ、实验数据:
①矿石样品质量为:8.22g ②每次转化所得固体成分只有一种
请你根据以上内容和中学化学知识回答以下问题
(1)写出由D制一种红色颜料的化学方程式:
(2)工业上的耐火材料通常由F及滤液E进一步转化而成,请你分析滤液E中可能含有成分,设计一个从滤液E制取耐火材料的实验方法:
(3)滤液B和NaOH溶液反应时,应控制溶液的pH在7-8之间,这是因为:
(4)通过计算,写出用氧化物的形式表示蛭石组成的化学式
查看习题详情和答案>>
某中学化学探究小组通过查阅相关资料,对蛭石的组成进行了实验探究.
I、相关资料:①蛭石的成分可看成是由MgO、Fe2O3、Al2O3、SiO2组成
②氢氧化物开始沉淀及沉淀完全时的pH
| 氢氧化物 | Fe(OH)3 | Mg(OH)2 | Al(OH)3 |
| 沉淀的pH范围 | 1.5-4.1 | 9.4-12.4 | 3.3-5.2 |

Ⅲ、实验数据:
①矿石样品质量为:8.22g ②每次转化所得固体成分只有一种
请你根据以上内容和中学化学知识回答以下问题
(1)写出由D制一种红色颜料的化学方程式:
2Fe(OH)3
Fe2O3+3H2O
| ||
2Fe(OH)3
Fe2O3+3H2O
| ||
(2)工业上的耐火材料通常由F及滤液E进一步转化而成,请你分析滤液E中可能含有成分,设计一个从滤液E制取耐火材料的实验方法:
向将所得的滤液E中加入足量的NaOH溶液,再进行过滤、洗涤、干燥,最后进行高温灼烧
向将所得的滤液E中加入足量的NaOH溶液,再进行过滤、洗涤、干燥,最后进行高温灼烧
(3)滤液B和NaOH溶液反应时,应控制溶液的pH在7-8之间,这是因为:
根据表中数据,控制溶液的pH在7~8之间,Mg2+没有变化,Al3+转化为AlO2-,只有Fe3+沉淀,保证沉淀只有Fe(OH)3
根据表中数据,控制溶液的pH在7~8之间,Mg2+没有变化,Al3+转化为AlO2-,只有Fe3+沉淀,保证沉淀只有Fe(OH)3
(4)通过计算,写出用氧化物的形式表示蛭石组成的化学式
8MgO?Al2O3?Fe2O3?4SiO2
8MgO?Al2O3?Fe2O3?4SiO2
.江苏省东海县矿产丰富,除了水晶制品名扬天下外,蛭石、蛇纹石等矿石储量大,品位高,其相关的耐火、保温隔热材料(主要成分为MgO、Al2O3)工业也较发达.
某中学化学探究小组通过查阅相关资料,对蛭石的组成进行了实验探究.
I、相关资料:①蛭石的成分可看成是由MgO、Fe2O3、Al2O3、SiO2组成
②氢氧化物开始沉淀及沉淀完全时的pH
Ⅱ、相关实验:
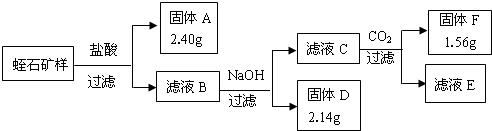
Ⅲ、实验数据:
①矿石样品质量为:8.22g ②每次转化所得固体成分只有一种
请你根据以上内容和中学化学知识回答以下问题
(1)写出由D制一种红色颜料的化学方程式:______
(2)工业上的耐火材料通常由F及滤液E进一步转化而成,请你分析滤液E中可能含有成分,设计一个从滤液E制取耐火材料的实验方法:______
(3)滤液B和NaOH溶液反应时,应控制溶液的pH在7-8之间,这是因为:______
(4)通过计算,写出用氧化物的形式表示蛭石组成的化学式______.
查看习题详情和答案>>
某中学化学探究小组通过查阅相关资料,对蛭石的组成进行了实验探究.
I、相关资料:①蛭石的成分可看成是由MgO、Fe2O3、Al2O3、SiO2组成
②氢氧化物开始沉淀及沉淀完全时的pH
| 氢氧化物 | Fe(OH)3 | Mg(OH)2 | Al(OH)3 |
| 沉淀的pH范围 | 1.5-4.1 | 9.4-12.4 | 3.3-5.2 |

Ⅲ、实验数据:
①矿石样品质量为:8.22g ②每次转化所得固体成分只有一种
请你根据以上内容和中学化学知识回答以下问题
(1)写出由D制一种红色颜料的化学方程式:______
(2)工业上的耐火材料通常由F及滤液E进一步转化而成,请你分析滤液E中可能含有成分,设计一个从滤液E制取耐火材料的实验方法:______
(3)滤液B和NaOH溶液反应时,应控制溶液的pH在7-8之间,这是因为:______
(4)通过计算,写出用氧化物的形式表示蛭石组成的化学式______.
江苏省东海县矿产丰富,除了水晶制品名扬天下外,蛭石、蛇纹石等矿石储量大,品位高,其相关的耐火、保温隔热材料(主要成分为MgO、Al2O3)工业也较发达.
某中学化学探究小组通过查阅相关资料,对蛭石的组成进行了实验探究.
I、相关资料:①蛭石的成分可看成是由MgO、Fe2O3、Al2O3、SiO2组成
②氢氧化物开始沉淀及沉淀完全时的pH
| 氢氧化物 | Fe(OH)3 | Mg(OH)2 | Al(OH)3 |
| 沉淀的pH范围 | 1.5-4.1 | 9.4-12.4 | 3.3-5.2 |

Ⅲ、实验数据:
①矿石样品质量为:8.22g ②每次转化所得固体成分只有一种
请你根据以上内容和中学化学知识回答以下问题
(1)写出由D制一种红色颜料的化学方程式:______
(2)工业上的耐火材料通常由F及滤液E进一步转化而成,请你分析滤液E中可能含有成分,设计一个从滤液E制取耐火材料的实验方法:______
(3)滤液B和NaOH溶液反应时,应控制溶液的pH在7-8之间,这是因为:______
(4)通过计算,写出用氧化物的形式表示蛭石组成的化学式______. 查看习题详情和答案>>
| |||||||||||||||||||||||
江苏省东海县矿产丰富,除了水晶制品名扬天下外,蛭石、蛇纹石等矿石储量大,品位高,其相关的耐火、保温隔热材料(主要成分为MgO、Al2O3)工业也较发达.
某中学化学探究小组通过查阅相关资料,对蛭石的组成进行了实验探究.
I、相关资料:①蛭石的成分可看成是由MgO、Fe2O3、Al2O3、SiO2组成
②氢氧化物开始沉淀及沉淀完全时的pH
Ⅱ、相关实验:

Ⅲ、实验数据:
①矿石样品质量为:8.22g ②每次转化所得固体成分只有一种
请你根据以上内容和中学化学知识回答以下问题
(1)写出由D制一种红色颜料的化学方程式:______ Fe2O3+3H2O 查看习题详情和答案>>
某中学化学探究小组通过查阅相关资料,对蛭石的组成进行了实验探究.
I、相关资料:①蛭石的成分可看成是由MgO、Fe2O3、Al2O3、SiO2组成
②氢氧化物开始沉淀及沉淀完全时的pH
| 氢氧化物 | Fe(OH)3 | Mg(OH)2 | Al(OH)3 |
| 沉淀的pH范围 | 1.5-4.1 | 9.4-12.4 | 3.3-5.2 |

Ⅲ、实验数据:
①矿石样品质量为:8.22g ②每次转化所得固体成分只有一种
请你根据以上内容和中学化学知识回答以下问题
(1)写出由D制一种红色颜料的化学方程式:______ Fe2O3+3H2O 查看习题详情和答案>>

