网址:http://m.1010jiajiao.com/timu3_id_41779[举报]
(7分) 科学家一直致力于“人工固氮”的方法研究。
⑴目前合成氨的技术原理为:
该反应的能量变化如图所示。

①在反应体系中加入催化剂,反应速率增大,E2的变化是: 。(填“增大”、“减小”或“不变”)。
②将一定量的N2(g)和H2(g)放入1L的密闭容器中,在500℃、2×107Pa下达到平衡,测得N2为0.1 mol,H2为0.3 mol,NH3为0.1 mol。该条件下H2的转化率为 。
③欲提高②容器中H2的转化率,下列措施可行的是 。
A.向容器中按原比例再充入原料气 B.向容器中再充入惰性气体
C.改变反应的催化剂 D.液化生成物分离出氨
⑵1998年希腊亚里士多德大学的两位科学家采用高质子导电性的SCY陶瓷(能传导H+),从而实现了高转化率的电解法合成氨。其实验装置如图所示。阴极的电极反应式为 。

⑶根据最新“人工固氮”的研究报道,在常温、常 压、光照条件下,N2在催化剂(掺有少量Fe2O3和TiO2)表面与水发生下列反应:

进一步研究NH3生成量与温度关系,常压下达到平衡时测得部分实验数据如下:
|
T/K |
303 |
313 |
323 |
|
NH3生成量/(10-6mol) |
4.8 |
5.9 |
6.0 |
①合成反应的a_ 0。(填“大于”、“小于”或“等于”)
②已知

则
查看习题详情和答案>>
(13分)
(1)稀有气体不能形成双原子分子是因为 。
(2)多电子原子中,在离核较近的区域内运动的电子能量 (填较高或较低)。
(3)不含中子的核素的核组成符号为 。
(4)ⅥA族氢化物中沸点最低的是 (写化学式)。
(5)在金属元素与非金属元素的分界线附近可以寻找制备 材料的元素;在
中可寻找制备催化剂及耐高温、耐腐蚀的元素。
(6)下列选项中,随原子序数递增而呈周期性变化的是 (填序号,后同);其中,起决定性作用的是
A.原子核外电子排布,B.原子半径,C.主要化合价,D.元素的金属性或非金属性。
(7)下列核素中,用于考古时测文物年代的是 (填序号)。
A.2H和3H, B.14C, C.235U。
(8)下列实验中,可产生白烟的是 (填序号)。
A.氢气与氯气反应,B钠与氯气反应。
(9)下列反应中,更剧烈的是 (填序号)。
A.钠与水反应,B.钾与水反应。
(10)取下列溶液分装两试管,再分别依次加入少量氯水和少量四氯化碳,用力振荡、静置后,四氯化碳层显橙红色的是 (填序号)。
A.溴化钠溶液,B.碘化钾溶液。
(11)用电子式表示MgCl2的形成过程 。
查看习题详情和答案>>
(13分)
(1)稀有气体不能形成双原子分子是因为 。
(2)多电子原子中,在离核较近的区域内运动的电子能量 (填较高或较低)。
(3)不含中子的核素的核组成符号为 。
(4)ⅥA族氢化物中沸点最低的是 (写化学式)。
(5)在金属元素与非金属元素的分界线附近可以寻找制备 材料的元素;在
中可寻找制备催化剂及耐高温、耐腐蚀的元素。
(6)下列选项中,随原子序数递增而呈周期性变化的是 (填序号,后同);其中,起决定性作用的是
A.原子核外电子排布,B.原子半径,C.主要化合价,D.元素的金属性或非金属性。
(7)下列核素中,用于考古时测文物年代的是 (填序号)。
A.2H和3H, B.14C, C.235U。
(8)下列实验中,可产生白烟的是 (填序号)。
A.氢气与氯气反应,B钠与氯气反应。
(9)下列反应中,更剧烈的是 (填序号)。
A.钠与水反应,B.钾与水反应。
(10)取下列溶液分装两试管,再分别依次加入少量氯水和少量四氯化碳,用力振荡、静置后,四氯化碳层显橙红色的是 (填序号)。
A.溴化钠溶液,B.碘化钾溶液。
(11)用电子式表示MgCl2的形成过程 。
查看习题详情和答案>>
(13分)
(1)稀有气体不能形成双原子分子是因为 。
(2)多电子原子中,在离核较近的区域内运动的电子能量 (填较高或较低)。
(3)不含中子的核素的核组成符号为 。
(4)ⅥA族氢化物中沸点最低的是 (写化学式)。
(5)在金属元素与非金属元素的分界线附近可以寻找制备 材料的元素;在
中可寻找制备催化剂及耐高温、耐腐蚀的元素。
(6)下列选项中,随原子序数递增而呈周期性变化的是 (填序号,后同);其中,起决定性作用的是
A.原子核外电子排布,B.原子半径,C.主要化合价,D.元素的金属性或非金属性。
(7)下列核素中,用于考古时测文物年代的是 (填序号)。
A.2H和3H, B.14C, C.235U。
(8)下列实验中,可产生白烟的是 (填序号)。
A.氢气与氯气反应,B钠与氯气反应。
(9)下列反应中,更剧烈的是 (填序号)。
A.钠与水反应,B.钾与水反应。
(10)取下列溶液分装两试管,再分别依次加入少量氯水和少量四氯化碳,用力振荡、静置后,四氯化碳层显橙红色的是 (填序号)。
A.溴化钠溶液,B.碘化钾溶液。
(11)用电子式表示MgCl2的形成过程 。
(14分)(1)二氧化硫的催化氧化的过程如图所示,
其中a、c二步的化学方程式可表示为:
SO2+V2O5 SO3+ V2O4
SO3+ V2O4
4VOSO4+O2 2V2O5+4SO3。
2V2O5+4SO3。
该反应的催化剂是 (写化学式)
(2)压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO2 7%,O2 11%,N2 82%):
| 压强/MPa 温度/℃ | 0.1[ | 0.5 | 1 | 10 |
| 400 | 99.2% | 99.6% | 99.7% | 99.9% |
| 500 | 93.5% | 96.9% | 97.8% | 99.3% |
| 600 | 73.7% | 85.8% | 89.5% | 96.4% |

(3)550 ℃时,SO2转化为SO3的平衡转化率(α)与体系总压强(p)的关系如右图所示。将2.0 mol SO2和1.0 mol O2置于5 L密闭容器中,反应达平衡后,体系总压强为0.10 M Pa。试计算反应2SO3
 2SO2+O2 在550 ℃时的平衡常数K= 。
2SO2+O2 在550 ℃时的平衡常数K= 。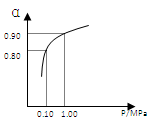
反应达平衡后,下列措施中能使n(SO3)/n(SO2)增大的是
A.升高温度 B.充入He(g),使体系总压强增大
C.再充入2 mol SO2和1 mol O2 D.再充入1 mol SO2和1 mol O2
(4)SO3溶于水得到硫酸。在25°C下,将x mol·L-1的氨水与y mol·L-1的硫酸等体积混合,反应后溶液中显中性,则c(NH4+) 2 c(SO42-)(填“>”、“<”或“=”);用含x和y的代数式表示出氨水的电离平衡常数 。 查看习题详情和答案>>