摘要:A:Al2O3 B:Al(OH)3 C:AlCl3 D:NaAlO2 4AlCl3+6Na2O2=4Al(OH)3+12NaCl
网址:http://m.1010jiajiao.com/timu3_id_41727[举报]
下列关于除去物质中杂质的方案设计,所选除杂试剂合理的是( )
|
查看习题详情和答案>>
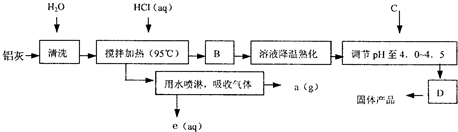
聚合氯化铝晶体的化学式为[Al2(OH)nCl6-n·xH2O]m,它是一种高效无机水处理剂,它的制备原理是调节增大AlCl3溶液的pH,通过促进其水解而结晶析出。其制备原料主要是铝加工行业的废渣--铝灰,它主要含
Al2O3、Al,还有SiO2等杂质。聚合氯化铝生产的工艺流程如下
Al2O3、Al,还有SiO2等杂质。聚合氯化铝生产的工艺流程如下

(1)搅拌加热操作过程中发生反应的离子方程式:________________、______________。
(2)生产过程中操作B和D的名称均为________(B和D为简单操作)。
(3)反应中副产品a是________(用化学式表示)。
(4)生产过程中可循环使用的物质是________(用化学式表示)。
(5)调节pH至4.0~4.5的目的是 __________________________。
(6)实验室要测定水处理剂产品中n和x的值。为使测定结果更准确,需得到的晶体较纯净。生产过程中C物质可选用__________
A.NaOH B.Al C.氨水 D.Al2O3 E.NaAlO2
查看习题详情和答案>>
(2)生产过程中操作B和D的名称均为________(B和D为简单操作)。
(3)反应中副产品a是________(用化学式表示)。
(4)生产过程中可循环使用的物质是________(用化学式表示)。
(5)调节pH至4.0~4.5的目的是 __________________________。
(6)实验室要测定水处理剂产品中n和x的值。为使测定结果更准确,需得到的晶体较纯净。生产过程中C物质可选用__________
A.NaOH B.Al C.氨水 D.Al2O3 E.NaAlO2
某混合物粉末可能含有Al、Fe、FeO、Al2O3,某研究小组在实验室积极探究其组成.
(1)研究小组首先排除了含有单质Al的可能性,加入的试剂是______(填序号)
A.硫酸 B.盐酸 C.氨水 D.氢氧化钠溶液
证明不含单质铝的现象是______.
(2)该混合物的组成基本确定为Fe、FeO、Al2O3.请以上述粉末为样品,验证其组成.限选实验仪器与试剂:烧杯、试管、玻璃棒、胶头滴管、药匙、过滤器;20%KSCN、3mol/LNaOH、3mol/L盐酸、3% H2O2、3mol/LCuSO4、蒸馏水.
根据你设计的实验方案,在答题卡上按下表的格式写出空白部分的实验操作、预期现象和结论.
| 实验操作 | 预期现象和结论 |
| 步骤1:取少量粉末于烧杯中,加入足量3mol/LNaOH溶液,充分搅拌,过滤,洗涤. | 粉末减少,说明粉末可能含有Al2O3 |
| 步骤2:取少量步骤1的滤液于试管中,逐滴滴加3mol/L盐酸至过量. | ______, 说明粉末中含有Al2O3. |
| 步骤3:将步骤1的滤渣转移到烧杯B中,加入足量3mol/L CuSO4,充分搅拌,过滤,洗涤. | 有红色固体生成,说明粉末中含有______. |
| 步骤4:______ | ______ |
 乙
乙 丙
丙 甲,则甲不可能是
甲,则甲不可能是