网址:http://m.1010jiajiao.com/timu3_id_41364[举报]
1,3―丙二醇是重要的化工原料,用乙烯合成1,3―丙二醇的路线如下:
CH2=CH2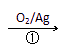
![]()
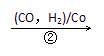 HOCH2CH2CHO
HOCH2CH2CHO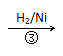 HOCH2CH2CH2OH
HOCH2CH2CH2OH
⑴通过反应①用乙烯和空气混合气体制备![]() ,测得反应前和某一时刻气体的体积分数如下表。
,测得反应前和某一时刻气体的体积分数如下表。
| C2H4 | O2 | N2 |
| |
| 反应前体积分数 | 25.0% | 15.0% | 60.0% | 0 |
| 某一时刻体积分数 | 5.56% | 5.54% | 66.7% | 22.2% |
计算此时乙烯的转化率。
⑵某化工厂已购得乙烯14t,考虑到原料的充分利用,反应②、③所需的CO和H2可由以下两个反应获得:
C+H2O![]() CO+H2 CH4+H2O
CO+H2 CH4+H2O![]() CO+3H2
CO+3H2
假设在生产过程中,反应②中CO和H2、反应③中H2均过量20%,且反应①、②、③中各有机物的转化率均为100%。
计算至少需要焦炭、甲烷各多少吨,才能满足生产需要?
查看习题详情和答案>>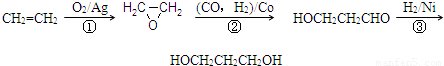
(1)通过反应①用乙烯和空气混合气体制备
| C2H4 | O2 | N2 | ||
| 反应前体积分数 | 25.0% | 15.0% | 60.0% | |
| 某一时刻体积分数 | 5.56% | 5.54% | 66.7% | 22.2% |
(2)某化工厂已购得乙烯14t,考虑到原料的充分利用,反应②、③所需的CO和H2可由以下两个反应获得:
C+H2O
 CO+H2
CO+H2 CH4+H2O
 CO+3H2
CO+3H2假设在生产过程中,反应②中CO和H2、反应③中H2均过量20%,且反应①、②、③中各有机物的转化率均为100%.计算至少需要焦炭、甲烷各多少吨,才能满足生产需要?
查看习题详情和答案>>
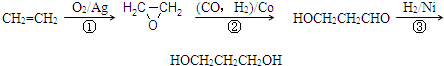
(1)通过反应①用乙烯和空气混合气体制备
| C2H4 | O2 | N2 | ||
| 反应前体积分数 | 25.0% | 15.0% | 60.0% | 0 |
| 某一时刻体积分数 | 5.56% | 5.54% | 66.7% | 22.2% |
(2)某化工厂已购得乙烯14t,考虑到原料的充分利用,反应②、③所需的CO和H2可由以下两个反应获得:
C+H2O
| ||
CH4+H2O
| ||
假设在生产过程中,反应②中CO和H2、反应③中H2均过量20%,且反应①、②、③中各有机物的转化率均为100%.计算至少需要焦炭、甲烷各多少吨,才能满足生产需要?
(12分)利用焦炭或天然气制取廉价的CO和H2,再用于氨合成和有机合成是目前工业生产的重要途径。回答下列问题:
(1)甲烷在高温下与水蒸气反应的化学方程式为:CH4+H2O=CO+3H2。部分物质的燃烧热数据如下表:
|
物 质 |
燃烧热(kJ·mol-1) |
|
H2(g) |
-285.8 |
|
CO(g) |
-283.0 |
|
CH4(g) |
-890.3 |
已知1 mol H2O(g)转变为1 mol H2O(l)时放出44.0 kJ热量。写出CH4和水蒸气在高温下反应的热化学方程式 。
(2)500℃、50MPa时,在容积为V L的容器中加入1 mol N2、3 mol H2,,此时N2的转化率为a。则平衡时NH3的浓度为 。
(3)1,3―丙二醇是重要的化工原料,用乙烯合成1,3―丙二醇的路线如下:

某化工厂已购得乙烯11.2 t,考虑到原料的充分利用,反应②、③所需的CO和H2可由以下两个反应获得:
C+H2O CO+H2 CH4+H2O
CO+H2 CH4+H2O CO+3H2
CO+3H2
假设在生产过程中,反应①、②、③中各有机物的转化率均为100%。且反应②中CO和H2、反应③中H2的转化率都为80%,计算至少需要焦炭 吨、甲烷 吨,
才能满足生产需要。
查看习题详情和答案>>
![]() 利用焦炭或天然气制取廉价的CO和H2,再用于氨合成和有机合成是目前工业生产的重要途径。回答下列问题:
利用焦炭或天然气制取廉价的CO和H2,再用于氨合成和有机合成是目前工业生产的重要途径。回答下列问题:
(1)甲烷在高温下与水蒸气反应的化学方程式为:CH4+H2O CO+3H2。部分物质的燃烧热数据如下表:
| 物 质 | 燃烧热(kJ·mol-1) |
| H2(g) | -285.8 |
| CO(g) | -283.0 |
| CH4(g) | -890.3 |
已知1mol H2O(g)转变为1 mol H2O(l)时放出44.0 kJ热量。写出CH4和水蒸气在高温下反应的热化学方程式 。
(2)500℃、50MPa时,在容积为VL的容器中加入1 mol N2、3 molNH3,反应达平衡后测得平衡常数为K,此时CH4的转化率为a。则K和a的关系是K= 。
(3)1,3―丙二醇是重要的化工原料,用乙烯合成1,3―丙二醇的路线如下:
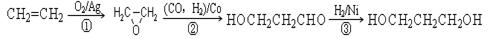
某化工厂已购得乙烯11.2 t,考虑到原料的充分利用,反应②、③所需的CO和H2可由以下两个反应获得:C+H2O![]() CO+H2 CH4+H2O
CO+H2 CH4+H2O![]() CO+3H2
CO+3H2
假设在生产过程中,反应①、②、③中各有机物的转化率均为100%。且反应②中CO和H2、反应③中H2的转化率都为80%,计算至少需要焦炭、甲烷各多少吨,才能满足生产需要?
查看习题详情和答案>>