摘要: 热化学方程式 ①.热化学方程式中必须注明物质的聚集状态: 气态 ②.热化学方程式中的化学计量数可以是整数. 也可以是 . ③.与参加反应的物质的物质的量有关.同一化学反应中.热化学方程式中物质的化学计量数不同. △H也不同.化学计量数加倍. △H . ④.书写热化学方程式时应注明反应的温度和压强.如果不注明温度和压强.则表示是在250C.101KPa条件下的反应热
网址:http://m.1010jiajiao.com/timu3_id_411934[举报]
[化学--化学与技术]硫酸工业在国民经济中占有极其重要的地位.请回答硫酸工业中的如下问题:
(1)若从下列四个城市中选择一处新建一座硫酸厂,你认为厂址宜选在
A.有丰富黄铁矿资源的城市
B.风光秀丽的旅游城市
C.消耗硫酸甚多的工业城市
D.人口稠密的文化、商业中心城市
(2)CuFeS2是黄铁矿的另一成分,煅烧时CuFeS2转化为CuO、Fe2O3 和SO2,该反应的化学方程式为
(3)为提高SO3吸收率,实际生产中通常用
(4)已知反应2SO2+O2?2SO3△H<0,现将0.050mol SO2和0.030mol O2充入容积为1L的密闭容器中,反应在一定条件下达到平衡,测得反应后容器压强缩小到原来压强的75%,则该条件下SO2的转化率为
(5)由硫酸厂沸腾炉排出的矿渣中含有Fe2O3、CuO、CuSO4(由CuO与SO3 在沸腾炉中化合而成),其中硫酸铜的质量分数随沸腾炉温度不同而变化(见下表)
已知CuSO4 在低于660℃时不会分解,请简要分析上表中CuSO4的质量分数随温度升高而降低的原因
(6)在硫酸工业尾气中,SO2是主要大气污染物,必须进行净化处理,处理方法可用
查看习题详情和答案>>
(1)若从下列四个城市中选择一处新建一座硫酸厂,你认为厂址宜选在
C
C
的郊区(填标号);A.有丰富黄铁矿资源的城市
B.风光秀丽的旅游城市
C.消耗硫酸甚多的工业城市
D.人口稠密的文化、商业中心城市
(2)CuFeS2是黄铁矿的另一成分,煅烧时CuFeS2转化为CuO、Fe2O3 和SO2,该反应的化学方程式为
4CuFeS2+13O2
4CuO+2Fe2O3+8SO2
| ||
4CuFeS2+13O2
4CuO+2Fe2O3+8SO2
.
| ||
(3)为提高SO3吸收率,实际生产中通常用
98.3%的浓硫酸
98.3%的浓硫酸
吸收SO3.(4)已知反应2SO2+O2?2SO3△H<0,现将0.050mol SO2和0.030mol O2充入容积为1L的密闭容器中,反应在一定条件下达到平衡,测得反应后容器压强缩小到原来压强的75%,则该条件下SO2的转化率为
80%
80%
;该条件下的平衡常数为1.6×103
1.6×103
.(5)由硫酸厂沸腾炉排出的矿渣中含有Fe2O3、CuO、CuSO4(由CuO与SO3 在沸腾炉中化合而成),其中硫酸铜的质量分数随沸腾炉温度不同而变化(见下表)
| 沸腾炉温度/℃ | 600 | 620 | 640 | 660 |
| 炉渣中CuSO4的质量分数/% | 9.3 | 9.2 | 9.0 | 8.4 |
SO2转化为SO3是正反应放热的可逆反应,随温度升高,平衡左移,SO3物质的量减少,所以CuSO4的量减少
SO2转化为SO3是正反应放热的可逆反应,随温度升高,平衡左移,SO3物质的量减少,所以CuSO4的量减少
.(6)在硫酸工业尾气中,SO2是主要大气污染物,必须进行净化处理,处理方法可用
石灰水
石灰水
(填名称)吸收,然后再用硫酸处理,重新生成SO2和一种生产水泥的辅料,写出这两步反应的化学方程式SO2+Ca(OH)2═CaSO3↓+H2O、CaSO3+H2SO4═CaSO4+SO2↑+H2O;
SO2+Ca(OH)2═CaSO3↓+H2O、CaSO3+H2SO4═CaSO4+SO2↑+H2O;
.化学实验室产生的废液中含有大量会污染环境的物质,为了保护环境,这些废液必须经处理后才能排放.某化学实验室产生的废液中含有两种金属离子:Fe3+、Cu2+,化学小组设计了如图所示的方案对废液进行处理,以回收金属,保护环境.
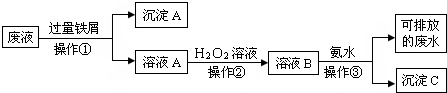
(1)操作①的名称是
(2)操作②反应时还需加入少量硫酸,操作②中观察到的实验现象是
(3)操作②中发生反应的离子方程式为
(4)简述以沉淀A为原料制得金属铜和绿矾晶体(FeSO4?7H2O)的实验方案
查看习题详情和答案>>

(1)操作①的名称是
过滤
过滤
.(2)操作②反应时还需加入少量硫酸,操作②中观察到的实验现象是
溶液由浅绿色变为棕黄色,有少量气泡出现
溶液由浅绿色变为棕黄色,有少量气泡出现
.(3)操作②中发生反应的离子方程式为
2Fe2++H2O2+2H+=2Fe3++H2O
2Fe2++H2O2+2H+=2Fe3++H2O
.(4)简述以沉淀A为原料制得金属铜和绿矾晶体(FeSO4?7H2O)的实验方案
在沉淀中加入稀硫酸,搅拌,至不再有气泡产生,过滤,洗涤固体并干燥得铜.滤液加热浓缩后冷却结晶,过滤,干燥得绿矾.
在沉淀中加入稀硫酸,搅拌,至不再有气泡产生,过滤,洗涤固体并干燥得铜.滤液加热浓缩后冷却结晶,过滤,干燥得绿矾.
.化学是一门以实验为基础的自然科学,掌握实验方法以及完成化学实验所必需的技能,是学好化学的关键.试回答下列与实验有关的问题:
(1)某同学认为MnO2与浓HCl反应制得的Cl2中含有HCl气体,该同学设计如图所示装置进行验证.最终该同学判定含有HCl气体的依据是:装置C中的试纸颜色无变化,装置D中产生白色沉淀.(部分夹持装置和加热装置省略)
①装置B中的试剂是
②装置C的作用是
(2)某课外研究小组设计如图所示的实验过程,用石油化学工业的废弃催化剂(主要成分:Ag/a-Al2O3)来回收金属银和a-Al2O3,a-Al2O3作为催化剂的载体,且不溶于硝酸.(部分操作过程省略)

①进行操作Ⅰ可选用如图所示装置中的装置

②实验操作Ⅱ中,所需的主要玻璃仪器有
③实验操作Ⅱ中能否用自来水代替蒸馏水,
查看习题详情和答案>>
(1)某同学认为MnO2与浓HCl反应制得的Cl2中含有HCl气体,该同学设计如图所示装置进行验证.最终该同学判定含有HCl气体的依据是:装置C中的试纸颜色无变化,装置D中产生白色沉淀.(部分夹持装置和加热装置省略)

①装置B中的试剂是
四氯化碳
四氯化碳
(填写名称);②装置C的作用是
检验Cl2是否除净,防止干扰实验效果
检验Cl2是否除净,防止干扰实验效果
.(2)某课外研究小组设计如图所示的实验过程,用石油化学工业的废弃催化剂(主要成分:Ag/a-Al2O3)来回收金属银和a-Al2O3,a-Al2O3作为催化剂的载体,且不溶于硝酸.(部分操作过程省略)

①进行操作Ⅰ可选用如图所示装置中的装置
a
a
(选填a、b、c);
②实验操作Ⅱ中,所需的主要玻璃仪器有
漏斗、烧杯、玻璃棒
漏斗、烧杯、玻璃棒
;③实验操作Ⅱ中能否用自来水代替蒸馏水,
否
否
(填“能”或“否”);为什么?因为自来水中含有Cl-,会发生反应Ag++Cl-=AgCl↓,导致回收的a-Al2O3中掺杂AgCl杂质
因为自来水中含有Cl-,会发生反应Ag++Cl-=AgCl↓,导致回收的a-Al2O3中掺杂AgCl杂质
(请结合有关离子方程式回答).
[化学与技术]
我国有丰富的天然气资源.以天然气为原料合成尿素的主要步骤如下图所示(图中某些转化步骤及生成物未列出):
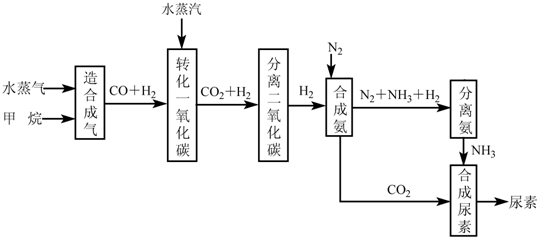
请填写下列空白:
(1)已知0.5mol甲烷和0.5mol水蒸气在t℃,p k Pa时,完全反应生成一氧化碳和氢气(合成气),吸收了a kJ热量.该反应的热化学方程式是: .
(2)上述流程中,工业上分离H2、CO2合理的方法是 .
A.混合气先通入氢氧化钠溶液,再在溶液中加盐酸
B.混合气加压冷却,使CO2液化
C.混合气用氨水洗涤
D.混合气先通入到石灰浆,然后高温煅烧固体,
(3)为了保证氨气顺利合成,在空气进入合成塔之前必须对空气进行 ,目的是 ;在合成氨的实际生产过程中,常采取将生成的氨从混合气体中分离出来,分离出氨的方法: .
(4)合理地利用资源不仅可以提高经济效益,而且也是对社会、对全人类负责的表现,请用线段和箭头画出图中的两处合理利用资源情况. 查看习题详情和答案>>
我国有丰富的天然气资源.以天然气为原料合成尿素的主要步骤如下图所示(图中某些转化步骤及生成物未列出):

请填写下列空白:
(1)已知0.5mol甲烷和0.5mol水蒸气在t℃,p k Pa时,完全反应生成一氧化碳和氢气(合成气),吸收了a kJ热量.该反应的热化学方程式是:
(2)上述流程中,工业上分离H2、CO2合理的方法是
A.混合气先通入氢氧化钠溶液,再在溶液中加盐酸
B.混合气加压冷却,使CO2液化
C.混合气用氨水洗涤
D.混合气先通入到石灰浆,然后高温煅烧固体,
(3)为了保证氨气顺利合成,在空气进入合成塔之前必须对空气进行
(4)合理地利用资源不仅可以提高经济效益,而且也是对社会、对全人类负责的表现,请用线段和箭头画出图中的两处合理利用资源情况. 查看习题详情和答案>>
Ⅰ.化学实验室制取氯化氢气体的方法之一是将浓硫酸滴入浓盐酸中。请从下图中挑选所需仪器,在方框内画出用该方法制备、收集干燥氯化氢气体的装置简图,并在图中标明所用试剂。(仪器可重复使用,固定装置不必画出)

|
Ⅱ.实验室制备少量硫酸亚铁晶体的实验步骤如下:取过量洁净的铁屑,加入20%—30%的稀硫酸溶液,在50℃—80℃水浴中加热至不再产生气泡。将溶液趁热过滤,滤液移至试管中,用橡胶塞塞紧试管口,静置、冷却一段时间后收集产品。
(1)写出该实验制备硫酸亚铁的化学方程式:__________________________________。
(2)硫酸溶液过稀会导致_________________________________________________。
(3)采用水浴加热的原因是__________________________________________________。
(4)反应时铁屑过量的目的是(用离子方程式表示)____________________________。
(5)溶液趁热过滤的原因是______________________。塞紧试管口的目的是__________________________。
(6)静置冷却一段时间后,在试管中观察到的现象是_____________________________。
查看习题详情和答案>>