摘要:13.NO + O2 + NO2 +H2O - HNO3.是多组化学计量数的化学方程式.当氧气有1/3被NO还原时.此反应中各化学计量数之比为 A.4∶9∶24∶14∶28 B.1∶1∶1∶1∶2 C.8∶9∶12∶10∶20 D.任意比均可
网址:http://m.1010jiajiao.com/timu3_id_411005[举报]
(2013?北京)NOx是汽车尾气中的主要污染物之一.
(1)NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:
(2)汽车发动机工作时会引发N2和O2反应,其能量变化示意图如下:

①写出该反应的热化学方程式:
②随温度升高,该反应化学平衡常数的变化趋势是:
(3)在汽车尾气系统中装置催化转化器,可有效降低NOX的排放.
①当尾气中空气不足时,NOx在催化转化器中被还原成N2排出.写出NO被CO还原的化学方程式:
②当尾气中空气过量时,催化转化器中的金属氧化物吸收NOx生成盐.其吸收能力顺序如下:12MgO<20CaO<38SrO<56BaO.原因是:
(4)通过NOx传感器可监测NOx的含量,其工作原理示意图如下:

①Pt电极上发生的是
②写出NiO电极的电极反应式:
查看习题详情和答案>>
(1)NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:
3NO2+H2O=2HNO3+NO
3NO2+H2O=2HNO3+NO
.(2)汽车发动机工作时会引发N2和O2反应,其能量变化示意图如下:

①写出该反应的热化学方程式:
N2(g)+O2(g)=2NO(g)△H=+183kJ?moL-1
N2(g)+O2(g)=2NO(g)△H=+183kJ?moL-1
.②随温度升高,该反应化学平衡常数的变化趋势是:
增大
增大
.(3)在汽车尾气系统中装置催化转化器,可有效降低NOX的排放.
①当尾气中空气不足时,NOx在催化转化器中被还原成N2排出.写出NO被CO还原的化学方程式:
2CO+2NO
N2+2CO2
| ||
2CO+2NO
N2+2CO2
.
| ||
②当尾气中空气过量时,催化转化器中的金属氧化物吸收NOx生成盐.其吸收能力顺序如下:12MgO<20CaO<38SrO<56BaO.原因是:
根据Mg、Ca、Sr和Ba的质子数,得知它们均为ⅡA族元素.同一主族的元素,从上到下,原子半径逐渐增大
根据Mg、Ca、Sr和Ba的质子数,得知它们均为ⅡA族元素.同一主族的元素,从上到下,原子半径逐渐增大
,元素的金属性逐渐增强,金属氧化物对NOx的吸收能力逐渐增强.(4)通过NOx传感器可监测NOx的含量,其工作原理示意图如下:

①Pt电极上发生的是
还原
还原
反应(填“氧化”或“还原”).②写出NiO电极的电极反应式:
NO+O2--2e-=NO2
NO+O2--2e-=NO2
.NO是一种剧毒气体,但近年来发现许多生物体组织中存在少量NO,它有扩张血管、免疫、增强记忆的功能,因而成为当前生命科学的研究热点.
(1)写出自然界形成NO的化学方程式:
(2)NO在大气层中可发生反应:NO+O3→NO2+O…①,NO2+O═NO+O2…②
上述反应①中,NO是
(3)为了消除NO对环境的污染,根据氧化还原反应原理,可选用NH3使NO转化为两种无毒气体(其中之一是水蒸气),该反应需要催化剂参加,其化学方程式为
查看习题详情和答案>>
(1)写出自然界形成NO的化学方程式:
N2+O2
2NO
| ||
N2+O2
2NO
.
| ||
(2)NO在大气层中可发生反应:NO+O3→NO2+O…①,NO2+O═NO+O2…②
上述反应①中,NO是
还原
还原
剂,上述反应②中,NO是还原
还原
产物.(3)为了消除NO对环境的污染,根据氧化还原反应原理,可选用NH3使NO转化为两种无毒气体(其中之一是水蒸气),该反应需要催化剂参加,其化学方程式为
4NH3+6NO
5N2+6H2O
| ||
| △ |
4NH3+6NO
5N2+6H2O
.
| ||
| △ |
水处理技术在生产、生活中应用广泛.
(1)工业上常用绿矾做混凝剂除去天然水中含有的悬浮物和胶体,为了达到更好的效果,要将待处理的水pH调到9左右,再加入绿矾.请解释这一做法的原因: (用必要的离子方程式和文字描述).
(2)根据水中Ca2+,Mg2+的多少,把天然水分为硬水和软水,硬水必须经过软化才能使用.
①硬水软化的方法通常有 、 和离子交换法.离子交换树脂使用了一段时间后,逐渐由NaR型变为CaR2(或MgR2)型,而失去交换能力.把CaR2(或MgR2)型树脂置于 中浸泡一段时间,便可再生.
②当洗涤用水硬度较大时,洗衣粉与肥皂相比, 洗涤效果较好,原因是 .
(3)最近我国某地苯胺大量泄漏于生活饮用水的河道中,当地采取的应急措施之一是向河水中撒入大量的活性碳,活性炭的作用是 .
(4)若生活污水中含大量的氮化合物,通常用生物膜脱氮工艺进行处理.首先在
消化细菌作用下将N
氧化为N
: N
+ O2═ N
+ H++ H2O.然后,加入甲醇与N
生成N2: N
+ CH3OH═ N2+ CO2+ H2O+ OH-(试配平以上两个离子方程式).
查看习题详情和答案>>
(1)工业上常用绿矾做混凝剂除去天然水中含有的悬浮物和胶体,为了达到更好的效果,要将待处理的水pH调到9左右,再加入绿矾.请解释这一做法的原因:
(2)根据水中Ca2+,Mg2+的多少,把天然水分为硬水和软水,硬水必须经过软化才能使用.
①硬水软化的方法通常有
②当洗涤用水硬度较大时,洗衣粉与肥皂相比,
(3)最近我国某地苯胺大量泄漏于生活饮用水的河道中,当地采取的应急措施之一是向河水中撒入大量的活性碳,活性炭的作用是
(4)若生活污水中含大量的氮化合物,通常用生物膜脱氮工艺进行处理.首先在
消化细菌作用下将N
| H | + 4 |
| O | - 3 |
| H | + 4 |
| O | - 3 |
| O | - 3 |
| O | - 3 |
 甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化).下列各组物质中,不满足图示转化关系的是( ) 甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化).下列各组物质中,不满足图示转化关系的是( )
|
查看习题详情和答案>>
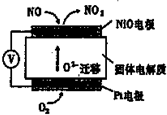 如图装置可用来监测空气中NO的含量,下列说法正确的是( )
如图装置可用来监测空气中NO的含量,下列说法正确的是( )