摘要:30.黄铜矿(主要成分为CuFeS2)是制取铜及其化合物的主要原料之一.还可制备硫及铁的化合物. (1)冶炼铜的有关反应为:8CuFeS2+21O28Cu+4FeO+2Fe2O3+16SO2. 已知在CuFeS2中Fe的化合价为+2.则该冶炼铜的反应中被氧化的元素是 . (2)上述冶炼过程中会产生大量SO2.下列处理方案中不合理的是 . a.高空排放 b.用于制备硫酸 c.用纯碱溶液吸收制取Na2SO3 d.用浓硫酸吸收 (3)过二硫酸钾(K2S2O8)具有强氧化性.可将I-氧化为I2.有关离子方程式为: +2I-2+I2.通过改变反应途径.Fe3+.Fe2+均可催化上述反应.Fe3+对上述反应的催化过程(Fe3+参与反应)用离子方程式可表示为 . . (4)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3.FeO.SiO2.Al2O3)可制备Fe2O3.方法为:a.用稀盐酸浸取炉渣.过滤.b.滤液先经过氧化.再加入过量的NaOH溶液.反应后过滤,c.将沉淀洗涤.干燥.煅烧得Fe2O3.据以上信息回答下列问题: ①b中除去Al3+的有关反应的离子方程式为 . ②2.3g黄铜矿(含CuFeS280%)理论上可制得Fe2O3 g.
网址:http://m.1010jiajiao.com/timu3_id_409382[举报]
铁及其化合物之间的相互转化可用下式表示:
Fe2+
Fe3+
FeO42-(高铁酸根离子)
回答下列有关问题:
(1)Fe与过量稀硫酸反应可以制取FeSO4.若用反应所得的酸性溶液,实现上述①的转化,要求产物纯净.可选用的试剂是
a.Cl2 b.Fe c.HNO3 d.H2O2
(2)上述转化得到的硫酸铁可用于电化浸出黄铜矿精矿工艺.精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2+4Fe3+=Cu2++5Fe2++2S.(CuFeS2中S为-2价)则下列说法正确的是
a.从物质分类的角度看,黄铜矿属于合金
b.反应中,所有铁元素均被还原
c.反应中,CuFeS2 既作氧化剂又作还原剂
d.当转移1mol电子时,46g CuFeS2参加反应
(3)下述反应中,若FeSO4和O2的系数比为2:1,试配平下列方程式:FeSO4+K2O2→K2FeO4+K2O+K2SO4+O2↑
(4)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中发生反应生成Fe(OH)3.高铁酸钾作为水处理剂发挥的作用是
查看习题详情和答案>>
Fe2+
| ① |
| ④ |
| ② |
| ③ |
回答下列有关问题:
(1)Fe与过量稀硫酸反应可以制取FeSO4.若用反应所得的酸性溶液,实现上述①的转化,要求产物纯净.可选用的试剂是
d
d
(选填序号);a.Cl2 b.Fe c.HNO3 d.H2O2
(2)上述转化得到的硫酸铁可用于电化浸出黄铜矿精矿工艺.精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2+4Fe3+=Cu2++5Fe2++2S.(CuFeS2中S为-2价)则下列说法正确的是
d
d
(选填序号);a.从物质分类的角度看,黄铜矿属于合金
b.反应中,所有铁元素均被还原
c.反应中,CuFeS2 既作氧化剂又作还原剂
d.当转移1mol电子时,46g CuFeS2参加反应
(3)下述反应中,若FeSO4和O2的系数比为2:1,试配平下列方程式:FeSO4+K2O2→K2FeO4+K2O+K2SO4+O2↑
(4)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中发生反应生成Fe(OH)3.高铁酸钾作为水处理剂发挥的作用是
净水
净水
、消毒
消毒
.铁及其化合物之间的相互转化可用下式表示:
Fe2+
Fe3+
FeO42-(高铁酸根离子)
回答下列有关问题:
(1)Fe与过量稀硫酸反应可以制取FeSO4.若用反应所得的酸性溶液,实现上述①的转化,要求产物纯净.可选用的试剂是______(选填序号);
a.Cl2 b.Fe c.HNO3 d.H2O2
(2)上述转化得到的硫酸铁可用于电化浸出黄铜矿精矿工艺.精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2+4Fe3+=Cu2++5Fe2++2S.(CuFeS2中S为-2价)则下列说法正确的是______(选填序号);
a.从物质分类的角度看,黄铜矿属于合金
b.反应中,所有铁元素均被还原
c.反应中,CuFeS2 既作氧化剂又作还原剂
d.当转移1mol电子时,46g CuFeS2参加反应
(3)下述反应中,若FeSO4和O2的系数比为2:1,试配平下列方程式:FeSO4+K2O2→K2FeO4+K2O+K2SO4+O2↑
(4)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中发生反应生成Fe(OH)3.高铁酸钾作为水处理剂发挥的作用是______、______.
查看习题详情和答案>>
Fe2+
| ① |
| ④ |
| ② |
| ③ |
回答下列有关问题:
(1)Fe与过量稀硫酸反应可以制取FeSO4.若用反应所得的酸性溶液,实现上述①的转化,要求产物纯净.可选用的试剂是______(选填序号);
a.Cl2 b.Fe c.HNO3 d.H2O2
(2)上述转化得到的硫酸铁可用于电化浸出黄铜矿精矿工艺.精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2+4Fe3+=Cu2++5Fe2++2S.(CuFeS2中S为-2价)则下列说法正确的是______(选填序号);
a.从物质分类的角度看,黄铜矿属于合金
b.反应中,所有铁元素均被还原
c.反应中,CuFeS2 既作氧化剂又作还原剂
d.当转移1mol电子时,46g CuFeS2参加反应
(3)下述反应中,若FeSO4和O2的系数比为2:1,试配平下列方程式:FeSO4+K2O2→K2FeO4+K2O+K2SO4+O2↑
(4)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中发生反应生成Fe(OH)3.高铁酸钾作为水处理剂发挥的作用是______、______.
铁及其化合物之间的相互转化可用下式表示:
Fe2+ Fe3+
Fe3+ FeO42-(高铁酸根离子)
FeO42-(高铁酸根离子)
回答下列有关问题:
(1)Fe与过量稀硫酸反应可以制取FeSO4.若用反应所得的酸性溶液,实现上述①的转化,要求产物纯净.可选用的试剂是______(选填序号);
a.Cl2 b.Fe c.HNO3 d.H2O2
(2)上述转化得到的硫酸铁可用于电化浸出黄铜矿精矿工艺.精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2+4Fe3+=Cu2++5Fe2++2S.(CuFeS2中S为-2价)则下列说法正确的是______(选填序号);
a.从物质分类的角度看,黄铜矿属于合金
b.反应中,所有铁元素均被还原
c.反应中,CuFeS2 既作氧化剂又作还原剂
d.当转移1mol电子时,46g CuFeS2参加反应
(3)下述反应中,若FeSO4和O2的系数比为2:1,试配平下列方程式:FeSO4+K2O2→K2FeO4+K2O+K2SO4+O2↑
(4)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中发生反应生成Fe(OH)3.高铁酸钾作为水处理剂发挥的作用是______、______.
查看习题详情和答案>>
Fe2+
 Fe3+
Fe3+ FeO42-(高铁酸根离子)
FeO42-(高铁酸根离子)回答下列有关问题:
(1)Fe与过量稀硫酸反应可以制取FeSO4.若用反应所得的酸性溶液,实现上述①的转化,要求产物纯净.可选用的试剂是______(选填序号);
a.Cl2 b.Fe c.HNO3 d.H2O2
(2)上述转化得到的硫酸铁可用于电化浸出黄铜矿精矿工艺.精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2+4Fe3+=Cu2++5Fe2++2S.(CuFeS2中S为-2价)则下列说法正确的是______(选填序号);
a.从物质分类的角度看,黄铜矿属于合金
b.反应中,所有铁元素均被还原
c.反应中,CuFeS2 既作氧化剂又作还原剂
d.当转移1mol电子时,46g CuFeS2参加反应
(3)下述反应中,若FeSO4和O2的系数比为2:1,试配平下列方程式:FeSO4+K2O2→K2FeO4+K2O+K2SO4+O2↑
(4)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中发生反应生成Fe(OH)3.高铁酸钾作为水处理剂发挥的作用是______、______.
查看习题详情和答案>>
铁及其化合物之间的相互转化可用下式表示:
Fe2+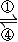 Fe3+
Fe3+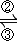 FeO42-(高铁酸根离子)
FeO42-(高铁酸根离子)
回答下列有关问题:
(1)Fe与过量稀硫酸反应可以制取FeSO4.若用反应所得的酸性溶液,实现上述①的转化,要求产物纯净.可选用的试剂是______(选填序号);
a.Cl2 b.Fe c.HNO3 d.H2O2
(2)上述转化得到的硫酸铁可用于电化浸出黄铜矿精矿工艺.精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2+4Fe3+=Cu2++5Fe2++2S.(CuFeS2中S为-2价)则下列说法正确的是______(选填序号);
a.从物质分类的角度看,黄铜矿属于合金
b.反应中,所有铁元素均被还原
c.反应中,CuFeS2 既作氧化剂又作还原剂
d.当转移1mol电子时,46g CuFeS2参加反应
(3)下述反应中,若FeSO4和O2的系数比为2:1,试配平下列方程式:FeSO4+K2O2→K2FeO4+K2O+K2SO4+O2↑
(4)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中发生反应生成Fe(OH)3.高铁酸钾作为水处理剂发挥的作用是______、______.
查看习题详情和答案>>
Fe2+
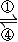 Fe3+
Fe3+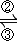 FeO42-(高铁酸根离子)
FeO42-(高铁酸根离子)回答下列有关问题:
(1)Fe与过量稀硫酸反应可以制取FeSO4.若用反应所得的酸性溶液,实现上述①的转化,要求产物纯净.可选用的试剂是______(选填序号);
a.Cl2 b.Fe c.HNO3 d.H2O2
(2)上述转化得到的硫酸铁可用于电化浸出黄铜矿精矿工艺.精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2+4Fe3+=Cu2++5Fe2++2S.(CuFeS2中S为-2价)则下列说法正确的是______(选填序号);
a.从物质分类的角度看,黄铜矿属于合金
b.反应中,所有铁元素均被还原
c.反应中,CuFeS2 既作氧化剂又作还原剂
d.当转移1mol电子时,46g CuFeS2参加反应
(3)下述反应中,若FeSO4和O2的系数比为2:1,试配平下列方程式:FeSO4+K2O2→K2FeO4+K2O+K2SO4+O2↑
(4)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中发生反应生成Fe(OH)3.高铁酸钾作为水处理剂发挥的作用是______、______.
查看习题详情和答案>>
工业上以黄铜矿(主要成分CuFeS2)为原料制备金属铜,有如下两种工艺。
I.火法熔炼工艺:将处理过的黄铜矿加人石英,再通人空气进行焙烧,即可制得粗铜。
(1)焙烧的总反应式可表示为:2CuFeS2 + 2SiO2+5O2=2Cu+2FeSi03+4SO2该反应的氧化剂是_____。
(2)下列处理SO2的方法,不合理的是_____
A.高空排放
B.用纯碱溶液吸收制备亚硫酸钠
C.用氨水吸收后,再经氧化制备硫酸铵
D.用BaCl2溶液吸收制备BaSO3
(3)炉渣主要成分有FeO 、Fe2O3 、SiO2 ,Al2O3等,为得到Fe2O3加盐酸溶解后,后续处理过程中,未涉及到的操作有_____。
A过滤;B加过量NaOH溶液;C蒸发结晶;D灼烧;E加氧化剂
II.FeCl3溶液浸取工艺:其生产流程如下图所示

(4)浸出过程中,CuFeS2与FeCl3溶液反应的离子方程式为? _____________。
(5)该工艺流程中,可以循环利用的物质是_____(填化学式)。
(6)若用石墨电极电解滤液,写出阳极的电极反式_____________。
(7)黄铜矿中含少量Pb,调节C1一浓度可控制滤液中Pb2+的浓度,当c(C1一)=2mo1·L-1时溶液中Pb2+物质的量浓度为__mol·L-1。[已知KSP(PbCl2)=1 x 10一5]
查看习题详情和答案>>