摘要: 由Fe(OH)3.NaCl.Ag2O.CaCO3.Al(OH)3组成的固体混合物.请用五种试剂逐一将这五种物质溶解而分离.这五种试剂依次是 A. 水.NaOH溶液.CO2.稀氨水.HCl溶液 B. NaOH溶液.水.稀氨水.CO2.HCl溶液 C. 水.NaOH溶液.稀氨水.CO2.HCl溶液 D. 稀氨水.水.NaOH溶液.CO2.HCl溶液
网址:http://m.1010jiajiao.com/timu3_id_409239[举报]
工业上制氯化铜无水物时,是将浓盐酸用蒸气加热至80℃左右,慢慢加入粗制氧化铜粉(含杂质氧化亚铁和SiO2),充分搅拌后使之溶解,制取流程如下:
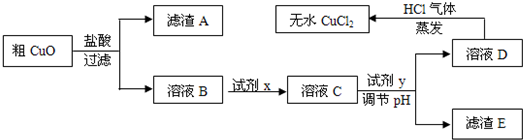
已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;常温时Ksp[Fe(OH)3]=c(Fe3+).c3(OH-)=1.0×10-38.试回答:
(1)根据常温时Fe(OH)3的Ksp计算,当溶液中的Fe3+完全沉淀(此时溶液中的Fe3+物质的量的浓度=10-5mol/L),溶液的pH=
(2)溶液D制取无水CuCl2时,需在HCl气体中蒸干,原因是
(3)粗CuO溶于过量盐酸后,得到的溶液B中加入试剂x将Fe2+氧化为Fe3+,试剂x可以是
A.KMnO4溶液 B.氯水 C.NaClO溶液 D.O3
若用H2O2溶液,则反应的离子方程式为
(4)溶液C加入试剂y,要调整溶液的pH至3-4,试剂y不能是
A.NaOH溶液 B.Cu(OH)2固体 C.Cu2(OH)2CO3固体 D.CuO固体
(5)将ag粗CuO经过以上一系列操作之后,最终得到bg无水CuCl2(不考虑实验过程中操作引起的损耗),下列说法正确的是
A.粗CuO中Cu2+数目小于
B.粗CuO中CuO物质的量小于
mol
C.粗CuO中所含的铜元素的质量分数为
x100%
D.粗CuO中关于CuO的量无法确定.
查看习题详情和答案>>

已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;常温时Ksp[Fe(OH)3]=c(Fe3+).c3(OH-)=1.0×10-38.试回答:
(1)根据常温时Fe(OH)3的Ksp计算,当溶液中的Fe3+完全沉淀(此时溶液中的Fe3+物质的量的浓度=10-5mol/L),溶液的pH=
3
3
.(2)溶液D制取无水CuCl2时,需在HCl气体中蒸干,原因是
HCl抑制CuCl2水解
HCl抑制CuCl2水解
.(3)粗CuO溶于过量盐酸后,得到的溶液B中加入试剂x将Fe2+氧化为Fe3+,试剂x可以是
BD
BD
(填以下选项序号).A.KMnO4溶液 B.氯水 C.NaClO溶液 D.O3
若用H2O2溶液,则反应的离子方程式为
2Fe2++H2O2+2H+=2Fe3++2H2O
2Fe2++H2O2+2H+=2Fe3++2H2O
.(4)溶液C加入试剂y,要调整溶液的pH至3-4,试剂y不能是
A
A
(填以下选项序号),原因是将引入新杂质NaCl
将引入新杂质NaCl
.A.NaOH溶液 B.Cu(OH)2固体 C.Cu2(OH)2CO3固体 D.CuO固体
(5)将ag粗CuO经过以上一系列操作之后,最终得到bg无水CuCl2(不考虑实验过程中操作引起的损耗),下列说法正确的是
ABD
ABD
.(NA表示阿伏伽德罗常数)A.粗CuO中Cu2+数目小于
| aNA |
| 80 |
| b |
| 135 |
C.粗CuO中所含的铜元素的质量分数为
| 64b |
| 135a |
D.粗CuO中关于CuO的量无法确定.
某固体混合物可能由K2SO4、NaCl、CuCl2和Na2SO3中的一种或几种组成.依次进行下列五步实验,观察到的现象记录如下:
①取一定量混合物加水溶解得无色透明溶液;
②向上述溶液中滴加足量BaCl2溶液,有白色沉淀生成,将该沉淀洗涤过滤干燥称得质量为a克;
③上述白色沉淀加入稀硝酸充分搅拌后,再次将沉淀洗涤过滤干燥称量,沉淀质量增加;
④往②的滤液中加入AgNO3溶液,有白色沉淀生成,该沉淀不溶于稀硝酸.
根据以上实验现象,可以判断出混合物中肯定含有的物质是
查看习题详情和答案>>
①取一定量混合物加水溶解得无色透明溶液;
②向上述溶液中滴加足量BaCl2溶液,有白色沉淀生成,将该沉淀洗涤过滤干燥称得质量为a克;
③上述白色沉淀加入稀硝酸充分搅拌后,再次将沉淀洗涤过滤干燥称量,沉淀质量增加;
④往②的滤液中加入AgNO3溶液,有白色沉淀生成,该沉淀不溶于稀硝酸.
根据以上实验现象,可以判断出混合物中肯定含有的物质是
Na2SO3
Na2SO3
;肯定不含有的物质是CuCl2
CuCl2
;不能判断混合物中是否含有的物质是K2SO4、NaCl
K2SO4、NaCl
.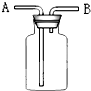 氯气是一种化学性质活泼的气体.
氯气是一种化学性质活泼的气体.(1)氯气是一种具有
刺激性
刺激性
气味的气体,密度比空气的大
大
(填“大”或“小”),若采用如图装置收集氯气,则氯气应由A
A
管(填“A”或“B”)通入.(2)氯气与NaOH溶液反应的化学方程式为
Cl2+2NaOH=NaCl+NaClO+H2O
Cl2+2NaOH=NaCl+NaClO+H2O
,该反应可用于工业上制取漂白液,其有效成分是NaClO
NaClO
.(2013?广东)大气中的部分碘源于O3对海水中I-的氧化.将O3持续通入NaI溶液中进行模拟研究.
(1)O3将I-氧化成I2的过程由3步反应组成:
①I-(aq)+O3(g)=IO-(aq)+O2(g)△H1
②IO-(aq)+H+(aq)?HOI(aq)△H2
③HOI(aq)+I-(aq)+H+(aq)?I2(aq)+H2O(l)△H3
总反应的化学方程式为
(2)在溶液中存在化学平衡:I2(aq)+I-(aq)?I3-(aq),其平衡常数表达式为
 .
.
(3)为探究Fe2+对O3氧化I-反应的影响(反应体系如图1),某研究小组测定两组实验中I3-浓度和体系pH,结果见图2和下表.
第1组实验中,导致反应后pH升高的原因是
②图1中的A为
③第2组实验进行18s后,I3-浓度下降.导致下降的直接原因有(双选)
A.c(H+)减小 B.c(I-)减小 C.I2(g)不断生成 D.c(Fe3+)增加
(4)据图2,计算3-18s内第2组实验中生成I3-的平均反应速率(写出计算过程,结果保留两位有效数字).
查看习题详情和答案>>
(1)O3将I-氧化成I2的过程由3步反应组成:
①I-(aq)+O3(g)=IO-(aq)+O2(g)△H1
②IO-(aq)+H+(aq)?HOI(aq)△H2
③HOI(aq)+I-(aq)+H+(aq)?I2(aq)+H2O(l)△H3
总反应的化学方程式为
2I-+O3+2H+ I2+O2+H2O
I2+O2+H2O
 I2+O2+H2O
I2+O2+H2O2I-+O3+2H+ I2+O2+H2O
I2+O2+H2O
,其反应△H= I2+O2+H2O
I2+O2+H2O△H1+△H2+△H3
△H1+△H2+△H3
(2)在溶液中存在化学平衡:I2(aq)+I-(aq)?I3-(aq),其平衡常数表达式为


(3)为探究Fe2+对O3氧化I-反应的影响(反应体系如图1),某研究小组测定两组实验中I3-浓度和体系pH,结果见图2和下表.

| 编号 | 反应物 | 反应前pH | 反应后pH |
| 第1组 | O3+I- | 5.2 | 11.0 |
| 第2组 | O3+I-+Fe2- | 5.2 | 4.1 |
由2I-+O3+2H+ I2+O2+H2O可知消耗酸,所以pH升高
I2+O2+H2O可知消耗酸,所以pH升高
 I2+O2+H2O可知消耗酸,所以pH升高
I2+O2+H2O可知消耗酸,所以pH升高由2I-+O3+2H+ I2+O2+H2O可知消耗酸,所以pH升高
I2+O2+H2O可知消耗酸,所以pH升高
. I2+O2+H2O可知消耗酸,所以pH升高
I2+O2+H2O可知消耗酸,所以pH升高②图1中的A为
Fe2+
Fe2+
,由Fe3+生成A的过程能显著提高Ⅰ-的转化率,原因是O3可以将Fe2+氧化为Fe3+:O3+2Fe2++2H+=2Fe3++O2+H2O,Fe3+氧化I-:2Fe3++2I-=I2+2Fe2+,即A是亚铁离子,I-消耗量增大,转化率增大.
O3可以将Fe2+氧化为Fe3+:O3+2Fe2++2H+=2Fe3++O2+H2O,Fe3+氧化I-:2Fe3++2I-=I2+2Fe2+,即A是亚铁离子,I-消耗量增大,转化率增大.
.③第2组实验进行18s后,I3-浓度下降.导致下降的直接原因有(双选)
BC
BC
.A.c(H+)减小 B.c(I-)减小 C.I2(g)不断生成 D.c(Fe3+)增加
(4)据图2,计算3-18s内第2组实验中生成I3-的平均反应速率(写出计算过程,结果保留两位有效数字).