摘要:21. 3 胶体的方法是: 取一个小烧杯.加入25mL蒸馏水.将烧杯的蒸馏水加热至 .向 中逐滴加入1~2mLFeCl3溶液.继续 至溶液呈红褐色.停止加热.即得到Fe(OH)3 胶体. : KMnO4+KCl+H2SO4=K2SO4+MnSO4+Cl2↑+H2O ①此反应的氧化剂是 .氧化产物是 .被氧化的元素 . ②上述反应中若标准状况下产生11.2L气体物质.则转移电子的数目为 . ③上述反应中氧化剂与氧化产物的物质的量比为 .
网址:http://m.1010jiajiao.com/timu3_id_408596[举报]
在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的过程简述如下,请回答下列问题: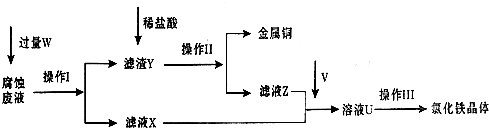
(1)请写出FeCl3溶液与铜反应的离子方程式:
(2)操作Ⅱ之前最好加入适量稀盐酸,某同学用10mol?L-1 的浓盐酸配制250mL 1mol?L-1 的稀盐酸,并进行有关实验.
①需要量取浓盐酸
②配制该稀盐酸时除量筒、烧杯、玻璃棒外,还必须用到的仪器有
③用已知浓度的氢氧化钠溶液滴定稀盐酸,滴定过程中眼睛应注视
(3)操作Ⅲ前需要通入气体V,请写出实验室制取气体V的化学方程式:
(4)操作Ⅲ应在HCl气流氛围中进行,其原因是
(5)若通入的V的量不足,则最后制得的氯化铁晶体不纯净,这是因为溶液U中含有杂质
供选择的试剂:酸性KMnO4溶液、KSCN溶液、氯水.
(6)若向氯化铁溶液中加入一定量石灰水,调节溶液pH,可得红褐色沉淀.该过程中调节溶液的pH为5,则金属离子浓度为
查看习题详情和答案>>

(1)请写出FeCl3溶液与铜反应的离子方程式:
2Fe3++Cu═2Fe2++Cu2+
2Fe3++Cu═2Fe2++Cu2+
;操作Ⅰ加入的试剂W是铁粉或Fe
铁粉或Fe
.(2)操作Ⅱ之前最好加入适量稀盐酸,某同学用10mol?L-1 的浓盐酸配制250mL 1mol?L-1 的稀盐酸,并进行有关实验.
①需要量取浓盐酸
25mL
25mL
mL.②配制该稀盐酸时除量筒、烧杯、玻璃棒外,还必须用到的仪器有
250mL容量瓶
250mL容量瓶
、胶头滴管
胶头滴管
.③用已知浓度的氢氧化钠溶液滴定稀盐酸,滴定过程中眼睛应注视
锥形瓶内溶液颜色的变化
锥形瓶内溶液颜色的变化
,实验时未用标准液润洗滴定管,测得锥形瓶中待测液的浓度大于
大于
实际浓度.(填“>”、“<”或“=”).(3)操作Ⅲ前需要通入气体V,请写出实验室制取气体V的化学方程式:
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
| ||
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
,该反应中
| ||
MnO2
MnO2
是氧化剂.(4)操作Ⅲ应在HCl气流氛围中进行,其原因是
抑制Fe3+(或FeCI3)的水解
抑制Fe3+(或FeCI3)的水解
.(5)若通入的V的量不足,则最后制得的氯化铁晶体不纯净,这是因为溶液U中含有杂质
FeCl2或Fe2+
FeCl2或Fe2+
.请设计合理的实验,验证溶液U中的成分,并判断通入的V的量是否不足取少量溶液U,加入几滴KSCN溶液,溶液显红色,则表明溶液U中有Fe3+(FeCl3);另取少量溶液U,加入几滴酸性KMnO4溶液,若KMnO4溶液退色,则表明溶液U中有Fe2+(或FeCl2),说明通入的V的量不足够若KMnO4溶液不退色,则说明通入的V的量充足
取少量溶液U,加入几滴KSCN溶液,溶液显红色,则表明溶液U中有Fe3+(FeCl3);另取少量溶液U,加入几滴酸性KMnO4溶液,若KMnO4溶液退色,则表明溶液U中有Fe2+(或FeCl2),说明通入的V的量不足够若KMnO4溶液不退色,则说明通入的V的量充足
(简要说明实验步骤、现象和结论).供选择的试剂:酸性KMnO4溶液、KSCN溶液、氯水.
(6)若向氯化铁溶液中加入一定量石灰水,调节溶液pH,可得红褐色沉淀.该过程中调节溶液的pH为5,则金属离子浓度为
4.0×10-11mol?L-1
4.0×10-11mol?L-1
.(己知:Ksp[Fe(OH)3]=4.0×10-38)中学常见的某反应的化学方程式为A+B-→C+D+H2O(未配平,反应条件略去).请回答下列有关问题:
(1)若A是铁,B是稀硝酸(过量),且A可溶于C溶液中.则A与B反应的离子方程式为
(2)若C、D均为气体,且都能使澄清石灰水变浑浊,则上述反应的化学方程式为
(3)若该反应是实验室制取C气体的反应.已知C是无色刺激性气味的气体,其水溶液呈弱碱性,C能生催化氧化反应.写出该反应的化学方程式
(4)若D为氯碱工业的主要原料,C是造成温室效应的主要气体之一,则上述反应的化学方程式
查看习题详情和答案>>
(1)若A是铁,B是稀硝酸(过量),且A可溶于C溶液中.则A与B反应的离子方程式为
Fe+4H++NO3-═Fe3++NO↑+2H2O
Fe+4H++NO3-═Fe3++NO↑+2H2O
.(2)若C、D均为气体,且都能使澄清石灰水变浑浊,则上述反应的化学方程式为
C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O,
| ||
C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O,
.
| ||
(3)若该反应是实验室制取C气体的反应.已知C是无色刺激性气味的气体,其水溶液呈弱碱性,C能生催化氧化反应.写出该反应的化学方程式
2NH4Cl+Ca(OH)2
2CaCl+2NH3↑+2H2O,
| ||
2NH4Cl+Ca(OH)2
2CaCl+2NH3↑+2H2O,
.
| ||
(4)若D为氯碱工业的主要原料,C是造成温室效应的主要气体之一,则上述反应的化学方程式
Na2CO3+2HCl═2NaCl+H2O+CO2↑或NaHCO3+HCl═NaCl+H2O+CO2↑
Na2CO3+2HCl═2NaCl+H2O+CO2↑或NaHCO3+HCl═NaCl+H2O+CO2↑
.下图中,A、D为气体非金属单质,N、P是金属单质;M为红褐色沉淀;B、E为有刺激性气味的气体;通常状况下,Z为液体;C是由三咱短周期非金属元素组成的离子化合物;I、L为白色沉淀.反应②、⑥均可用于实验室制取某种常见气体;工业上以D为原料生产B(图中部分反应物和生成物没有列出).
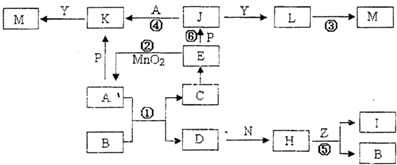
请按要求回答:
(1)写出D的结构式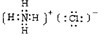
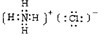 ;H的电子式
;H的电子式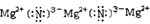
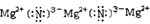 .
.
(2)上述①--⑥反应中属于氧化还原反应的有
用于除去K溶液中含有的少量J(填写序号).
(3)反应②的离子方程式为了
实验室制B的化学方程式为
(4)生活中K可用作净水剂,用离子方程式表示其原理
(5)写出A、M和氢氧化钾在一定条件下反应生成K2PO4(P为题中P物质的元素符号,答题时用所对应的元素符号表示)
查看习题详情和答案>>

请按要求回答:
(1)写出D的结构式
N≡N
N≡N
,C的电子式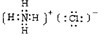
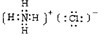
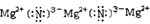
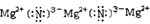
(2)上述①--⑥反应中属于氧化还原反应的有
①②③④⑥
①②③④⑥
(填写序号),其中反应④
④
可用于除去K溶液中含有的少量J(填写序号).
(3)反应②的离子方程式为了
4H++MnO2
Cl2↑+Mn2++2H2O
| ||
4H++MnO2
Cl2↑+Mn2++2H2O
.
| ||
实验室制B的化学方程式为
Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O
| ||
Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O
.
| ||
(4)生活中K可用作净水剂,用离子方程式表示其原理
Fe3++3H2O
Fe(OH)3(胶体)+3H+
| ||
Fe3++3H2O
Fe(OH)3(胶体)+3H+
.
| ||
(5)写出A、M和氢氧化钾在一定条件下反应生成K2PO4(P为题中P物质的元素符号,答题时用所对应的元素符号表示)
3Cl2+2Fe(OH)3+10KOH
2K2FeO4+6KCl
| ||
3Cl2+2Fe(OH)3+10KOH
2K2FeO4+6KCl
.
| ||
 I、下表是实验室制备气体的有关内容:
I、下表是实验室制备气体的有关内容:| 编号 | 实验内容 | 实验原理 | 发生装置 |
| ① | 制氧气 | H2O2→O2 | |
| ② | 制氨气 | NH4Cl→NH3 | |
| ③ | 制氯气 | HCl→Cl2 |
Cl2
Cl2
(填气体的化学式,下同);从反应中有无电子转移的角度看,明显不同于其他气体的是NH3
NH3
,写出实验室制取该气体的化学方程式Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O
| ||
Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O
.
| ||
(2)根据表中所列实验原理,从下列装置中选择合适的发生装置,将其编号填入上表的空格中.
(3)若用上述制备O2的装置制备NH3,则选择的试剂为
浓氨水和氢氧化钠(或生石灰或碱石灰)
浓氨水和氢氧化钠(或生石灰或碱石灰)
.已知:NH3?H2O的电离方程式为:NH3?H2O?NH+4+OH-,试写出NH3溶于水后,形成的NH3?H2O的合理结构


(4)制备Cl2需用8mol?L-1的盐酸100mL,现用12mol?L-1的盐酸来配制.
①需要12mol?L-1的盐酸的体积为
66.7
66.7
mL(精确到0.1mL)②在容量瓶的使用方法中,下列操作不正确的是
BC
BC
(填写标号).A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时用量筒量取浓盐酸后用玻璃棒引流入容量瓶中,缓慢加入蒸馏水到接近标线1cm~2cm处,用胶头滴管滴加蒸馏水直到凹液面的最低处和标线相平
D.定容后盖好瓶塞,用食指顶住,用另一只手手指托住瓶底,把容量瓶倒转和摇动多次
II、(1)常温下,已知0.1mol?L-1一元酸HA溶液中c(OH-)/c(H+)=1×10-8.
写出该酸HA与NaOH溶液反应的离子方程式式:
HA+OH-═A-+H2O
HA+OH-═A-+H2O
;(2)t℃时,有pH=2的稀硫酸和pH=11的NaOH溶液等体积混合后溶液呈中性,
则该温度下(t℃),将100mL 0.1mol?L-1的稀H2SO4溶液与100mL 0.4mol?L-1的NaOH溶液混合后(溶液体积变化忽略不计),溶液的pH=
12
12
. 某化学兴趣小组欲制取氨气和氯化氢气体并完成喷泉实验(图中夹持装置均已略去).
某化学兴趣小组欲制取氨气和氯化氢气体并完成喷泉实验(图中夹持装置均已略去).(1)写出实验室制取氨气的化学方程式:
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+H2O.
| ||
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+H2O.
.
| ||
(2)(每空1分)若实验室只有浓硫酸、浓盐酸、浓氨水、氢氧化钠固体、氯化铵固体、氧化钙、无水氯化钙、石蕊试液和如图1所示气体发生装置,你认为他们能制得所需的气体吗?把你的判断填入下表:
| 你的判断 | NH2 | HCl |  |
| 能够制的 | a中药品: 浓氨水 浓氨水 b中药品: 氢氧化钠固体或氧化钙 氢氧化钠固体或氧化钙 |
a中药品: 浓盐酸 浓盐酸 b中药品: 浓硫酸 浓硫酸 | |
| 不能制的 | 原因: 无 无 |
原因: 无 无 |
向上排空气
向上排空气
法,要得到干燥的氨气可选用碱石灰
碱石灰
作干燥剂.(3)如果用图2装置进行喷泉实验,上部烧瓶已装满干燥氨气,打开止水夹,挤出胶头滴管中的水引水上喷.该实验的原理是
氨气极易溶解于水,致使烧瓶内气体压强迅速减小
氨气极易溶解于水,致使烧瓶内气体压强迅速减小
.(4)如果用图3装置进行喷泉实验,上部烧瓶已装满干燥氨气气体,请说明引发喷泉的方法.
打开夹子,用手(或热毛巾)将烧瓶捂热,氨气受热膨胀,赶出玻璃导管内的空气,氨气与水接触,即发生喷泉.
打开夹子,用手(或热毛巾)将烧瓶捂热,氨气受热膨胀,赶出玻璃导管内的空气,氨气与水接触,即发生喷泉.
(5)若至喷泉实验停止时,图2中剩有烧瓶容积1/5的气体;图3烧瓶中剩有烧瓶容积1/4的气体;则图3烧瓶中盐酸的物质的量浓度为
| 1 |
| 22.4 |
| 1 |
| 22.4 |
等于
等于
(填“大于”、“小于”、“等于”)图3烧瓶中盐酸的物质的量浓度.(6)若使上述两种溶液混合后,溶液中铵离子和氯离子浓度相等,应如何操作:
向混合溶液中滴加氨水至溶液PH=7
向混合溶液中滴加氨水至溶液PH=7
.