摘要:14.某化学研究性学习小组拟采用粗氧化铜(含少量氧化亚铁及不溶于酸的杂质)制取无水氯化铜并测定样品中氧化铜的质量分数.其实验流程如图所示: 实验过程中的pH调节为: 物质 开始沉淀时的pH 完全测定时的pH Fe(OH)3 2.7 3.7 Fe(OH)2 7.6 9.6 Cu(OH)2 5.2 6.4 请回答以下问题: (1)步骤①.③过滤操作中.除用到仪器:铁架台.漏斗.烧杯除外.还需要使用的仪器用品有 . (2)步骤①中发生的离子反应方程式为 .(3)步骤②溶液Ⅰ中加入试剂X是 .其目的是 . a.氢氧化钠 b.氯水 c.碱式碳酸铜 d.氧化铜 (4)步骤③中将溶液pH调节到的范围是 [选填问题(3)所给试剂的编号].选择这种试剂的原因是 . (5)步骤⑤要得到无水氯化铜.需要在干燥的HCl气流中加热CuCl2·xH2O.其原因是 . (6)经检测.CuCl2·xH2O中含水28.6%.则CuCl2·xH2O中x的值为 . (7)若步骤④中80%的氯化铜转入晶体.其余各步转化都是完全的.请根据流程图中表示的质量数据.写出样品中氧化铜质量分数的计算式.
网址:http://m.1010jiajiao.com/timu3_id_407684[举报]
某化学研究性学习小组拟采用粗氧化铜(含少量氧化亚铁及不溶于酸的杂质)制取无水氯化铜并测定样品中氧化铜的质量分数,其实验流程如图所示:

实验过程中的pH调节为:
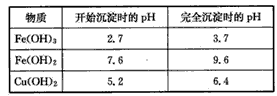
请回答以下问题:
(1)步骤①、③过滤操作中,除用到仪器:铁架台(带铁圈)、漏斗、烧杯外,还需要使用的仪器用品有________。
(2)步骤①中发生的离子反应方程式为________、____。
(3)步骤②溶液I中加入试剂X可以是____(填下列试剂的编号)。
A.氢氧化钠
B.氯水
C.碱式碳酸铜
D.氧化铜
(4)步骤③中将溶液pH调节到的范围是____。
(5)步骤⑤要得到无水氯化铜,需要在干燥的HCl气流中加热CuCl2·xH2O,其原因是____ 。
(6)经检测,CuCl2·xH2O中含水28. 6%,则CuCl2·xH2O中x的值为____。
(7)若步骤④中80%的氯化铜转入晶体,其余各步转化都是完全的,请根据流程图中表示的质量数据,写出 样品中氧化铜质量分数的计算式。
查看习题详情和答案>>
(1)步骤①、③过滤操作中,除用到仪器:铁架台(带铁圈)、漏斗、烧杯外,还需要使用的仪器用品有________。
(2)步骤①中发生的离子反应方程式为________、____。
(3)步骤②溶液I中加入试剂X可以是____(填下列试剂的编号)。
A.氢氧化钠
B.氯水
C.碱式碳酸铜
D.氧化铜
(4)步骤③中将溶液pH调节到的范围是____。
(5)步骤⑤要得到无水氯化铜,需要在干燥的HCl气流中加热CuCl2·xH2O,其原因是____ 。
(6)经检测,CuCl2·xH2O中含水28. 6%,则CuCl2·xH2O中x的值为____。
(7)若步骤④中80%的氯化铜转入晶体,其余各步转化都是完全的,请根据流程图中表示的质量数据,写出 样品中氧化铜质量分数的计算式。