摘要:8.下列表示中正确的是 A.熔点:Na>Mg>Al,半径:Si<P<S B.还原性:Be<Mg<Ca<Ba,氧化性:O>S>Se>Te C.稳定性:HF>HCl>HBr>HI,沸点:HF>HCl>HBr>HI D.酸性:HClO4>HBrO4>HIO4,碱性:NaOH>KOH>RbOH 9.某校研究性学习小组利用铁生锈原理设计了一个可给收音机供电的装置.在此装置中.下列说法正确的是 A.0.1mol Fe完全反应.转移电子0.3mol B.铁作阴极 C.正极反应式为:O2+2H2O+4e-=4OH- D.溶液中的Cl-移向正极 1,3,5 10.设NA表示阿伏加德罗常数的值.下列说法正确的是 A.100mL 0.1mol/L NaCl溶液中含0.01NA个 Na+离子 B.标准状况下22.4L SO3含有的分子数为NA C.20g重水(H2O)含有的分子数为8NA D.1mol Fe完全转化成Fe3胶体后.Fe(OH)3胶体微粒数为NA个
网址:http://m.1010jiajiao.com/timu3_id_407380[举报]
(2011?松江区模拟)用NA表示阿伏加德罗常数,下列说法中正确的是:( )
①18gD2O含有的电子数为10NA ②同温、同压下,相同体积的氟气和氩气所含的原子数相等 ③标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为NA ④在标准状况下,22.4LSO3的物质的量为1mol ⑤4℃时5.4mL的水所含的原子总数为0.9NA ⑥0.1molOH-含NA个电子 ⑦1molNa2O2与水完全反应时转移电子数为2NA.
①18gD2O含有的电子数为10NA ②同温、同压下,相同体积的氟气和氩气所含的原子数相等 ③标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为NA ④在标准状况下,22.4LSO3的物质的量为1mol ⑤4℃时5.4mL的水所含的原子总数为0.9NA ⑥0.1molOH-含NA个电子 ⑦1molNa2O2与水完全反应时转移电子数为2NA.
查看习题详情和答案>>
用NA表示阿伏加德罗常数,下列说法中正确的是:( )
①18gD2O含有的电子数为10NA ②同温、同压下,相同体积的氟气和氩气所含的原子数相等 ③标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为NA ④在标准状况下,22.4LSO3的物质的量为1mol ⑤4℃时5.4mL的水所含的原子总数为0.9NA ⑥0.1molOH-含NA个电子 ⑦1molNa2O2与水完全反应时转移电子数为2NA.
查看习题详情和答案>>
①18gD2O含有的电子数为10NA ②同温、同压下,相同体积的氟气和氩气所含的原子数相等 ③标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为NA ④在标准状况下,22.4LSO3的物质的量为1mol ⑤4℃时5.4mL的水所含的原子总数为0.9NA ⑥0.1molOH-含NA个电子 ⑦1molNa2O2与水完全反应时转移电子数为2NA.
| A.③⑤⑥⑦ | B.③⑤⑥ | C.①②④⑦ | D.③④⑤⑥ |
A、B、C均为常见的物质,且有如下转化关系:

(1)若M是第IVA族某元素的最高价氧化物,且M为气体,组成A的阴阳离子均含有10个电子.
①请用离子方程式表示C溶液呈现酸碱性的原因:______.
②用石墨电极电解B的饱和溶液时,观察到的现象是______,
阳极反应式为______,电解一段时间后,溶液的pH______(填“增大”、“减小”或“不变”).
(2)若A、B、C均为含硫元素的物质,则A分子中的化学键类型是______.
①若C在一定条件下可发生如下的反应:2SO2+O2 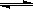 2SO3△H<0,下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是______.
2SO3△H<0,下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是______.
A t2时加入了催化剂 B t3时降低了温度
C t5时增大了压强 D t4~t5时间内反应物的转化率最低
②一定温度下的密闭容器内,充入4mol SO2、2mol O2 发生反应2SO2+O2 2SO3达到平衡后,SO3的体积分数为 a%,SO2的转化率为m.
2SO3达到平衡后,SO3的体积分数为 a%,SO2的转化率为m.
等温等容时再充入2mol SO2、1mol O2,达到平衡时若SO3的体积分数为b%,SO2的转化率为n,则a______b,m______n(填“>”、“=”或“<”,下同).若改为等温等压,则a______b,m______n.
查看习题详情和答案>>
|
用 NA表示阿伏加德罗常数的值,下列说法中正确的是① 2 L 1 mol/L的HCl溶液中,含有的HCl分子数目为2NA② 14 g乙烯和丙烯的混合物中,含有共用电子对数目为3NA③标况下, 22.4 L NO2与水反应,转移的电子数为NA④在 1 L 0.1 mol/L-1碳酸钠溶液中,阳离子总数大于0.2NA⑤ 6 g金刚石中,含有的共价键数为NA⑥25℃时,pH=14的Ba(OH)2溶液1 L,Ba2+数为NA ⑦一定条件下,1 mol H2和1 mol I2反应达到平衡后,密闭容器内分子总数等于2NA | |
| [ ] | |
A. |
①②③⑤ |
B. |
③④⑥⑦ |
C. |
②④⑤⑦ |
D. |
④⑤⑥⑦ |
|
用NA表示阿伏加德罗常数,下列说法中正确的是 ①18 g D2O含有的电子数为10NA ②同温、同压下,相同体积的氟气和氩气所含的原子数相等 ③标准状况下,11.2 L以任意比例混合的氮气和氧气所含的原子数为NA ④在标准状况下,22.4 L SO3的物质的量为1 mol ⑤4℃时5.4 mL的水所含的原子总数为0.9NA ⑥0.1 mol OH-含0.1NA个电子 ⑦1 mol Na2O2与水完全反应时转移电子数为2NA | |
| [ ] | |
A. |
③⑤⑥⑦ |
B. |
③⑤ |
C. |
①②④⑦ |
D. |
③④⑤⑥ |