摘要:26.氯气是一种重要的化工原料.在生产和生活中应用十分广泛. 已知:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O .所以在实验室可用高锰酸钾固体和浓盐酸制氯气. (1)请为该实验选择合适的发生装置 . (2)在2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O反应中.氧化剂是 . (3)当集气瓶中收集满氯气时.可以观察到气体呈 色. (4)工业上常用电解饱和食盐水制取氯气.试写出该反应的化学方程式: . (5)写出仪器①的名称 .
网址:http://m.1010jiajiao.com/timu3_id_40462[举报]
 氯气是一种重要的化工原料,在生产和生活中应用十分广泛.
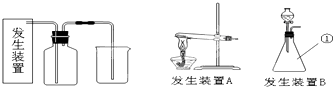
氯气是一种重要的化工原料,在生产和生活中应用十分广泛.已知:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O,在实验室可用二氧化锰固体或高锰酸钾固体和浓盐酸反应制取氯气.可供选用的发生装置如图.
(1)若用高锰酸钾固体和浓盐酸反应制取氯气,发生装置是
B
B
.(选填A或B或C)(2)写出用二氧化锰固体和浓盐酸反应制取氯气的化学方程式:
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
| ||
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
.
| ||
(3)实验室收集氯气的方法是
向上排空气集气法(或排饱和食盐水法)
向上排空气集气法(或排饱和食盐水法)
.(4)常用NaOH溶液吸收氯气防止污染.写出该反应的离子方程式
Cl2+2OH-=Cl-+ClO-+H2O
Cl2+2OH-=Cl-+ClO-+H2O
.氯气是一种重要的化工原料,在生产和生活中应用十分广泛.在实验室可用二氧化锰固体和浓盐酸制氯气.
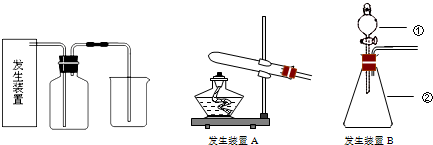
(1)请为该实验选择合适的发生装置
(2)当集气瓶中收集满氯气时,可以观察到气体呈
(3)工业上常用电解饱和食盐水制取氯气,试写出该反应的化学方程式:
查看习题详情和答案>>
(1)请为该实验选择合适的发生装置
B
B
(填A或B),写出仪器①的名称圆底烧瓶
圆底烧瓶
(2)当集气瓶中收集满氯气时,可以观察到气体呈
黄绿色
黄绿色
色.尾气通常用氢氧化钠溶液
氢氧化钠溶液
吸收.(3)工业上常用电解饱和食盐水制取氯气,试写出该反应的化学方程式:
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
| ||
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
.
| ||

氯气是一种重要的化工原料,在生产和生活中应用十分广泛.已知:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,所以在实验室可用高锰酸钾固体和浓盐酸制氯气.
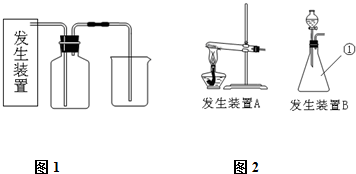
(1)请为该实验选择合适的发生装置 (填A或B).
(2)处理尾气时,发生反应的化学方程式: .
(3)用双线桥法标出2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O反应中电子转移的方向和数目.
(4)在该反应中,氧化剂是 ,氧化产物是 .
(5)若生成标准状况下11.2L 氯气,则转移电子 mol,被氧化的HCl为 mol.
查看习题详情和答案>>

(1)请为该实验选择合适的发生装置
(2)处理尾气时,发生反应的化学方程式:
(3)用双线桥法标出2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O反应中电子转移的方向和数目.
(4)在该反应中,氧化剂是
(5)若生成标准状况下11.2L 氯气,则转移电子