网址:http://m.1010jiajiao.com/timu3_id_40372[举报]
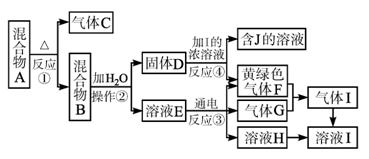
图1-5-22
(1)在实验室中,收集气体C可选择如图图1-5-23甲装置中的_______ (填选项字母)。

图甲 图乙
图1-5-23
(2)操作②的名称是_______,在操作②中所使用的玻璃仪器的名称是_______。在得到固体D时必须进行洗涤、干燥等操作,洗涤固体D的操作方法是____________________________。
(3)写出下列反应的化学方程式或离子方程式:
反应①______________;反应③______________;反应④______________。
(4)在实验室中,要获得干燥纯净的黄绿色气体F,可以将它通过如上面图乙所示的装置,其中瓶Ⅰ中盛放的是_______,瓶Ⅱ中盛放的是_______。
(5)实验中多余的气体F必须吸收,以免污染空气。图1-5-24是实验室用NaOH吸收气体F的装置,为防止产生倒吸现象,合理的装置是_______ (填序号)。
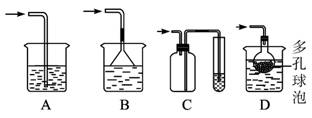
图1-5-24
查看习题详情和答案>> 实验室用浓硫酸与铜的反应制取少量NaHSO3,实验装置如图所示:
实验室用浓硫酸与铜的反应制取少量NaHSO3,实验装置如图所示:请回答:
(1)实验中取一定量Cu片和一定量浓H2SO4放在圆底烧瓶中共热,至反应结束后,发现烧瓶中还有少量Cu剩余,有人认为还有一定量的H2SO4剩余,原因是
(2)向反应后的溶液中加入足量的CuO,使剩余的H2SO4全部转化为CuSO4,过滤后将滤液加热浓缩,冷却结晶制得硫酸铜晶体(CuSO4?XH2O)某小组同学采用加热法测定该晶体里结晶水X的值;
①在他们的实验操作中至少称量
②下面是其中一次实验的数据
| 坩埚质量 | 坩埚与晶体总质量 | 加热后坩埚与固体总质量 |
| 11.7g | 22.7g | 18.6g |
(3)装置乙的作用是:
(4)下列说法正确的是:
a.甲装置使用的玻璃仪器有:酒精灯、玻璃管、长颈漏斗、圆底烧瓶
b.KMnO4溶液用于尾气处理
c.当把品红溶液滴入到锥形瓶中,若品红不褪色,说明无NaHSO3产生
d.当把品红溶液滴入到锥形瓶中,若品红褪色,说明NaOH已完全转化为NaHSO3
e.若把品红溶液换成酸性高锰酸钾溶液,并滴入到锥形瓶中,不显紫红色,说明NaOH已完全转化为NaHSO3
f.此装置换上其它药品后,不能制取和收集少量纯净的氯气.
(化学实验)饱和氯水与石灰石的反应是制取较浓HClO溶液的方法之一.2005年的《化学教育》报道了如下实验研究:
实验一、定性研究:
①在试管中加入过量的块状碳酸钙,再加入约20 mL饱和氯水,充分反应,有少量气泡产生,溶液浅黄绿色褪去;
②过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强;
③为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体;
将第三份加热,看到溶液变浑浊且有大量无色气体产生.经检测,上述实验中产生的无色气体均为CO2.请回答:
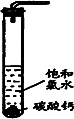
(1)反应后所得的溶液漂白性增强的原因是____________.
(2)依据上述实验可推知:②的滤液中的溶质除CaCl2、HClO外,还含有__________.
实验二、定量研究:
在圆底烧瓶底部,有一用塑料网包住的过量块状碳酸钙和150 mL饱和氯水,按如图所示装置实验,待不再产生气泡后,将塑料网中剩余的石灰石提出液面,密封后再加热、煮沸烧瓶中的液体,直到量筒中的气体不再增加(不考虑HClO的分解).请回答:
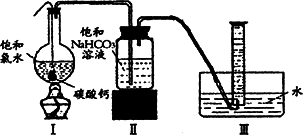
(3)为减少用装置Ⅲ收集气体过程中CO2因溶解而造成的损失,且水槽中仍然为水,请你对装置Ⅲ进行改进,最简单的方法是____________.
(4)用改进后的装置进行上述实验,测得塑料网内的碳酸钙质量减少Ag,总共收集到标准状况下的CO2气体BL,发现B/22.4 moL明显小于A/100 moL.若不考虑实验操作和CO2的溶解等因素造成的误差,从化学反应原理来看,导致这一大小关系的原因是____________.
(5)实验后发现,装置Ⅱ中的液体增多了,其原因是________.