摘要:4.35.2gCu和CuO的混合物.加入到175mL某浓度的硝酸中.混合物恰好完全溶 解.并得到8.96L标准状况下的气体.将其通过足量水后.变为4.48L.试求算(假定NO2不转化成N2O4), (1)被还原硝酸的物质的量 . (2)混合物中Cu元素的质量分数 . (3)所用硝酸的物质的量浓度 .
网址:http://m.1010jiajiao.com/timu3_id_401653[举报]
(2012?四川)向27.2gCu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO和Cu(NO3)2.在所得溶液中加入1.0mol/L 的NaOH溶液1.0L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2g.下列有关说法不正确的是( )
查看习题详情和答案>>
 某化学小组拟采用如下装置(夹持和加热仪器已略去)来电解饱和食盐水,并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量,同时检验氯气的氧化性.
某化学小组拟采用如下装置(夹持和加热仪器已略去)来电解饱和食盐水,并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量,同时检验氯气的氧化性.(1)D装置中电解饱和食盐水的离子反应方程式为:
2Cl-+2H2O
2OH-+H2↑+Cl2↑
| ||
2Cl-+2H2O
2OH-+H2↑+Cl2↑
| ||
(2)为检验氯气的氧化性,则E装置的溶液可以是
ACD
ACD
.A.淀粉碘化钾溶液 B.酸性KMnO4溶液 C.FeCl2溶液 D.Na2S溶液
(3)F装置的目的是
吸收未反应的氯气
吸收未反应的氯气
.(4)为测定Cu的相对原子质量,某同学设计了如下的方案:
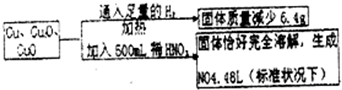
精确测量硬质玻璃管的质量为a g,放入CuO后,精确测量硬质玻璃管和CuO的总质量为b g,实验完毕后(通过足量的氢气),通过精确测量硬质玻璃管和Cu粉的总质量为c g,进而确定Cu的相对原子质量.
①对B装置中的氧化铜粉末加热前,需要进行的操作为
通入氢气排尽装置内空气
通入氢气排尽装置内空气
;②A装置中盛放的试剂为
浓硫酸
浓硫酸
;③根据测得结果进行计算,则Cu的相对原子质量为
| 16(c-a) |
| b-c |
| 16(c-a) |
| b-c |