网址:http://m.1010jiajiao.com/timu3_id_40114[举报]
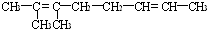 ,
,它与过量的酸性高锰酸钾溶液作用得到下列三种化合物:CH3COCH3,CH3COCH2CH2COOH,CH3COOH.若化合物B与A互为同分异构体,且A、B分别与酸性高锰酸钾溶液反应得到的产物相同,则化合物B的结构简式正确的是( )
高锰酸钾是锰的重要化合物和常用的氧化剂.以下是工业上用软锰矿(主要成分MnO2)制备高锰酸钾的一种工艺流程.
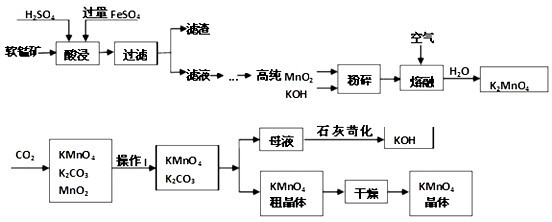
请回答:
(1)KMnO4稀溶液是一种常用的消毒剂.其消毒机理与______(填字母)相同.
a.NaClO溶液 b.乙醛 c.双氧水 d.75%的酒精
(2)操作Ⅰ的名称是______;硫酸亚铁在酸性条件下将MnO2还原为MnSO4,酸浸时发生主要反应的化学方程式为______
(3)上述流程中可以循环使用的物质有______和______(填化学式).若不考虑物质循环与制备过程中的损失,则1mol MnO2可制得______mol KMnO4.
(4)MnO2在酸性条件下具有强氧化性,可被还原为Mn2+.写出MnO2与浓盐酸制取氯气的化学方程式______
为验证MnO2具有强氧化性,下列方案可行的是______(填字母)
A.MnO2固体加入到FeCl3溶液中,再加KSCN溶液,观察溶液是否变红
B.MnO2固体加入到Na2SO3溶液中,再加BaCl2溶液,观察是否有白色沉淀生成
C.MnO2固体加入到FeSO4与KSCN的酸性混合液中,观察溶液是否变红
(5)酸性KMnO4与H2C2O4溶液反应,反应开始时溶液褪色较慢,反应一段时间后褪色会迅速加快,其原因是______.
查看习题详情和答案>>
Ⅰ.测定过氧化氢的含量
(1)取10.00mL密度为ρg/mL的过氧化氢溶液稀释至250mL,移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样.用高锰酸钾标准溶液滴定被测试样,写出滴定过程中发生反应的离子方程式:
(2)重复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为
Ⅱ.探究过氧化氢的性质
(1)H2O2与铜的有关探究实验:
①将铜丝置于用硫酸酸化的H2O2溶液中,铜被迅速氧化,溶液变蓝;同时产生大量气体,经检测该气体能使余烬木条复燃,反应的离子方程式为:
②将铜丝置于H2O2溶液中,没有气泡产生,加热溶液时,观察到铜丝表面产生大量气体,且气体能使余烬木条复燃,在该变化中铜丝所起的作用是
(2)将氯气用导管通入较浓的NaOH和H2O2的混和液中,在导管口与混和液的接触处有闪烁的红光出现,这是因为通气后混和液中产生的ClO-被H2O2还原,发生激烈反应,产生能量较高的氧分子,它立即转变为普通氧分子,将多余的能量以红光放出,ClO-与H2O2反应的离子方程式是
Ⅰ.过氧化氢(H2O2)的水溶液俗称双氧水,近年来倍受人们的青睐,被称为“绿色氧化剂”。
⑴写出H2O2的电子式_________________,其分子内存在______键和_______键。
⑵你认为H2O2被成为“绿色氧化剂”的主要原因是________________________________________。
⑶与H2O2分子具有相同电子数的双原子单质分子为(写化学式)______________,与H2O2分子具有相同电子数的三原子化合物分子为(写化学式)______________。
⑷某工业废水中含有一定量氯气,为了除去氯气,常加入H2O2作脱氯剂,写出该反应的化学方程式为___________________________________________,反应中H2O2作_____________剂。
⑸将双氧水加入用盐酸酸化的FeCl2溶液中,溶液由浅绿色变为棕黄色,写出该反应的离子方程式为___________________________________________,反应中H2O2作_____________剂。
⑹双氧水能使酸性高锰酸钾溶液褪色,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里:
MnO4-+ H2O2+ H+=== Mn2++ H2O+ 。
Ⅱ.某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2,已知该反应中H2O2只发生如下过程:H2O2→ O2
⑴该反应的化学方程式为_____________________________________________。
⑵如反应转移了0.3mol电子,则产生的气体在标准状况下体积为
过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质。

Ⅰ.测定过氧化氢的含量
(1)取10.00 mL密度为ρ g/mL的过氧化氢溶液稀释至250mL,移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。用高锰酸钾标准溶液滴定被测试样,写出滴定过程中发生反应的离子方程式: _____________________________________________________
(2)重复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为____________。
Ⅱ.探究过氧化氢的性质
(1)H2O2与铜的有关探究实验:将铜丝置于用硫酸酸化的H2O2溶液中,铜被迅速氧化,溶液变蓝;同时产生大量气体,经检测该气体能使余烬木条复燃,反应的离子方程式为:_________________________。
②将铜丝置于H2O2溶液中,没有气泡产生,加热溶液时,观察到铜丝表面产生大量气体,且气体能使余烬木条复燃,在该变化中铜丝所起的作用是__________,写出产生气体这一现象的反应的化学方程式__________________________。
(2)将氯气用导管通入较浓的NaOH和H2O2的混和液中,在导管口与混和液的接触处有闪烁的红光出现,这是因为通气后混和液中产生的ClO-被H2O2还原,发生激烈反应,产生能量较高的氧分子,它立即转变为普通氧分子,将多余的能量以红光放出,ClO-与H2O2反应的离子方程式是___________________________。
查看习题详情和答案>>