摘要:16.常温时.下列两种溶液等体积混合后.混合液中微粒的物质的量浓度关系正确的是 A.0.1mol·L-1的NaOH溶液与0.1mol·L-1的H2SO3溶液:c(H2SO3)>c(SO32-) B.0.1mol·L-1的NaOH溶液与0.1mol·L-1的醋酸溶液:c(Na+)<c(CH3COO-) C.pH=3的盐酸和pH=11的氨水:c(OH-)>c(H+) D.0.1mol·L-1的NH4Cl溶液和0.1mol·L-1的氨水:c(NH4+)<c(Cl-)
网址:http://m.1010jiajiao.com/timu3_id_400340[举报]
下列有关说法正确的是( )
查看习题详情和答案>>
| A.常温时,0.1mol/LHA溶液的pH>1,0.1mol/LBOH溶液中c(OH-)/c(H+)=1012,将这两种溶液等体积混合,混合后溶液中离子浓度的大小关系为:c(B+)>c(OH-)>c(H+)>c(A-) |
| B.用pH=3和pH=2的醋酸溶液中和含等量NaOH的溶液所消耗的醋酸溶液的体积分别为Va和Vb,则Va<10Vb |
| C.0.1mol?L-1的NH4Cl溶液与0.05mol?L-1的NaOH溶液等体积混合:c(Cl-)>c(Na+)>c(NH4+)>c(OH-)>c(H+) |
| D.浓度相等的(NH4)2SO4溶液、(NH4)2CO3溶液和NH4Cl溶液中c(NH4+):c( NH4Cl)<c[(NH4)2CO3]<c[(NH4)2SO4] |
下列叙述正确的是( )
A.将pH=12 Ba(OH)2与pH=14 NaOH溶液等体积混合后,混和液13<pH<14
B.常温时,0.1 mol?L-1HA溶液的pH>1,0.1 mol?L-1BOH溶液中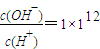 ,将这两种溶液等体积混合,混合后溶液中离子浓度的大小关系为:c(B+)>c(OH-)>c(H+)>c(A-)
,将这两种溶液等体积混合,混合后溶液中离子浓度的大小关系为:c(B+)>c(OH-)>c(H+)>c(A-)
C.过量SO2通入到Ba(NO3)2溶液中,正确的离子反应方程式为: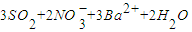 ═3BaSO4↓+2NO↑+4H+
═3BaSO4↓+2NO↑+4H+
D.相同条件下,pH=5的 ①NH4Cl溶液、②CH3COOH溶液、③稀盐酸溶液中由水电离出的c(H+):①>②>③
查看习题详情和答案>>
查看习题详情和答案>>
A.将pH=12 Ba(OH)2与pH=14 NaOH溶液等体积混合后,混和液13<pH<14
B.常温时,0.1 mol?L-1HA溶液的pH>1,0.1 mol?L-1BOH溶液中
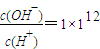 ,将这两种溶液等体积混合,混合后溶液中离子浓度的大小关系为:c(B+)>c(OH-)>c(H+)>c(A-)
,将这两种溶液等体积混合,混合后溶液中离子浓度的大小关系为:c(B+)>c(OH-)>c(H+)>c(A-)C.过量SO2通入到Ba(NO3)2溶液中,正确的离子反应方程式为:
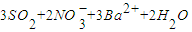 ═3BaSO4↓+2NO↑+4H+
═3BaSO4↓+2NO↑+4H+D.相同条件下,pH=5的 ①NH4Cl溶液、②CH3COOH溶液、③稀盐酸溶液中由水电离出的c(H+):①>②>③
查看习题详情和答案>>
(10分)(1)常温下,某水溶液M中存在的离子有:Na+、A2-、HA-、H+、OH-,存在的分子有H2O、H2A。根据题意回答下列问题:
①写出酸H2A的电离方程式__________________________。
②若溶液M由2 mol·L-1NaHA溶液与2mol·L-1NaOH溶液等体积混合而得,则溶液M的pH ____7 (填“>”、“<”或“=”);溶液M中各微粒的浓度关系正确的是 。
A.c(Na+)>c(A2-)>c(OH-)>c(H+)
B.c(HA-) +c(H2A) +c(H+)=c(OH-)
C.c(A2-)+c(HA-)+c(H2A)=1 mol·L-1
D. c(A2-)+c(HA-)+c(OH-)=c(Na+)+c(H+)
(2)室温时,氢氧化钙的溶度积KSP =4.7×10-6, 室温时将9 mL0.02 mol·L—1的氯化钙溶液与1 mL pH=13的氢氧化钠溶液混合后(溶液体积可直接加和),溶液中___ 沉淀析出(填“有”或“无”)。
(3) 某校课外活动小组为测定已部分脱水的生石膏的组成(xCaSO4·yH2O),做如下实验:将固体加热,经测量剩余固体质量随时间变化如图所示。
则x:y= 。t2~t3时间段固体的化学式为 。t5~t6时间段固体质量减轻的原因是产生了两种气体,其中一种能使品红溶液褪色。则该时间所发生反应的化学方程式为 。
查看习题详情和答案>>