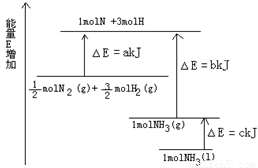
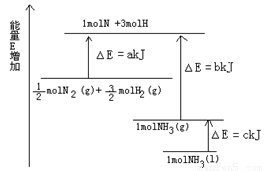
摘要:20.氨气是氮循环中的重要物质.在人类的生产和生活中有着广泛的应用.也是氮肥工业和硝酸工业的重要原料. 已知:合成氨反应是一个可逆反应.在298K时.该反应的化学平衡常数K=4.1x106mol-2·L2. 请回答: (1)右图是N2与H2反应过程中能量变化的示意图.则该反应的热化学方程式是--o (2)在温度不变.体积恒定为10L的密闭容器中充入10molN2.30molH2和10molNH3.开始反应时.反应速率的关系为v(正) v(逆)(填“< “= 或“> ).在该容器中.能说明该反应已达到化学平衡状态的依据是 . A.容器中压强不变 B.混合气体的密度不变 C.v正(N2)=2v逆(NH3) D. c(NH3):c(N2):c(H2)=2:1:3 E.混合气体的平均摩尔质量不变
网址:http://m.1010jiajiao.com/timu3_id_399882[举报]
(6分)氨气是氮循环中的重要物质,在人类的生产和生活中有着广泛的应用。
(1)上图是N2与H2反应过程中能量变化的示意图,则该反应生成液态氨的热化学方程式是______________________ 。
(2).若由N2和H2合成1molNH3时可放出46.2kJ/mol的热量。从手册上查出N≡N键的键能是948.9kJ/mol,H-H键的键能是436. 0kJ/mol,则N-H键的键能是________ kJ/mol。
查看习题详情和答案>>
(6分)氨气是氮循环中的重要物质,在人类的生产和生活中有着广泛的应用。
(1)如图是N2与H2反应过程中能量变化的示意图,则该反应生成液态氨的热化学方程式是______________________。
(2).若由N2和H2合成1molNH3时可放出46.2kJ/mol的热量。从手册上查出N≡N键的键能是948.9kJ/mol,H-H键的键能是436. 0kJ/mol,则N-H键的键能是________ kJ/mol。
查看习题详情和答案>>
(6分)氨气是氮循环中的重要物质,在人类的生产和生活中有着广泛的应用。
(1)如图是N2与H2反应过程中能量变化的示意图,则该反应生成液态氨的热化学方程式是______ ________________。
________________。
(2).若由N2和H2合成1molNH3时可放出46.2kJ/mol的热量。从手册上查出N≡N键的键能是948.9kJ/mol,H-H键的键能是436. 0kJ/mol,则N-H键的键能是________ kJ/mol。