摘要:30.赤铁矿是炼铁的主要原料之一.它的主要成分在一定条件下有下列反应: Fe2O3+CO 2FeO+CO2 在反应形成的固体混合物(Fe2O3.FeO)中.元素铁和氧的质量比用m表示. (1)根据上述反应.固体质量每减烃1.6g.将产生CO2 L. (2)上述反应形成的固体混和物中.m不可能是 . A.21:9 B.21:7.5 C.21:5 D.21:8 (3)Fe2O3被CO还原的百分率为50%.则m= .
网址:http://m.1010jiajiao.com/timu3_id_399801[举报]
(2013?朝阳区一模)工业上常以赤铁矿石(主要成分为Fe2O3)和焦炭为主要原料,在高温下炼铁.焦炭产生CO的反应是:
C+O2
CO2; C+CO2
2CO
(1)CO还原赤铁矿的化学方程式是
(2)下列说法正确的是
a.为使赤铁矿石充分燃烧,需将其粉碎
b.足量的空气能提高炼铁反应速率
c.与生铁相比较,纯铁转化为“铁水”的温度低
(3)生铁的用途很多,某电镀厂用生铁将废水中的Cr2O72-转化为Cr3+,流程图1:
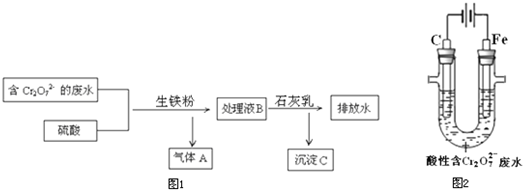
①气体A是
②在上述酸性溶液中,生铁比纯铁产生Fe2+的速率快,原因是
③将Cr3+转化为Cr(OH)3的离子方程式是
(4)电解法将一定浓度的酸性废水中的Cr2O72-转化为Cr3+,其原理示意图2:
①阳极附近溶液中Cr2O72-转化为Cr3+的离子方程式是
②一段时间后,试管底部出现沉淀.解释生成沉淀的原因:
查看习题详情和答案>>
C+O2
| ||
| ||
(1)CO还原赤铁矿的化学方程式是
Fe2O3+3CO
2Fe+3CO2
| ||
Fe2O3+3CO
2Fe+3CO2
| ||
(2)下列说法正确的是
ab
ab
a.为使赤铁矿石充分燃烧,需将其粉碎
b.足量的空气能提高炼铁反应速率
c.与生铁相比较,纯铁转化为“铁水”的温度低
(3)生铁的用途很多,某电镀厂用生铁将废水中的Cr2O72-转化为Cr3+,流程图1:

①气体A是
H2
H2
②在上述酸性溶液中,生铁比纯铁产生Fe2+的速率快,原因是
生铁中含有C,在硫酸溶液中形成无数微小原电池,加快反应速率
生铁中含有C,在硫酸溶液中形成无数微小原电池,加快反应速率
③将Cr3+转化为Cr(OH)3的离子方程式是
2Cr3++3Ca(OH)2═2Cr(OH)3↓+3Ca2+
2Cr3++3Ca(OH)2═2Cr(OH)3↓+3Ca2+
(4)电解法将一定浓度的酸性废水中的Cr2O72-转化为Cr3+,其原理示意图2:
①阳极附近溶液中Cr2O72-转化为Cr3+的离子方程式是
6Fe2++Cr2O72-+14H+═6Fe3++2Cr3++7H2O
6Fe2++Cr2O72-+14H+═6Fe3++2Cr3++7H2O
②一段时间后,试管底部出现沉淀.解释生成沉淀的原因:
随着电解进行,溶液中c(H+)逐渐减少,c(OH-)浓度增大,生成Fe(OH)3和Cr(OH)3沉淀
随着电解进行,溶液中c(H+)逐渐减少,c(OH-)浓度增大,生成Fe(OH)3和Cr(OH)3沉淀
.钢铁工业是国家工业的基础.请回答钢铁冶炼、腐蚀、防护过程中的有关问题.
(1)工业用热还原法炼铁,写出由CO还原赤铁矿(主要成分为Fe2O3)的化学方程式:
(2)铁是一种重要的催化剂,请写出铁在有机反应中做催化剂的化学方程式:
(3)生产中可用盐酸来除铁锈.现将一生锈的铁片放入盐酸中,当铁锈被除尽后,溶液中发生的化合反应的化学方程式
(4)下列哪个装置可防止铁棒被腐蚀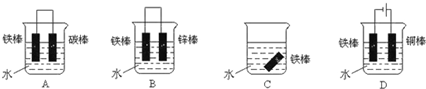
(5)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀.装置示意图如下:
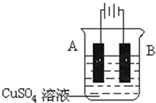
请回答:
①A电极对应的金属是
②若电镀前铁.铜两片金属质量相同,电镀完成后将它们取出洗净.烘干.称量,二者质量差为5.12g,则电镀时电路中通过的电子为
③镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因
查看习题详情和答案>>
(1)工业用热还原法炼铁,写出由CO还原赤铁矿(主要成分为Fe2O3)的化学方程式:
Fe2O3+3CO
2Fe+3CO2
| ||
Fe2O3+3CO
2Fe+3CO2
.
| ||
(2)铁是一种重要的催化剂,请写出铁在有机反应中做催化剂的化学方程式:
C6H6+Br2
C6H5Br+HBr
| Fe |
C6H6+Br2
C6H5Br+HBr
.| Fe |
(3)生产中可用盐酸来除铁锈.现将一生锈的铁片放入盐酸中,当铁锈被除尽后,溶液中发生的化合反应的化学方程式
2FeCl3+Fe═3FeCl2
2FeCl3+Fe═3FeCl2
.(4)下列哪个装置可防止铁棒被腐蚀
BD
BD
.
(5)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀.装置示意图如下:

请回答:
①A电极对应的金属是
铜
铜
(写元素名称),B电极的电极反应式是Cu2++2e-═Cu
Cu2++2e-═Cu
.②若电镀前铁.铜两片金属质量相同,电镀完成后将它们取出洗净.烘干.称量,二者质量差为5.12g,则电镀时电路中通过的电子为
0.08
0.08
mol.③镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因
铁比铜活泼,镀层破坏后,在潮湿环境中形成原电池,铁为负极,加速铁的腐蚀
铁比铜活泼,镀层破坏后,在潮湿环境中形成原电池,铁为负极,加速铁的腐蚀
.