摘要:将14.4g由NaCl和CaCl2组成的固体混合物.溶于45.6g的水中.向所得到的混合溶液中逐滴加入质量分数为21.2%的Na2CO3溶液.所加入Na2CO3溶液的质量与产生沉淀的质量关系如图: (1)中考资源网当CaCl2和Na2CO3恰好完全反应时.消耗21.2%的Na2CO3溶液的质量为 g, (2)中考资源网原混合溶液中CaCl2的质量为多少g? (3)中考资源网当混合溶液中的CaCl2和Na2CO3恰好完全反应后.过滤.所得溶液中溶质的质量分数为多少?
网址:http://m.1010jiajiao.com/timu3_id_3997916[举报]
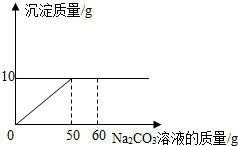 将14.4g由NaCl和CaCl2组成的固体混合物,溶于45.6g的水中,向所得到的混合溶液中逐滴加入质量分数为21.2%的Na2CO3溶液,所加入Na2CO3溶液的质量与产生沉淀的质量关系如图:
将14.4g由NaCl和CaCl2组成的固体混合物,溶于45.6g的水中,向所得到的混合溶液中逐滴加入质量分数为21.2%的Na2CO3溶液,所加入Na2CO3溶液的质量与产生沉淀的质量关系如图:(1)当CaCl2和Na2CO3恰好完全反应时,消耗21.2%的Na2CO3溶液的质量为
(2)原混合物中CaCl2的质量为
(3)当混合溶液中的CaCl2和Na2CO3恰好完全反应后,过滤,所得溶液中溶质的质量分数为多少? 查看习题详情和答案>>
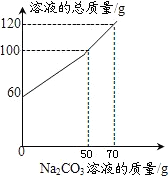 将14.4g由NaCl和CaCl2组成的固体混合物溶于水配成60g溶液,向所得到的混合溶液中逐滴加入一定质量分数的Na2CO3溶液,所加入Na2CO3溶液的质量与所得溶液的总质量关系如图:
将14.4g由NaCl和CaCl2组成的固体混合物溶于水配成60g溶液,向所得到的混合溶液中逐滴加入一定质量分数的Na2CO3溶液,所加入Na2CO3溶液的质量与所得溶液的总质量关系如图:(1)当恰好完全反应时,得到沉淀的质量为
(2)当恰好完全反应后,过滤,求所得滤液中溶质的质量分数为多少? 查看习题详情和答案>>
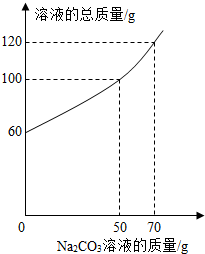 将14.4g由NaCl和CaCl2组成的固体混合物溶于水配成60g溶液,向所得到的混合溶液中逐滴加入一定质量分数的Na2CO3溶液,所加入Na2CO3溶液的质量与所得溶液的总质量关系如图:
将14.4g由NaCl和CaCl2组成的固体混合物溶于水配成60g溶液,向所得到的混合溶液中逐滴加入一定质量分数的Na2CO3溶液,所加入Na2CO3溶液的质量与所得溶液的总质量关系如图:(1)写出滴加过程中发生反应的化学方程式:
(2)当CaCl2和Na2CO3恰好完全反应时,消耗Na2CO3溶液的质量为
(3)当混合溶液中的CaCl2和Na2CO3恰好完全反应后,过滤,求所得溶液中溶质的质量分数为多少?(可能用到的相对分子质量:CaCl2-111;Na2CO3-106;NaCl-58.5) 查看习题详情和答案>>
 将14.4g由NaCl和CaCl2组成的固体混合物溶于水配成60g溶液,向所得到的混合溶液中逐滴加入一定质量分数的Na2CO3溶液,所加入Na2CO3溶液的质量与所得溶液的总质量关系如图:
将14.4g由NaCl和CaCl2组成的固体混合物溶于水配成60g溶液,向所得到的混合溶液中逐滴加入一定质量分数的Na2CO3溶液,所加入Na2CO3溶液的质量与所得溶液的总质量关系如图: 将14.4g由NaCl和CaCl2组成的固体混合物,溶于45.6g的水中,向所得到的混合溶液中逐滴加入质量分数为21.2%的Na2CO3溶液,所加入Na2CO3溶液的质量与产生沉淀的质量关系如图:
将14.4g由NaCl和CaCl2组成的固体混合物,溶于45.6g的水中,向所得到的混合溶液中逐滴加入质量分数为21.2%的Na2CO3溶液,所加入Na2CO3溶液的质量与产生沉淀的质量关系如图: