摘要: 某同学将一个表面生锈的铁钉(铁锈主要成分是Fe2O3)放入盐酸中.开始观察到铁锈逐渐 .反应的化学方程式为 ,然后观察到铁钉表面有 产生.反应的化学方程式为: .
网址:http://m.1010jiajiao.com/timu3_id_3993329[举报]
某化学兴趣小组对酸的性质进行了系列研究,下面是他们的研究过程,请你一起参与.
(1)探究盐酸的某些性质
该小组进行了如下实验:将一只表面生锈的铁钉放入盛有稀盐酸的烧杯中,发现不同阶段产生不同的现象,具体记录如下:
试解释:
①溶液从无色变成黄色是因为反应生成了
②写出产生气泡所发生反应的化学方程式
③反应停止的原因是
④上述实验说明,盐酸在工业上可以用来
(2)探究盐酸和氢氧化钙能否发生化学反应
小静向盛有氢氧化钙溶液的烧杯中滴加了稀盐酸后,没有观察到明显的现象.为了确定盐酸与氢氧化钙是否反应,小静从烧杯中取出少量反应后的溶液于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色.于是她得出“两种物质能发生化学反应,并且反应后的溶液呈中性”的结论.请回答:
①她得出的结论中有不完善的地方,因为酚酞试液只能在
②我们还可以从多个角度设计实验,探究上述烧杯中的溶液是否恰好完全中和.请你选择一种方法完成下面的表格:
查看习题详情和答案>>
(1)探究盐酸的某些性质
该小组进行了如下实验:将一只表面生锈的铁钉放入盛有稀盐酸的烧杯中,发现不同阶段产生不同的现象,具体记录如下:
| 反应阶段 | 1 | 2 | 3 | 4 | 5 |
| 现象 | 溶液颜色从无色变黄色 | 黄色逐渐加深并有少量气泡 | 气泡逐渐增多 | 气泡逐渐减少 | 反应停止 铁钉变亮 |
①溶液从无色变成黄色是因为反应生成了
FeCl3
FeCl3
(填化学式).②写出产生气泡所发生反应的化学方程式
Fe+2HCl=FeCl2+H2↑
Fe+2HCl=FeCl2+H2↑
.③反应停止的原因是
盐酸已反应完
盐酸已反应完
.④上述实验说明,盐酸在工业上可以用来
除锈
除锈
.(2)探究盐酸和氢氧化钙能否发生化学反应
小静向盛有氢氧化钙溶液的烧杯中滴加了稀盐酸后,没有观察到明显的现象.为了确定盐酸与氢氧化钙是否反应,小静从烧杯中取出少量反应后的溶液于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色.于是她得出“两种物质能发生化学反应,并且反应后的溶液呈中性”的结论.请回答:
①她得出的结论中有不完善的地方,因为酚酞试液只能在
碱
碱
性溶液中变色,无法确定溶液是否呈中性.②我们还可以从多个角度设计实验,探究上述烧杯中的溶液是否恰好完全中和.请你选择一种方法完成下面的表格:
| 实验方法 | 可能观察到的现象 | 结论 |
用玻璃棒蘸取反应后的溶液滴在pH试纸上,并与标准比色卡对比. 用玻璃棒蘸取反应后的溶液滴在pH试纸上,并与标准比色卡对比. |
pH试纸的颜色与标准比色卡上pH为7处的颜色一致(浅黄色) pH试纸的颜色与标准比色卡上pH为7处的颜色一致(浅黄色) |
恰好完全反应 恰好完全反应 |
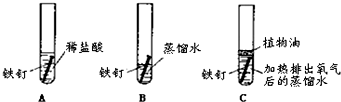 某化学兴趣小组的同学为探究铁生锈的条件,他们将等质量、相同规格的光亮的铁钉同时放入如图所示装置中进行实验.回答下列问题:
某化学兴趣小组的同学为探究铁生锈的条件,他们将等质量、相同规格的光亮的铁钉同时放入如图所示装置中进行实验.回答下列问题:(1)一段时间后,铁钉无变化的是
C
C
(填写字母,下同);(2)铁生锈的条件是
与水和氧气接触
与水和氧气接触
.(3)实验用蒸馏水的原因
蒸馏水中无氧气
蒸馏水中无氧气
(4)用植物油将水封住的原因
隔绝空气(氧气)
隔绝空气(氧气)
(5)要探究铁生锈的条件,上述实验还不够完善,还需要补充的一个实验是
将铁钉置于干燥空气中
将铁钉置于干燥空气中
.(5)请你提出防止钢铁锈蚀的两条合理措施①
涂油、刷漆
涂油、刷漆
进行表面防护处理,②改变金属内部结构(制成不锈钢)
改变金属内部结构(制成不锈钢)
.某化学兴趣小组的同学为探究铁生锈的条件,他们将等质量、相同规格的光亮的铁钉同时放入如图所示装置中进行实验.回答下列问题:

(1)一段时间后,铁钉无变化的是
(2)整个过程中铁钉表面没有铁锈出现,但质量发生变化的是
(3)同时结束实验后,将铁钉取出烘干、称重,其质量由大到小的顺序为
(4)要探究铁生锈的条件,上述实验还不够完善,还需要补充的一个实验是
(5)请你提出防止钢铁锈蚀的两条合理措施①
查看习题详情和答案>>

(1)一段时间后,铁钉无变化的是
C
C
(填写字母,下同);(2)整个过程中铁钉表面没有铁锈出现,但质量发生变化的是
A
A
;(3)同时结束实验后,将铁钉取出烘干、称重,其质量由大到小的顺序为
BCA
BCA
;(4)要探究铁生锈的条件,上述实验还不够完善,还需要补充的一个实验是
将铁钉置于干燥空气中
将铁钉置于干燥空气中
;(5)请你提出防止钢铁锈蚀的两条合理措施①
进行表面防护处理
进行表面防护处理
,②改变金属内部结构
改变金属内部结构
.
