摘要:15.向滴有石蕊试液的稀盐酸溶液中.慢慢滴入氢氧化钠溶液直止过量.溶液颜色变化的过程是---------------------------- A.红→蓝→紫 B.紫→蓝→红 C.蓝→紫→红 D.红→紫→蓝
网址:http://m.1010jiajiao.com/timu3_id_3992757[举报]
向稀盐酸中滴入紫色石蕊试液,石蕊会变成红色,稀盐酸中主要含有H+、Clˉ、H2O分子.某探究小组为探究稀盐酸中的哪种微粒能使石蕊试液变红,设计了如下实验方案,得出了初步结论.
(1)请填写下表中的实验结论:
(2)是否还需要做“向水中滴加酚酞试液”的对比实验?为什么?
查看习题详情和答案>>
(1)请填写下表中的实验结论:
| 实 验 过 程 | 实验现象 | 实 验 结 论 |
| 向盛有少量NaCl溶液的试管中滴入石蕊试液,振荡 | 溶液无明显 变化 |
查看习题详情和答案>>
盐酸和氢氧化钠溶液发生反应过程中溶液的pH变化如图一,请分析并回答问题: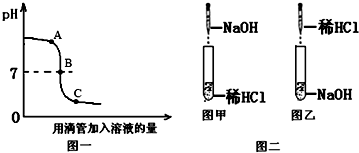
(1)根据pH变化图象判断,该反应的实验过程是按照图二中的图______(选填“甲”或“乙”)进行.
(2)图一中A、B、C三点表示的溶液,二种反应物恰好完全反应的是______(选填“A”“B”或“C”,下同)点的溶液:加入紫色石蕊溶液会呈现红色的是______点的溶液,此时溶液中一定含有的阳离子是______.
(3)为了探究盐酸与氢氧化钠溶液反应的生成物,小明的实验操作过程如下:
实验过程:向装有一定量稀盐酸的试管中滴加氢氧化钠溶液,振荡后再滴加硝酸银溶液.
得出结论:证明生成了氯化钠
小思认为该结论不正确,合理的解释是______.
查看习题详情和答案>>

(1)根据pH变化图象判断,该反应的实验过程是按照图二中的图______(选填“甲”或“乙”)进行.
(2)图一中A、B、C三点表示的溶液,二种反应物恰好完全反应的是______(选填“A”“B”或“C”,下同)点的溶液:加入紫色石蕊溶液会呈现红色的是______点的溶液,此时溶液中一定含有的阳离子是______.
(3)为了探究盐酸与氢氧化钠溶液反应的生成物,小明的实验操作过程如下:
实验过程:向装有一定量稀盐酸的试管中滴加氢氧化钠溶液,振荡后再滴加硝酸银溶液.
得出结论:证明生成了氯化钠
小思认为该结论不正确,合理的解释是______.
向盛有10mL稀盐酸(其中滴有少量紫色石蕊试剂)的烧杯中加入氢氧化钠溶液,用pH计(测pH的仪器)测定溶液的pH,所得数据如下.请分析并回答下列问题:
(1)当加入氢氧化钠溶液的体积为
(2)当加入氢氧化钠溶液的体积为12mL时,溶液显
(3)当烧杯中溶液的pH=1.4时,溶液中的溶质有
(4)若要配制40g质量分数为15%的氢氧化钠溶液,需称取氢氧化钠固体的质量为
10%,则需要加入水
查看习题详情和答案>>
| 加入NaOH溶液的体积/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 |
| 烧杯中溶液的pH | 1.1 | 1.2 | 1.4 | 1.6 | 2.0 | 7.0 | 11.0 | 12.2 |
10
10
mL时,稀盐酸和氢氧化钠溶液恰好完全反应;(2)当加入氢氧化钠溶液的体积为12mL时,溶液显
蓝
蓝
色;(3)当烧杯中溶液的pH=1.4时,溶液中的溶质有
NaCl、HCl
NaCl、HCl
(写化学式);(4)若要配制40g质量分数为15%的氢氧化钠溶液,需称取氢氧化钠固体的质量为
6
6
g,若将该氢氧化钠溶液稀释到10%,则需要加入水
20
20
mL.