网址:http://m.1010jiajiao.com/timu3_id_398905[举报]
右图为氯化钠晶体的结构示意图。已知:Mr(NaCl)=58.5 g· mol-1 ρ(NaCl)=2.2 g· cm-3NA=6.02×1023 mol-1,试求氯化钠晶体中两个最近的Na+中心间的距离。
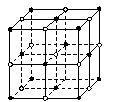

(1)在NaCl晶体中,每个Na+同时吸引_____个Cl-,而Na+数目与Cl-数目之比为_____。
(2)NaCl晶体离子键的键长为_____。
(3)Na+半径与Cl-半径之比r(Na+)/r(Cl-)=_______。
(已知:
 = 1.414,
= 1.414,  =1.732,
=1.732, 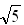 =2.236)
=2.236) (4)NaCl中晶体不存在分子,但在温度达到1 413℃时,NaCl晶体形成气体,并以分子形式存在。现有29.25g NaCl晶体,加强热使温度达到1 450℃,测得气体体积为5.6 L(已折算为标准状况),则此时氯化钠气体的分子式(化学式)为__________。
 (08年龙海五中最后三卷)氢能是理想的无污染的绿色能源,利用太阳能光催化裂解水制取氢气是能源的一次新技术革命。钙钛矿型层状氧化物是一种新型光催化剂。右图为钙铁矿晶体结构示意圈.下列有关说法不正确的是( )
(08年龙海五中最后三卷)氢能是理想的无污染的绿色能源,利用太阳能光催化裂解水制取氢气是能源的一次新技术革命。钙钛矿型层状氧化物是一种新型光催化剂。右图为钙铁矿晶体结构示意圈.下列有关说法不正确的是( )
A.钙钛矿的化学式可表示为![]()
B.钙钛矿晶体中与1个Ca2+距离最近且等距离的O2-有6个
C.太阳能光催化裂解水制氢气的反应可表示为:![]()
D.太阳能光催化裂解水制氢气的反应为放热反应
查看习题详情和答案>>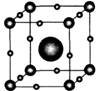 (08年龙海五中最后三卷)氢能是理想的无污染的绿色能源,利用太阳能光催化裂解水制取氢气是能源的一次新技术革命。钙钛矿型层状氧化物是一种新型光催化剂。右图为钙铁矿晶体结构示意圈.下列有关说法不正确的是( )
(08年龙海五中最后三卷)氢能是理想的无污染的绿色能源,利用太阳能光催化裂解水制取氢气是能源的一次新技术革命。钙钛矿型层状氧化物是一种新型光催化剂。右图为钙铁矿晶体结构示意圈.下列有关说法不正确的是( )
A.钙钛矿的化学式可表示为![]()
B.钙钛矿晶体中与1个Ca2+距离最近且等距离的O2-有6个
C.太阳能光催化裂解水制氢气的反应可表示为:![]()
D.太阳能光催化裂解水制氢气的反应为放热反应
查看习题详情和答案>>
[化学—物质结构与性质]铜是过渡元素。化合物中,铜常呈现+1价或+2价。
(1)右图为某铜矿晶体结构单元,该铜矿的化学式为________。
(2)已知,铜的第一电离能为746kJ·mol-1,第二电离能为
1958kJ·mol-1。请结合核外电子排布相关知识解释,铜第二电离能远
远大于第一电离能的原因![]()
答:____________________________________。
(3)对于CuX(X为卤素)而言,铜与X形成的化学键极性越强,对应的CuX的溶解度越大。据此可知,CuCl的溶解度比CuI的溶解度__________(填“更大”或“更小”)。
(4)CO、NH3都能提供孤电子对与Cu+形成配合物。Cu+与NH3形成的配合物可表示为[Cu(NH3) n]+。该配合物中,Cu+的4s轨道及4p轨道通过sp杂化接受NH3提供的孤电子对。
①[Cu(NH3)n]+中n =______________________。
②[Cu(NH3) n]+中Cu+与n个氮原子构成的空间结构呈___________型。
③[Cu(NH3) n]+溶液可用于吸收合成氨原料气中的CO,加热吸收CO后的溶液又将放出CO。加热分解放出CO的过程中,必须克服微粒间的哪类作用力?答:______________。
查看习题详情和答案>>