网址:http://m.1010jiajiao.com/timu3_id_3988931[举报]
研究化学反应原理对于生产生活是很有意义的。
(1)下列关于醋酸的叙述正确的是 (填写符号)。
a.醋酸俗名冰醋酸,是食醋的主要成分
b.向醋酸溶液中加入一定量NaOH固体,溶液的导电性增强
c.加水稀释醋酸溶液,溶液中的所有离子浓度均减小
d.常温下,醋酸溶液中水的电离程度减小
(2)牙釉质对牙齿起着保护作用,其主要成分为Ca5(PO4)3OH,该物质在水中存在沉淀溶解
平衡,试写出该物质的溶度积常数表达式Kap= 。
(3)钢铁生锈现象随处可见,钢铁的电化腐蚀原理
如图所示:
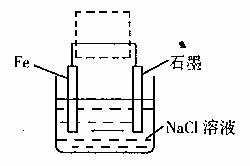
①写出石墨电极的电极反应式 ;
②将该装置作简单修改即可成为钢铁电化学防护的装置,请在右图虚线框内所示位置作出修改,并用箭头标出导线中电子流动方向。
③写出修改后石墨电极的电极反应式 。
查看习题详情和答案>>(14分)在化学反应中,只要物质所含元素的化合价发生变化的反应就是氧化还原反应。例如:2Na+C12 =2NaCl,反应前后,Na元素、Cl元素的化合价分别发生了变化,该反应是氧化还原反应。
(1)根据化合价是否变化分析,下列反应(部分反应条件略去)属于氧化还原反应的是
(填写序号);
①C+O2 == CO2 ②CaO+H2O==Ca(OH)2 ③CaCO3==CaO+CO2↑
④2H2O2 == 2H2O+O2↑ ⑤CO+CuO=Cu+CO2 ⑥HCl+NaOH=NaCl+H2O
(2) 含有高价态元素的化合物,通常具有氧化性,如在氯化铁溶液中,氯化铁能将单质铜氧化成氯化铜,自身被还原成氯化亚铁。试回答下列问题:
①该反应的化学方程式可表示为 ;
②向上述反应后的溶液中加入过量的锌粉充分反应后过滤,则滤纸上一定有的固体是
(写化学式,下同),滤液中的溶质是 。
(3) 通过进一步定量分析上述氧化还原反应的化合价变化发现:氧化还原反应中其元素化合价升高总数 (填“大于”、“等于”或“小于”)化合价降低升高总数。氟气是氧化性最强的非金属单质,在加热条件下,等物质的量的F2和烧碱完全反应,生成NaF、H2O和另一种气体,该气体可能是_______。 (写化学式)
(4)柠檬果汁中含有维生素C(C6H8O6,简写成Vc)是还原剂,它能被I2氧化生成C6H6O6。当前市场上测定柠檬果汁中Vc含量的方法是取10.00mL果汁,用醋酸酸化,再加入20.00mL 0.02500 mol?dm-3标准碘溶液,然后以淀粉溶液作指示剂,最后用0.01000 mol?dm-3Na2S2O3标准溶液滴定过量的I2,消耗Na2S2O3溶液10.00mL。
①Vc中碳元素的平均化合价是 。
②写出Vc与I2反应的离子方程式。
③此份果汁中含Vc= mg/100mL果汁。
查看习题详情和答案>>
现有一定量含有NaOH杂质的Na2O2试样5.00 g,分成等质量两份,用两种方法测定Na2O2试样的纯度。请填写下列空白:
(1)第一种方法:取第一份试样,从下图中选用适当的实验装置,设计一个实验以测定过氧化钠的纯度(可供选用的反应物只有CaCO3固体、MnO2固体、6 mol·L-1盐酸和蒸馏水).

 ①若实验要求装置尽可能简单,应选用上图中的装置是(只要求写出图中装置的标号) 。
①若实验要求装置尽可能简单,应选用上图中的装置是(只要求写出图中装置的标号) 。
②所选用装置的连接顺序应是(填各接口的字母;连接胶管略). 。
③若实验过程中共产生氧气140 mL(已折算成标准状况),则试样中过氧化钠的纯度为 。
(2)第二种方法:取第二份试样,配成250.00 mL溶液,用0.255 0 mol·L-1的标准盐酸滴定。
① 取上述所配溶液25.00 mL于锥形瓶中,操作如下图所示(手持部分省略):正确的操作是图 ,
取溶液所用仪器的名称是 。
② 滴定操作平行实验的数据记录如下表:
|
| 第一次滴定 | 第二次滴定 | 第三次滴定 |
| 消耗标准盐酸的体积(mL) | 24.98 | 25.00 | 25.02 |
由表中数据计算样品中Na2O2纯度为 。
(3)若上述两个实验中不存在重大的操作失误,测得的实验数据也是真实可靠的,但以上两种方法测得的Na2O2纯度数据误差较大。
① 你认为上述两种方法中,哪种方法更为可靠 ?
② 产生较大实验误差的原因最可能是 。
③ 在题中所给出的仪器和药品范围内,如何用简单的方法加以改进,使实验误差大为减少,写出改进的方法 。
查看习题详情和答案>>
现有一定量含有NaOH杂质的Na2O2试样5.00 g,分成等质量两份,用两种方法测定Na2O2试样的纯度。请填写下列空白:
(1)第一种方法:取第一份试样,从下图中选用适当的实验装置,设计一个实验以测定过氧化钠的纯度(可供选用的反应物只有CaCO3固体、MnO2固体、6 mol·L-1盐酸和蒸馏水).
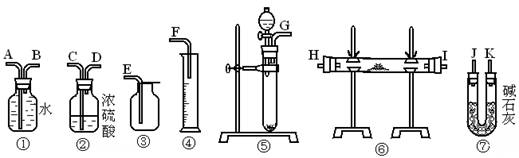
 ①若实验要求装置尽可能简单,应选用上图中的装置是(只要求写出图中装置的标号) 。
①若实验要求装置尽可能简单,应选用上图中的装置是(只要求写出图中装置的标号) 。
②所选用装置的连接顺序应是(填各接口的字母;连接胶管略). 。
③若实验过程中共产生氧气140 mL(已折算成标准状况),则试样中过氧化钠的纯度为 。
(2)第二种方法:取第二份试样,配成250.00 mL溶液,用0.255 0 mol·L-1的标准盐酸滴定。
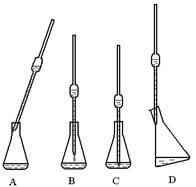
① 取上述所配溶液25.00 mL于锥形瓶中,操作如下图所示(手持部分省略):正确的操作是图 ,
取溶液所用仪器的名称是 。
② 滴定操作平行实验的数据记录如下表:
|
|
第一次滴定 |
第二次滴定 |
第三次滴定 |
|
消耗标准盐酸的体积(mL) |
24.98 |
25.00 |
25.02 |
由表中数据计算样品中Na2O2纯度为 。
(3)若上述两个实验中不存在重大的操作失误,测得的实验数据也是真实可靠的,但以上两种方法测得的Na2O2纯度数据误差较大。
① 你认为上述两种方法中,哪种方法更为可靠 ?
② 产生较大实验误差的原因最可能是 。
③ 在题中所给出的仪器和药品范围内,如何用简单的方法加以改进,使实验误差大为减少,写出改进的方法 。
查看习题详情和答案>>