摘要:我们学过的氢气.一氧化碳.碳三种物质的共同点是 A.都具有可燃性和还原性 B.都是单质 C.在一定条件下都能与二氧化碳起反应 D.燃烧时都生成二氧化碳
网址:http://m.1010jiajiao.com/timu3_id_3988265[举报]
让我们和小亮一起走进化学实验室,共同来学习科学探究的方法.
小亮在实验室用一小块生铁与稀盐酸反应,观察到生铁表面出现 ,同时发现反应后的液体中有少量黑色不溶物.
提出问题:这种黑色不溶物是什么呢?
猜想与假设:这种黑色不溶物中可能含碳.
设计方案:将黑色固体灼烧,如果黑色固体中含有碳,就会有 (填化学式)气体生成,要想进一步确定这种气体,可以用 (填俗称)来检验,其化学方程式为 、 .
进行实验:小亮按设计方案进行实验,得到了预想的结果.
解释与结论:由此小亮得出结论:
(1)生铁中 碳(填“含”或“不含”);
(2)碳与稀盐酸 反应(填“能”或“不能”),铁与稀盐酸 反应(填“能”或“不能”).
请你和小明一起进行实验室制取二氧化碳的探究.
(1)选择药品.小明对三组药品进行了研究,实验记录如下:
从制取和 的角度分析,一般选择第 ①组药品,该组药品发生反应的化学方程式
为 ;
不选择第③组药品的原因是 .
(2)选择装置.通过对制取氧气装置的分析,他选择用过氧化氢制取氧气的发生装置.你认为他选择的依据是 .
(3)制取气体.将药品装入所选装置制取气体,并用向上排空气法收集.
验满方法是 .
(4)气体检验.将生成的气体通入石蕊溶液中,溶液变红,因此他确定该气体是二氧化碳.他的检验方法是否正确?请说明理由.
.
查看习题详情和答案>>
小亮在实验室用一小块生铁与稀盐酸反应,观察到生铁表面出现
提出问题:这种黑色不溶物是什么呢?
猜想与假设:这种黑色不溶物中可能含碳.
设计方案:将黑色固体灼烧,如果黑色固体中含有碳,就会有
进行实验:小亮按设计方案进行实验,得到了预想的结果.
解释与结论:由此小亮得出结论:
(1)生铁中
(2)碳与稀盐酸
请你和小明一起进行实验室制取二氧化碳的探究.
(1)选择药品.小明对三组药品进行了研究,实验记录如下:
| 组别 | 药品 | 实验现象 |
| ① | 块状石灰石和稀盐酸 | 产生气泡速率适中 |
| ② | 块状石灰石和稀硫酸 | 产生气泡速率缓慢并逐渐停止 |
| ③ | 碳酸钠粉末和稀盐酸 | 产生气泡速率很快 |
为
不选择第③组药品的原因是
(2)选择装置.通过对制取氧气装置的分析,他选择用过氧化氢制取氧气的发生装置.你认为他选择的依据是
(3)制取气体.将药品装入所选装置制取气体,并用向上排空气法收集.
验满方法是
(4)气体检验.将生成的气体通入石蕊溶液中,溶液变红,因此他确定该气体是二氧化碳.他的检验方法是否正确?请说明理由.
 21、一年的化学学习,我们亲身体验了一系列的探究实验,感受到了化学的无穷魅力.小强在回顾整理下列实验中提炼了许多探究方法:
21、一年的化学学习,我们亲身体验了一系列的探究实验,感受到了化学的无穷魅力.小强在回顾整理下列实验中提炼了许多探究方法:实验一:探究分子在不断运动(如右图)
实验现象:
酚酞溶液变红色
.该实验的探究方法是:对看不见、摸不着的粒子,要“观察它的
运动可以设计实验,通过宏观的现象来间接认识.
实验二:探究二氧化碳与水的反应(取四朵用紫色石蕊溶液染
成紫色的干燥的小花,进行下图所示实验)

实验现象:Ⅰ、Ⅳ中的小花变红.
设计Ⅱ、Ⅲ实验的目的是:
作对比试验.验证水和二氧化碳能否使石蕊变色
.该实验的探究方法是:设计分析
B
(填“A”、“B”或“C”),获得结论.A.仅一个单因素的实验B.有多种因素的对比实验
C.用前面实验的生成物继续实验
实验三:验证二氧化碳与氢氧化钠溶液确实发生了反应(实验如下表所示)

我能写出实验三中方案2所涉及到的一个化学方程式
2NaOH+CO2═Na2CO3+H2O
.我认为方案1的探究方法是
B
(填序号,下同),方案2的探究方法是A
.A.通过验证生成物的存在来判断反应的发生
B.通过密闭容器内气体压强变化程度的对比来判断反应的发生
小结:上述三个实验告诉我们:当某些化学反应现象不明显或不足以说明问题时,要千方百计通过设计出具有明显现象的实验,来准确推知和认识化学反应.又如:如氢氧化钠与稀盐酸的中和反应过程没有任何现象,我们可以通过在氢氧化钠溶液中先滴加
酚酞试液
,然后逐滴加入稀盐酸,通过溶液颜色的变化来判断中和反应的进行.让我们和小亮一起走进化学实验室,共同来学习科学探究的方法.
小亮在实验室用一小块生铁与稀盐酸反应,观察到生铁表面出现______,同时发现反应后的液体中有少量黑色不溶物.
提出问题:这种黑色不溶物是什么呢?
猜想与假设:这种黑色不溶物中可能含碳.
设计方案:将黑色固体灼烧,如果黑色固体中含有碳,就会有______(填化学式)气体生成,要想进一步确定这种气体,可以用______(填俗称)来检验,其化学方程式为______、______.
进行实验:小亮按设计方案进行实验,得到了预想的结果.
解释与结论:由此小亮得出结论:
(1)生铁中______碳(填“含”或“不含”);
(2)碳与稀盐酸______反应(填“能”或“不能”),铁与稀盐酸______反应(填“能”或“不能”).
请你和小明一起进行实验室制取二氧化碳的探究.
(1)选择药品.小明对三组药品进行了研究,实验记录如下:
| 组别 | 药品 | 实验现象 |
| ① | 块状石灰石和稀盐酸 | 产生气泡速率适中 |
| ② | 块状石灰石和稀硫酸 | 产生气泡速率缓慢并逐渐停止 |
| ③ | 碳酸钠粉末和稀盐酸 | 产生气泡速率很快 |
为______;
不选择第③组药品的原因是______.
(2)选择装置.通过对制取氧气装置的分析,他选择用过氧化氢制取氧气的发生装置.你认为他选择的依据是______.
(3)制取气体.将药品装入所选装置制取气体,并用向上排空气法收集.
验满方法是______.
(4)气体检验.将生成的气体通入石蕊溶液中,溶液变红,因此他确定该气体是二氧化碳.他的检验方法是否正确?请说明理由.
____________. 查看习题详情和答案>>
白醋是我们日常生活中常用的调味品,白醋中含有3%~5%的醋酸(CH3COOH).某化学研究小组围绕白醋开展了下列探究.
Ⅰ.探究白醋的性质.
请完成表格内的相关内容:(可选择的试剂:白醋、镁条、碳酸钠粉末、5%的氢氧化钠溶液、酚酞试液、石蕊试液)
Ⅱ.探究影响化学反应快慢的因素.
该小组同学根据酸的性质想到,白醋也能与铁锈反应.于是他们将生锈的铁钉放入白醋中,没有看到明显现象,老师提示这可能是因反应太慢造成的,于是他们对影响白醋与铁锈反应快慢的因素展开了探究.
【猜想】影响白醋与铁锈反应快慢的因素可能有:温度、铁锈的表面积大小、______等.
【探究过程】实验用品:5%的醋酸溶液、10%的醋酸溶液、20%的醋酸溶液、锈蚀程度相同的铁钉数枚、酒精灯、大试管等.
实验1.实验方案:如图,向三支试管中分别加入10mL不同浓度的醋酸溶液,然后同时放入锈蚀程度相同的铁钉1枚,观察现象.
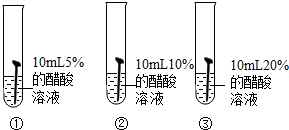
现象:试管①中看不到明显现象;试管②中铁锈消失较慢;试管③中铁锈很快消失.
结论:______.
实验2.实验方案:(请用简要文字说明)______.
结论:升高温度,白醋与铁锈反应能加快.
【总结反思】依据实验室制氧气的原理,______也是影响化学反应快慢的因素.
查看习题详情和答案>>
Ⅰ.探究白醋的性质.
请完成表格内的相关内容:(可选择的试剂:白醋、镁条、碳酸钠粉末、5%的氢氧化钠溶液、酚酞试液、石蕊试液)
| 序号 | 实验方案 | 现象 | 结论 |
| 方案一 | 取少量白醋于试管中,加入紫色石蕊试液 | ______ | 白醋呈酸性 |
| 方案二 | ______ | ______ | 白醋能于碱反应 |
| 方案三 | ______ | ______ | ______ |
该小组同学根据酸的性质想到,白醋也能与铁锈反应.于是他们将生锈的铁钉放入白醋中,没有看到明显现象,老师提示这可能是因反应太慢造成的,于是他们对影响白醋与铁锈反应快慢的因素展开了探究.
【猜想】影响白醋与铁锈反应快慢的因素可能有:温度、铁锈的表面积大小、______等.
【探究过程】实验用品:5%的醋酸溶液、10%的醋酸溶液、20%的醋酸溶液、锈蚀程度相同的铁钉数枚、酒精灯、大试管等.
实验1.实验方案:如图,向三支试管中分别加入10mL不同浓度的醋酸溶液,然后同时放入锈蚀程度相同的铁钉1枚,观察现象.

现象:试管①中看不到明显现象;试管②中铁锈消失较慢;试管③中铁锈很快消失.
结论:______.
实验2.实验方案:(请用简要文字说明)______.
结论:升高温度,白醋与铁锈反应能加快.
【总结反思】依据实验室制氧气的原理,______也是影响化学反应快慢的因素.
26、空气是一种十分重要的天然资源.
(1)空气成分按体积计算,含量最多的是
(2)实验室可通过多种途径制取氧气,如分解过氧化氢、加热高锰酸钾、电解水等,因为这三种物质都含有
(3)保护空气,提倡“低碳”,减少温室效应,是我们必须关注的问题.科学家正在研究如图所示的二氧化碳新的循环体系.

从图中分析得出的下列结论中,正确的是
A.二氧化碳也是一种重要的资源 B.利用降温、加压将二氧化碳分离是化学变化
C.二氧化碳与氢气在复合催化剂下反应产物是混合物 D.液化石油气、汽油、甲醇等物质燃烧都有二氧化碳产生
(4)酸雨的形成主要是二氧化硫与水作用产生的亚硫酸(H2SO3)被空气中的氧气氧化为硫酸(H2SO4)的缘故.该氧化反应的化学方程式为
(5)“绿色化学”的特点之一是“零排放”.一定条件下,一氧化碳和氢气可以按照不同比例反应,若只生成一种产物就能实现“零排放”,符合这一要求的产物是
A.甲醇(CH4O) B.甲醛(CH2O)
C.乙醇(C2H6O) D.乙醛(C2H4O)
查看习题详情和答案>>
(1)空气成分按体积计算,含量最多的是
N2
(填写化学式).(2)实验室可通过多种途径制取氧气,如分解过氧化氢、加热高锰酸钾、电解水等,因为这三种物质都含有
O
元素(填元素符号);从降低能量消耗上思考,你选择的实验室制取氧气的方法是分解过氧化氢
.(3)保护空气,提倡“低碳”,减少温室效应,是我们必须关注的问题.科学家正在研究如图所示的二氧化碳新的循环体系.

从图中分析得出的下列结论中,正确的是
ACD
(填字母序号).A.二氧化碳也是一种重要的资源 B.利用降温、加压将二氧化碳分离是化学变化
C.二氧化碳与氢气在复合催化剂下反应产物是混合物 D.液化石油气、汽油、甲醇等物质燃烧都有二氧化碳产生
(4)酸雨的形成主要是二氧化硫与水作用产生的亚硫酸(H2SO3)被空气中的氧气氧化为硫酸(H2SO4)的缘故.该氧化反应的化学方程式为
SO2+H2O═H2SO3;2H2SO3+O2═2H2SO4
(5)“绿色化学”的特点之一是“零排放”.一定条件下,一氧化碳和氢气可以按照不同比例反应,若只生成一种产物就能实现“零排放”,符合这一要求的产物是
A、B
(填字母序号).A.甲醇(CH4O) B.甲醛(CH2O)
C.乙醇(C2H6O) D.乙醛(C2H4O)