摘要:Ⅰ将一定质量的铁粉加入到装有100 mL某浓度的稀硝酸溶液中充分反应. ⑴容器中剩有m g的铁粉.收集到NO气体448 mL. ① 所得溶液中的溶质的化学式是 , ② 原硝酸溶液的物质的量浓度为: mol/L ⑵向上述固-液混合物中逐滴加入稀硫酸直到刚好不再产生气体为止.该气体遇空气变成红棕色.此时容器中有铁粉n g. ①此时溶液中溶质的化学式是 , ②m–n的值为 g . Ⅱ:向某密闭容器中加人 0.3 molA.0.1 molC和一定量的B三种气体.一定条件下发生反应.各物质浓度随时间的变化如下图中甲图所示.附图中乙图为 t2时刻后改变容器中条件.平衡体系中反应速率随时间变化的情况.且四个阶段都各改变一种不同的条件.所用条件均不同.已知t3 ~t4阶段为使用催化剂[已知 t0~ t1阶段 c ( B)未画出]. (1)若 t1= 15 s .则t0~ t1阶段以C 浓度变化表示的反应速率为 , (2)t4 ~t5阶段改变的条件为 .B的起始物质的量为 , (3)t5 ~t6阶段容器内A的物质的量共减少0. 03 mol .而此过程中容器与外界的热交换总量为akJ .写出该反应的热化学方程式 .
网址:http://m.1010jiajiao.com/timu3_id_398693[举报]
将一定质量的铁粉加入到装有100 ml某浓度的稀硝酸溶液中充分反应。
(1)容器中剩有m g的铁粉,收集到NO气体448 ml(标准状况下)。
①所得溶液中的溶质的化学式是____________;
②原硝酸溶液的物质的量浓度为__________ mol/L。
(2)向上述固-液混合物中逐滴加入稀硫酸直到刚好不再产生气体为止,该气体遇空气变成红棕色。此时容器中有铁粉n g。
①此时溶液中溶质的化学式是 ____________ ;
②m-n的值为(计算精确到0.1g)____________ g 。
查看习题详情和答案>>某草酸亚铁样品中含有少量硫酸亚铁.现用滴定法测定该样品中FeC2O4的含量.滴定反应是:
5Fe2++5C2O42-+3MnO4-+24H+═5Fe3++10CO2↑+3Mn2++12H2O.
实验方案设计为:
①将准确称量的a g草酸亚铁样品置于250mL锥形瓶内,加入适量2mol/L的H2SO4溶液,使样品溶解,加热至70℃左右,立即用浓度为0.02000mol/L的高锰酸钾标准溶液滴定至终点,记下滴定管内液面读数为b ml.
②向上述滴定混合液中加入适量的Zn粉和过量的2mol/L的H2SO4溶液,煮沸5-8min,经检验溶液合格后(不含Fe3+),继续用0.02000mol/L的高锰酸钾标准溶液滴定至终点,记下滴定管内液面读数为c ml.
③______.
④数据处理.
请回答下列问题:
(1)上述实验方案中的步骤③是______.
(2)洁净的滴定管在滴定前必须进行的操作是:
Ⅰ.______;
Ⅱ.用高锰酸钾标准溶液润洗滴定管;
Ⅲ.加入高锰酸钾标准溶液,赶走尖嘴部位的气泡;
Ⅳ.______.
(3)步骤②中检验溶液是否合格的操作是:取1滴煮沸后的溶液滴入装有______溶液的试管中,如______,则说明溶液合格.
(4)某实验探究小组的一次测定数据记录如下:
| a/g | 起始读数/mL | b/mL | c/mL |
| 0.1582 | 0.00 | 29.90 | 40.90 |
| 0.1582 | 0.00 | 30.10 | 41.10 |
| 0.1582 | 0.00 | 32.10 | 43.10 |
某草酸亚铁样品中含有少量硫酸亚铁.现用滴定法测定该样品中FeC2O4的含量.滴定反应是:
5Fe2++5C2O42-+3MnO4-+24H+═5Fe3++10CO2↑+3Mn2++12H2O.
实验方案设计为:
①将准确称量的a g草酸亚铁样品置于250mL锥形瓶内,加入适量2mol/L的H2SO4溶液,使样品溶解,加热至70℃左右,立即用浓度为0.02000mol/L的高锰酸钾标准溶液滴定至终点,记下滴定管内液面读数为b ml.
②向上述滴定混合液中加入适量的Zn粉和过量的2mol/L的H2SO4溶液,煮沸5-8min,经检验溶液合格后(不含Fe3+),继续用0.02000mol/L的高锰酸钾标准溶液滴定至终点,记下滴定管内液面读数为c ml.
③______.
④数据处理.
请回答下列问题:
(1)上述实验方案中的步骤③是______.
(2)洁净的滴定管在滴定前必须进行的操作是:
Ⅰ.______;
Ⅱ.用高锰酸钾标准溶液润洗滴定管;
Ⅲ.加入高锰酸钾标准溶液,赶走尖嘴部位的气泡;
Ⅳ.______.
(3)步骤②中检验溶液是否合格的操作是:取1滴煮沸后的溶液滴入装有______溶液的试管中,如______,则说明溶液合格.
(4)某实验探究小组的一次测定数据记录如下:
根据数据计算0.1582g 样品中:n(Fe2+)=______; n(C2O42-)=______;FeC2O4(FeC2O4 的摩尔质量为144g/mol)的质量分数为______.(精确到0.1%)
查看习题详情和答案>>
5Fe2++5C2O42-+3MnO4-+24H+═5Fe3++10CO2↑+3Mn2++12H2O.
实验方案设计为:
①将准确称量的a g草酸亚铁样品置于250mL锥形瓶内,加入适量2mol/L的H2SO4溶液,使样品溶解,加热至70℃左右,立即用浓度为0.02000mol/L的高锰酸钾标准溶液滴定至终点,记下滴定管内液面读数为b ml.
②向上述滴定混合液中加入适量的Zn粉和过量的2mol/L的H2SO4溶液,煮沸5-8min,经检验溶液合格后(不含Fe3+),继续用0.02000mol/L的高锰酸钾标准溶液滴定至终点,记下滴定管内液面读数为c ml.
③______.
④数据处理.
请回答下列问题:
(1)上述实验方案中的步骤③是______.
(2)洁净的滴定管在滴定前必须进行的操作是:
Ⅰ.______;
Ⅱ.用高锰酸钾标准溶液润洗滴定管;
Ⅲ.加入高锰酸钾标准溶液,赶走尖嘴部位的气泡;
Ⅳ.______.
(3)步骤②中检验溶液是否合格的操作是:取1滴煮沸后的溶液滴入装有______溶液的试管中,如______,则说明溶液合格.
(4)某实验探究小组的一次测定数据记录如下:
| a/g | 起始读数/mL | b/mL | c/mL |
| 0.1582 | 0.00 | 29.90 | 40.90 |
| 0.1582 | 0.00 | 30.10 | 41.10 |
| 0.1582 | 0.00 | 32.10 | 43.10 |
查看习题详情和答案>>
(2012?门头沟区一模)黄铁矿石的主要成分为FeS2和少量FeS(假设其他杂质中不含Fe、S元素,且高温下不发生化学变化),是我国大多数硫酸厂制取硫酸的主要原料.某化学兴趣小组对该黄铁矿石进行如下实验探究.
将m1g该黄铁矿石的样品放入如下图装置(夹持和加热装置略)的石英管中,从a处不断地缓缓通入空气,高温灼烧黄铁矿样品至反应完全.其反应的化学方程式为:
4FeS2+11O2
2Fe2O3+8SO2
4FeS+7O2
2Fe2O3+4SO2
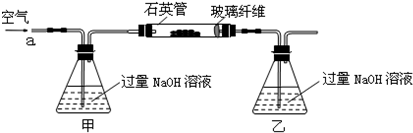
实验一:测定硫元素的含量
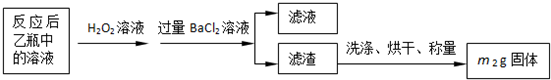
反应结束后,将乙瓶中的溶液进行如下处理:
(1)甲、乙两装置的作用分别是
乙瓶内发生反应的离子方程式为
(2)反应后乙瓶中的溶液需加足量H2O2溶液的目的是
(3)该黄铁矿石中硫元素的质量分数为
×100%
×100%.
实验二:测定铁元素的含量
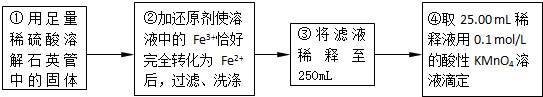
(4)②中,若用铁粉作还原剂,则所测得的铁元素的含量
(5)③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有
(6)某同学一共进行了三次滴定实验,三次实验结果记录如下:
根据所给数据,计算该稀释液中Fe2+的物质的量浓度为c(Fe2+)=
查看习题详情和答案>>
将m1g该黄铁矿石的样品放入如下图装置(夹持和加热装置略)的石英管中,从a处不断地缓缓通入空气,高温灼烧黄铁矿样品至反应完全.其反应的化学方程式为:
4FeS2+11O2
| ||
4FeS+7O2
| ||

实验一:测定硫元素的含量
反应结束后,将乙瓶中的溶液进行如下处理:

(1)甲、乙两装置的作用分别是
除去空气中的CO2 使乙装置中的溶液只吸收黄铁矿煅烧产生的SO2
除去空气中的CO2 使乙装置中的溶液只吸收黄铁矿煅烧产生的SO2
、吸收黄铁矿煅烧产生的SO2
吸收黄铁矿煅烧产生的SO2
;乙瓶内发生反应的离子方程式为
SO2+2OH-=SO32-+H2O
SO2+2OH-=SO32-+H2O
、2SO32-+O2=2SO42-
2SO32-+O2=2SO42-
;(2)反应后乙瓶中的溶液需加足量H2O2溶液的目的是
使SO32-完全氧化为SO42-
使SO32-完全氧化为SO42-
.(3)该黄铁矿石中硫元素的质量分数为
| 32m2 |
| 233m1 |
| 32m2 |
| 233m1 |
实验二:测定铁元素的含量

(4)②中,若用铁粉作还原剂,则所测得的铁元素的含量
偏大
偏大
(填“偏大”、“偏小”或“无影响”).(5)③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有
250ml容量瓶
250ml容量瓶
.(6)某同学一共进行了三次滴定实验,三次实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗KMnO4溶液体积/mL | 25.00 | 25.03 | 24.97 |
0.5mol/L
0.5mol/L
.