摘要:青海湖是我国最大的内陆盐湖.盛产天然碱.天然碱是天然形成的碳酸钠和碳酸氢钠的结晶水合物.其化学式可用m Na2CO3·n NaHCO3·k H2O表示.某校初三自然科学探究小组同学为了测定一种天然碱的组成.进行了如下实验: ① 称取3.32克天然碱样品.溶解在足量的稀盐酸中.产生1.32克二氧化碳, ② 另称取3.32克天然碱样品.在300℃下加热至质量不再减少.产生0.22克二氧化碳和0.45克水. 试通过计算.确定该天然碱的化学式.(提示:300℃下加热.碳酸钠不分解.而碳酸氢钠分解成碳酸钠.二氧化碳和水) 5.2003年10月15日上午.我国首位航天员杨利伟乘坐“神舟五号 载人飞船.在酒泉卫星发射中心成功升空.并按预定计划绕地球飞行了14圈.历时21小时23分.行程60万公里.于16日清晨成功返回.首次载人航天飞行的圆满成功.标志着我国成为继前苏联.美国后第三个进入太空的国家.这是我们伟大祖国的经济实力.科技实力和综合国力日益强大的象征.华夏儿女为之欢欣鼓舞.请根据你所学的自然科学相关知识.回答下列有关航天航空方面的问题: (1) 火箭发射时.能量的转化情况主要是 ▲ . A.太阳能转化为机械能 B.机械能转化为化学能 C.化学能转化为机械能 D.电能转化为机械能 (2) “神舟五号 通过喷射燃气完成了变轨.姿态确定(即改变运行高度和运行方向)等数百个运行动作.这是应用了物理学中哪条原理? ▲ ,而太阳能电池帆板展开.是为了 ▲ . (3) 若在飞船舱内.航天员拟进行下列实验.估计最难完成的是 ▲ . A.用温度计测温度 B.用显微镜观察叶绿体 C.在水中溶解食盐 D.用漏斗.滤纸过滤除去水中的泥沙 (4) 航天飞船内需配备氧气的再生装置.以保证长时间的飞行.过氧化钠(Na2O2)固体在常温下能与二氧化碳发生如下反应:2 Na2O2+2 CO2=2 Na2CO3+O2.若将该反应作为飞船内供氧的方法.其最大的优点是 ▲ . (5) 推动“神舟五号 飞船升空的火箭为“长征二号F 火箭.该火箭使用的主要燃料名称是偏二甲肼.其相对分子质量为60.其中含碳40%.含氢13.33%.其余为氮.则偏二甲肼的分子式为 ▲ ,此燃料与氧化剂N2O4混合后发生剧烈反应.燃烧后的产物是氮气.二氧化碳和水.试写出该反应的化学方程式: ▲ (6) 据报道.神舟5号上载有一些植物种子.将这些植物种子经太空旅行再返回地面种植.目的是使决定生物性状的 ▲ 发生变化.从而培育出新品种. 半山钢苑中学科学组 余永新
网址:http://m.1010jiajiao.com/timu3_id_3984181[举报]
青海钾肥厂是我国最大的钾盐生产基地.根据下图判断,下列说法中正确的是

[ ]
A.KCl的溶解度大于NaCl的溶解度
B.23℃时,KCl和NaCl的溶解度不相等
C.50℃时KCl、NaCl两种物质的饱和溶液中,溶质质量分数相等
D.从含有少量NaCl的KCl中,分离NaCl,得到较纯净的KCl,可用冷热饱和溶液的方法
据报道,我国最大的海水淡化研发和制造基地将在我市滨海新区建成.海水是化工原料的主要来源之一,下面是工业上对海水综合利用的示意图
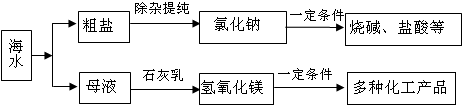
某校化学兴趣小组的同学对海水的有关问题进行了研究:
(1)甲同学查资料获知:石灰乳的主要成分为Ca(OH)2,Ca(OH)2可用高温煅烧海滩贝壳(主要成分为CaCO3)等反应制得,请写出制备Ca(OH)2过程中所发生的化学方程式
(2)乙同学用天平称量一定量的含氯化镁、硫酸钠和氯化钙的粗盐,并设计了如下过程进行除杂提纯,试验后得到较纯净的氯化钠固体.(此题中微溶物视为可溶物)
请回答下列问题:
①写出乙同学所加的试剂:A ;
②白色固体Ⅱ的成分是 ;
白色固体Ⅲ的成分是 ;
③加入适量B溶液的作用是除去 .
查看习题详情和答案>>

某校化学兴趣小组的同学对海水的有关问题进行了研究:
(1)甲同学查资料获知:石灰乳的主要成分为Ca(OH)2,Ca(OH)2可用高温煅烧海滩贝壳(主要成分为CaCO3)等反应制得,请写出制备Ca(OH)2过程中所发生的化学方程式
(2)乙同学用天平称量一定量的含氯化镁、硫酸钠和氯化钙的粗盐,并设计了如下过程进行除杂提纯,试验后得到较纯净的氯化钠固体.(此题中微溶物视为可溶物)

请回答下列问题:
①写出乙同学所加的试剂:A
②白色固体Ⅱ的成分是
白色固体Ⅲ的成分是
③加入适量B溶液的作用是除去
(2013?大丰市一模)(1)人体中必需的微量元素铁、氟、锌、硒、碘等,虽然含量少,但对健康至关重要.下面提供几种微量元素的相关信息,请认真分析并回答下列问题:

①上述微量元素中属于非金属元素的有
②铁原子核外电子数为
③硒原子在化学反应中容易得到2个电子,形成
(2)下面是某同学对所学物质的分类归纳,请仔细分析并回答下列问题:
纯净物
①写出C组物质所属的类别
②在分类所列举的物质中,有一种物质归类错误,这种物质是
③A组物质中的MgO中的阳离子符号为
④D组物质KMnO4中Mn的化合价为
⑤在分类所列举的物质中,单质铝能与足量氢氧化钠溶液反应,方程式为2Al+2NaOH+2H2O=2NaAlO2+3X↑,则X的化学式为
(3)我国南海海域辽阔,那里散布着范围最广的珊瑚礁群,蕴含有巨量的矿产资源、渔业资源等,有“第二个波斯湾”之称.
①南海海域鱼类众多,产量丰富.鱼类能提供的有机营养素主要为
②如图为海水淡化装置,利用的能源是
A.单质 B.氧化物 C.混合物
③从海水中提取食盐,采用的方法是
④南海已成为我国最大的海上化石燃料生产基地.写出你知道的一种化石燃料

(4)如图所示,A、B、C、D、E、F均是初中化学常见物质.A与B发生的是复分解反应,B与C发生的是中和反应,F是人体正常生理活动必不可少的一种盐.结合图中信息,回答有关问题:
①A的化学式为
②C与D反应的化学方程式为
查看习题详情和答案>>

①上述微量元素中属于非金属元素的有
3
3
种.②铁原子核外电子数为
26
26
.③硒原子在化学反应中容易得到2个电子,形成
阴
阴
(选填“阴”或“阳”)离子.(2)下面是某同学对所学物质的分类归纳,请仔细分析并回答下列问题:
纯净物
|
①写出C组物质所属的类别
碱
碱
.②在分类所列举的物质中,有一种物质归类错误,这种物质是
NH4NO3
NH4NO3
.③A组物质中的MgO中的阳离子符号为
Mg2+
Mg2+
.④D组物质KMnO4中Mn的化合价为
+7
+7
.⑤在分类所列举的物质中,单质铝能与足量氢氧化钠溶液反应,方程式为2Al+2NaOH+2H2O=2NaAlO2+3X↑,则X的化学式为
H2
H2
.(3)我国南海海域辽阔,那里散布着范围最广的珊瑚礁群,蕴含有巨量的矿产资源、渔业资源等,有“第二个波斯湾”之称.
①南海海域鱼类众多,产量丰富.鱼类能提供的有机营养素主要为
蛋白质
蛋白质
.②如图为海水淡化装置,利用的能源是
太阳能
太阳能
,获得的蒸馏供能装置蒸馏装置水属于B
B
(填字母序号).A.单质 B.氧化物 C.混合物
③从海水中提取食盐,采用的方法是
蒸发结晶
蒸发结晶
.④南海已成为我国最大的海上化石燃料生产基地.写出你知道的一种化石燃料
煤;或石油;或天然气
煤;或石油;或天然气
.
(4)如图所示,A、B、C、D、E、F均是初中化学常见物质.A与B发生的是复分解反应,B与C发生的是中和反应,F是人体正常生理活动必不可少的一种盐.结合图中信息,回答有关问题:
①A的化学式为
Na2CO3或NaHCO3
Na2CO3或NaHCO3
;B的化学式为HCl
HCl
;F的化学式为NaCl
NaCl
.②C与D反应的化学方程式为
2NaOH+CO2═Na2CO3+H2O
2NaOH+CO2═Na2CO3+H2O
.(2013?句容市一模)(1)我国最大的盐场--渤海湾长芦盐场,因其具有大面积滩涂,日照充足,雨日少,非常适合晒盐,海水晒盐的原理是
(2)粗盐中含有泥沙不溶性杂质和氯化钙等可溶性杂质,某学习小组设计分离氯化钠和氯化钙固体方案如下:

①操作A是
②蒸发氯化钙溶液过程中需要用到的仪器除蒸发皿、烧杯、铁架台(带铁圈)、酒精灯、火柴外,还必须要有的一种仪器是
③有同学提出滤液中含有少量的碳酸钠,应加入
查看习题详情和答案>>
通过减少溶剂使溶质析出或蒸发结晶
通过减少溶剂使溶质析出或蒸发结晶
.(2)粗盐中含有泥沙不溶性杂质和氯化钙等可溶性杂质,某学习小组设计分离氯化钠和氯化钙固体方案如下:

①操作A是
过滤
过滤
.②蒸发氯化钙溶液过程中需要用到的仪器除蒸发皿、烧杯、铁架台(带铁圈)、酒精灯、火柴外,还必须要有的一种仪器是
玻璃棒
玻璃棒
.③有同学提出滤液中含有少量的碳酸钠,应加入
稀盐酸
稀盐酸
至过量,再蒸发结晶才能得到纯净的氯化钠.
人类社会的发展需要充足的能源、丰富的材料、良好的环境.广阔的海洋中蕴含着无穷无尽的资源,开发海洋,利用海洋成为人们关注的热点.
(1)我国最大的盐场--渤海湾长芦盐场,因其具有大面积滩涂,日照充足,雨日少,非常适合晒盐,海水晒盐的原理是 .
(2)某兴趣小组利用如下仪器进行粗盐提纯实验,
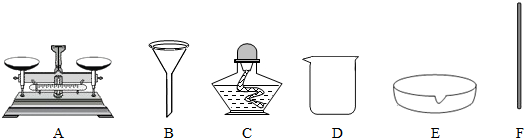
①写出下列仪器的名称:C ,E .
②其具体操作步骤如下:
步骤一:溶解 用托盘天平称取经研钵研磨过的粗盐2.0g投入烧杯中,要对粗盐进行研磨的原因是 .
步骤二:过滤 组装一套过滤器,此时所需要的仪器除需要图中的仪器外还需要的仪器有 ,将粗盐水分几次沿玻璃棒小心倒入漏斗内,玻璃棒所起的作用是 .观察滤纸上方和滤液情形,发现滤液呈混浊状态,其原因可能是 (填一种可能性即可)
步骤三:蒸发 搭建一套蒸发装置,将滤液倒入蒸发皿中,点燃酒精灯加热,并用玻璃棒轻轻搅拌,当 时,撤去酒精灯.待冷却后,用玻璃棒将精盐拨到滤纸上再称量.
③提纯之后该兴趣小组计算的氯化钠的产率偏低(产率=
×100%),则可能的原因是(填字母)
A.溶解含有泥沙的粗盐时,搅拌时间不足
B.过滤时,液面高于滤纸边缘
C.蒸发时,未用玻璃棒搅拌
(3)该小组的小Y同学查阅资料后了解到粗盐中还含有硫酸钠、氯化镁、氯化钙等可溶性杂质,针对实验(2),他提出如下反思:
①这些杂质会在溶解时引入 等杂质离子(写微粒符号)
②可选用如下试剂将它们除去,正确的添加顺序为 (填字母)
A.过量的碳酸钠溶液 B.过量的氯化钡溶液 C.过量的氢氧化钠溶液
③然后将含有沉淀和不溶性泥沙的悬浊液过滤,并在滤液中添加适量的 (填溶液名称)将溶液调至中性.
④所得精盐无必要计算产率,原因是 .
查看习题详情和答案>>
(1)我国最大的盐场--渤海湾长芦盐场,因其具有大面积滩涂,日照充足,雨日少,非常适合晒盐,海水晒盐的原理是
(2)某兴趣小组利用如下仪器进行粗盐提纯实验,

①写出下列仪器的名称:C
②其具体操作步骤如下:
步骤一:溶解 用托盘天平称取经研钵研磨过的粗盐2.0g投入烧杯中,要对粗盐进行研磨的原因是
步骤二:过滤 组装一套过滤器,此时所需要的仪器除需要图中的仪器外还需要的仪器有
步骤三:蒸发 搭建一套蒸发装置,将滤液倒入蒸发皿中,点燃酒精灯加热,并用玻璃棒轻轻搅拌,当
③提纯之后该兴趣小组计算的氯化钠的产率偏低(产率=
| 所得晶体的质量 | 所取样品的质量 |
A.溶解含有泥沙的粗盐时,搅拌时间不足
B.过滤时,液面高于滤纸边缘
C.蒸发时,未用玻璃棒搅拌
(3)该小组的小Y同学查阅资料后了解到粗盐中还含有硫酸钠、氯化镁、氯化钙等可溶性杂质,针对实验(2),他提出如下反思:
①这些杂质会在溶解时引入
②可选用如下试剂将它们除去,正确的添加顺序为
A.过量的碳酸钠溶液 B.过量的氯化钡溶液 C.过量的氢氧化钠溶液
③然后将含有沉淀和不溶性泥沙的悬浊液过滤,并在滤液中添加适量的
④所得精盐无必要计算产率,原因是