摘要:35.为粗略测量空气中O2与N2的体积比.某学生设计了如右图所示的实验装置进行实验.实验时.先关闭弹簧夹a.将螺旋状的铜丝在酒精灯的灼烧后迅速插入大试管.接触试管底部的过量的白磷.然后立即塞紧橡皮塞.由于白磷的着火点比红磷低得多.因此反应很容易发生.可观察到大试管中产生大量的白烟.试回答以下问题: (1)写出磷燃烧的化学方程式 (2)待试管冷却后打开弹簧夹.此时可观察到的现象为 .据此可证实空气中O2与N2的体积比大约为 . (3)如果装置气密性不好.则测出的O2与N2的体积比将 (填“偏大 .“偏小 .或“不变 ).
网址:http://m.1010jiajiao.com/timu3_id_3976321[举报]
 为粗略测量空气中O2与N2的体积比,某学生设计了如 图 所示的实验装置进行实验.实验时,先关闭弹簧夹,将螺旋状的铜 丝在酒精灯上灼烧后迅速插入大试管,接触试管底部的过量的白磷(白磷在空气中燃烧的温度为40℃),然后立即塞紧橡皮塞,可观察到大试管中产生大量的白烟.试回答以下问题:
为粗略测量空气中O2与N2的体积比,某学生设计了如 图 所示的实验装置进行实验.实验时,先关闭弹簧夹,将螺旋状的铜 丝在酒精灯上灼烧后迅速插入大试管,接触试管底部的过量的白磷(白磷在空气中燃烧的温度为40℃),然后立即塞紧橡皮塞,可观察到大试管中产生大量的白烟.试回答以下问题:(1)写出上述反应化学方程式:
(2)待试管冷却后打开弹簧夹,此时可观察到的现象为
(3)装置中砂子的作用是
(4)实验中白磷的用量要合适,若用量太少则使测出的O2与N2的体积比
 为粗略测量空气中O2与N2的体积比,某学生设计了如右图所示的实验装置进行实验.实验时,先关闭弹簧夹a,将螺旋状的铜丝在酒精灯的灼烧后迅速插入大试管,接触试管底部的过量的白磷,然后立即塞紧橡皮塞.由于白磷的着火点比红磷低得多,因此反应很容易发生,可观察到大试管中产生大量的白烟.试回答以下问题:
为粗略测量空气中O2与N2的体积比,某学生设计了如右图所示的实验装置进行实验.实验时,先关闭弹簧夹a,将螺旋状的铜丝在酒精灯的灼烧后迅速插入大试管,接触试管底部的过量的白磷,然后立即塞紧橡皮塞.由于白磷的着火点比红磷低得多,因此反应很容易发生,可观察到大试管中产生大量的白烟.试回答以下问题:(1)试配平下列化学方程式:
(2)待试管冷却后打开弹簧夹,此时可观察到的现象为
(3)如果装置气密性不好,则测出的O2与N2的体积比将
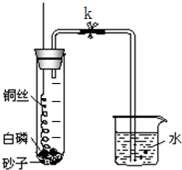 为粗略测量空气中O2与N2的体积比,某学生设计了如图所示的实验装置进行实验.实验时,先关闭弹簧夹k,将螺旋状的铜丝在酒精灯火焰上灼烧后迅速插入大试管,接触试管底部的过量的白磷,然后立即塞紧橡皮塞.由于白磷的着火点(燃烧所需的最低温度)比红磷低得多,因此反应很容易发生,可观察到大试管中产生大量的白烟.
为粗略测量空气中O2与N2的体积比,某学生设计了如图所示的实验装置进行实验.实验时,先关闭弹簧夹k,将螺旋状的铜丝在酒精灯火焰上灼烧后迅速插入大试管,接触试管底部的过量的白磷,然后立即塞紧橡皮塞.由于白磷的着火点(燃烧所需的最低温度)比红磷低得多,因此反应很容易发生,可观察到大试管中产生大量的白烟.试回答以下问题:
(1)白磷燃烧反应的符号表达式
磷+氧气
五氧化二磷
| 点燃 |
磷+氧气
五氧化二磷
;| 点燃 |
(2)待试管冷却后打开弹簧夹,此时可观察到的现象为
水倒流进试管,约占试管容积的1/5
水倒流进试管,约占试管容积的1/5
,据此可证实空气中O2与N2的体积比大约为1:4
1:4
;(3)如果装置气密性不好,则测出的O2与N2的体积比将
偏小
偏小
(填“偏大”、“偏小”、或“不变”).(4)可以选用白磷进行该实验,从反应物性质及生成物的状态等角度考虑,其中的原因有:
着火点低
着火点低
;只与氧气反应
只与氧气反应
;生成物是固体
生成物是固体
. 为粗略测量空气中O2与N2的体积比,某学生设计了如图所示的实验装置进行实验.实验时,先关闭弹簧夹k,将螺旋状的铜丝在酒精灯火焰上灼烧后迅速插入大试管,接触试管底部的过量的白磷,然后立即塞紧橡皮塞.由于白磷的着火点(燃烧所需的最低温度)比红磷低得多,因此反应很容易发生,可观察到大试管中产生大量的白烟.
为粗略测量空气中O2与N2的体积比,某学生设计了如图所示的实验装置进行实验.实验时,先关闭弹簧夹k,将螺旋状的铜丝在酒精灯火焰上灼烧后迅速插入大试管,接触试管底部的过量的白磷,然后立即塞紧橡皮塞.由于白磷的着火点(燃烧所需的最低温度)比红磷低得多,因此反应很容易发生,可观察到大试管中产生大量的白烟.试回答以下问题:
(1)白磷燃烧反应的文字或符号表达式
磷+氧气
五氧化二磷
| 点燃 |
磷+氧气
五氧化二磷
;| 点燃 |
(2)待试管冷却后打开弹簧夹,此时可观察到的现象为
水倒流进试管,约占试管容积的
| 1 |
| 5 |
水倒流进试管,约占试管容积的
,据此可证实空气中O2与N2的体积比大约为| 1 |
| 5 |
1:4
1:4
;(3)如果装置气密性不好,则测出的O2与N2的体积比将
偏小
偏小
(填“偏大”、“偏小”、或“不变”).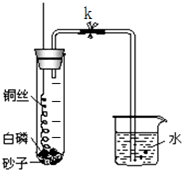 为粗略测量空气中O2与N2的体积比,某学生设计了如图所示的实验装置进行实验.实验时,先关闭弹簧夹k,将螺旋状的铜丝在酒精灯火焰上灼烧后迅速插入大试管,接触试管底部的过量的白磷,然后立即塞紧橡皮塞.由于白磷的着火点(燃烧所需的最低温度)比红磷低得多,因此反应很容易发生,可观察到大试管中产生大量的白烟.
为粗略测量空气中O2与N2的体积比,某学生设计了如图所示的实验装置进行实验.实验时,先关闭弹簧夹k,将螺旋状的铜丝在酒精灯火焰上灼烧后迅速插入大试管,接触试管底部的过量的白磷,然后立即塞紧橡皮塞.由于白磷的着火点(燃烧所需的最低温度)比红磷低得多,因此反应很容易发生,可观察到大试管中产生大量的白烟.